1 . 某实验小组探究 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。
(1)取实验2后的溶液,进行如下实验:
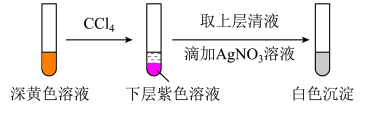
①根据______ 现象,判断实验2中有I2生成,因此反应后溶液显黄色。
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:_____ 。
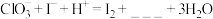
(2)查阅资料:一定条件下, 和I2都可以被氧化成
和I2都可以被氧化成 。
。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是______ 。
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。
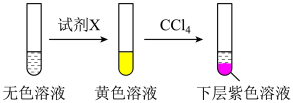
其中试剂X可以是______ (填字母)。
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 |
| 1 | 0.05mL | 浅黄色 |
2 | 0.02mL | 深黄色 | |
3 | 0.25mL | 浅黄色 | |
4 | 0.30mL | 无色 |

①根据
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:
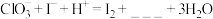
(2)查阅资料:一定条件下,
 和I2都可以被氧化成
和I2都可以被氧化成 。
。作出假设:NaClO3溶液用量增加导致溶液褪色的原因是
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。

其中试剂X可以是
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
您最近一年使用:0次
名校
解题方法
2 . 某小组研究钠与不同浓度盐酸的反应。
【实验操作】
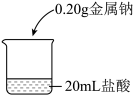
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。
【实验现象与数据】
经检验,⑤中出现的白色浑浊中的固体为NaCl。
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式:
_______ :
(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是_______ 。
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间_______ 。
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的氯化钠改变了盐酸与钠的_______ ,该因素影响了化学反应速率,进而影响了钠完全消失所用的时间。
【实验操作】
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。

【实验现象与数据】
| 编号 | ① | ② | ③ | ④ | ⑤ |
| c(HCl)/(mol·L-1) | 0.5 | 1.0 | 1.5 | 3.0 | 6.0 |
| 主要现象 | 钠浮在液面上,四处游动 | ||||
| 钠燃烧。溶液澄清 | 钠短时燃烧。溶液澄清 | 钠的表面有火花。溶液澄清 | 钠的表面。有少量火花。溶液澄清 | 钠的周围出现白色浑浊,一段时间后变澄清 | |
| 钠完全消失所用的时间/s | 11 | 21 | 37 | 65 | 114 |
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式:

(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的氯化钠改变了盐酸与钠的
您最近一年使用:0次
2023-03-15更新
|
505次组卷
|
3卷引用:2023年北京市第一次普通高中学业水平合格性考试化学试题
解题方法
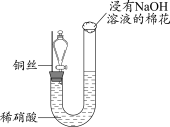
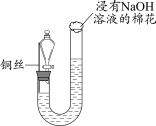
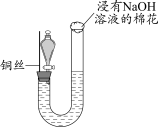
3 . 某同学研究铜与稀硝酸的反应,实验如下(夹持装置已略去,气密性良好)。
(1)HNO3中的氮元素为+5价,是氮元素的最高价态,HNO3具有_______ (填“氧化”或“还原”)性。
(2)步骤III中分液漏斗内的红棕色气体是_______ 。
(3)补全铜与稀硝酸反应的化学方程式:_______ 。_______ (写出一条即可)。
| 步骤I | 步骤II | 步骤III |
|
|
|
| 如图组装仪器并加入药品,分液漏斗旋塞关闭,U型管左侧无气体 | 将铜丝下移,一段时间后,U型管左侧产生无色气体,溶液逐渐变蓝,当液面低于铜丝时,反应逐渐停止 | 将铜丝上移,打开分液漏斗旋塞,U型管内气体进入分液漏斗立即变为红棕色,待气体全部进入分液漏斗后关闭旋塞 |
(2)步骤III中分液漏斗内的红棕色气体是
(3)补全铜与稀硝酸反应的化学方程式:
3Cu+8HNO3(稀)=3Cu(NO3)2+ _______↑+4H2O
_______↑+4H2O
您最近一年使用:0次
名校
解题方法
4 . 实验小组利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
【分析与解释】
(1)实验I中,溶解时吸收热量的物质是_______ 。
(2)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为_______ ,OH-未参与该反应的实验证据是_______ 。
(3)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,造成这种差异是由于滴加NaHCO3溶液的烧杯中有_______ (填写离子符号)参与反应。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下述实验过程的温度变化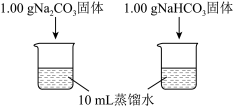 | 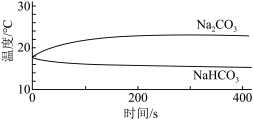 |
| 实验II | 测量下述实验过程的pH变化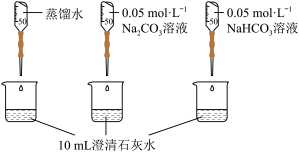 |  |
(1)实验I中,溶解时吸收热量的物质是
(2)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(3)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,造成这种差异是由于滴加NaHCO3溶液的烧杯中有
您最近一年使用:0次
2022-11-30更新
|
293次组卷
|
13卷引用:北京市2020年普通高中学业水平合格性模拟考试化学试题
北京市2020年普通高中学业水平合格性模拟考试化学试题2020年北京市第一次普通高中学业水平合格性考试化学试题北京市回民学校2020-2021学年高一上学期期中考试化学试题北京市第三十一中学2020—2021学年度高一下学期期中考试化学试题北京第七中学2020-2021学年高一下学期期中考试化学试题(已下线)北京市第四中学2022-2023学年高一上学期期中考试化学试题北京市第四十三中学2022-2023学年高一上学期期中考试化学试题北京市第八中学2022-2023学年高一下学期期末考试化学试题北京市第十一中学2023-2024学年高一上学期期中考试化学试题北京市月坛中学2023-2024学年高一上学期期中考试化学试题高一必修第一册(苏教2019)专题3 第二单元 金属钠及钠的化合物4天津市红桥区2020-2021学年高一下学期期末考试化学试题(已下线)专题八 钠及其化合物
5 . “鱼浮灵”又称固态双氧水,主要成分为2Na2CO3·3H2O2,是水产品运输过程中常用的化学增氧剂。某小组为探究溶液酸碱性对H2O2溶液中溶解氧含量的影响,进行了如下实验。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
[分析解释]
(1)H2O2发生分解反应的产物是___________ 。
(2)由实验②可知,H2O2 溶液显___________ ( 填字母)。
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是____________ 。
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有___________ 。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
| 实验编号 | ① | ② | ③ |
| 加入的试剂 | 稀硫酸 | Na2SO4溶液 | NaOH溶液 |
| pH | 0.44 | 5.97 | 11.74 |
| 溶解氧含量/ (mg·L-1) | 5.9 | 6.5 | 13.1 |
[分析解释]
(1)H2O2发生分解反应的产物是
(2)由实验②可知,H2O2 溶液显
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有
您最近一年使用:0次
解题方法
6 . 某小组同学利用下面的实验装置(气密性已检验)验证稀硝酸的性质。
(1)步骤I中,红棕色气体是 ___________ 。
(2)得出结论:铜与稀硝酸反应生成NO,所依据的实验现象是____________ 。
(3)步骤II中,生成蓝色沉淀的离子方程式是___________ 。
(4)上述实验说明稀硝酸具有的性质是酸性、___________ 。
| 实验装置 | 实验步骤 | 实验现象 |
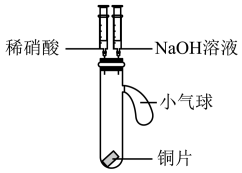 | I.向试管中加入2 mL稀硝酸 | 铜片表面产生无色气泡; 溶液逐渐变为蓝色; 试管上部气体逐渐变为红棕色 |
| II.试管上部气体变为红棕色后, 立即将NaOH溶液加入到试管中 | 溶液中产生蓝色沉淀; 试管上部气体逐渐变为无色 |
(2)得出结论:铜与稀硝酸反应生成NO,所依据的实验现象是
(3)步骤II中,生成蓝色沉淀的离子方程式是
(4)上述实验说明稀硝酸具有的性质是酸性、
您最近一年使用:0次
2021-12-25更新
|
515次组卷
|
2卷引用:2021年北京第二次普通高中学业水平合格性考试化学试题
7 . 某小组同学为验证NaHCO3受热分解的产物,设计如图实验(部分夹持装置已略去,气密性已检验)。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明NaHCO3受热分解的产物中含有___ 。
(2)实验Ⅰ中,加热试管a至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为Na2CO3。试剂X是___ 。
(3)NaHCO3受热分解的化学方程式为__ 。
(4)依据上述实验,除去Na2CO3固体中的少量NaHCO3,可采用的方法是__ 。

(1)实验Ⅰ中,澄清石灰水变浑浊,说明NaHCO3受热分解的产物中含有
(2)实验Ⅰ中,加热试管a至不再产生气体,观察到内壁有无色液滴生成,有白色固体剩余。为验证剩余白色固体的成分,小组同学设计并完成了实验Ⅱ,观察到有大量无色气体生成,证明白色固体为Na2CO3。试剂X是
(3)NaHCO3受热分解的化学方程式为
(4)依据上述实验,除去Na2CO3固体中的少量NaHCO3,可采用的方法是
您最近一年使用:0次
2021-06-28更新
|
770次组卷
|
6卷引用:北京市2021年第一次普通高中合格性考试化学试题
北京市2021年第一次普通高中合格性考试化学试题北京教育学院附属中学2022-2023学年高一上学期期中练习化学试题北京市第四十三中学2022-2023学年高一上学期期中考试化学试题北京市第三十一中学2023-2024学年高一上学期期中考试化学试题(已下线)专题2.1.2 碳酸钠和碳酸氢钠(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)(已下线)必考点07 钠盐及焰色试验-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)
名校
8 . 实验小组探究某补铁口服液中铁元素的价态。
【查阅资料】
KSCN中的硫元素为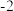 价,易被氧化为
价,易被氧化为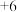 价。
价。
【实验过程】
【分析与解释】
(1)由实验Ⅰ可得出的结论是___________ 。
(2)根据实验Ⅱ中的现象,可以断定该补铁口服液中铁元素的价态为 价,滴加
价,滴加 溶液后
溶液后 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(3)一段时间后,发现实验Ⅱ中溶液红色褪去,可能的原因是___________ ;小组同学为证实自己的猜想,设计如下对照实验:向1mL 0.1 KSCN溶液中加入足量5%
KSCN溶液中加入足量5%  溶液,再加入
溶液,再加入 溶液,观察到
溶液,观察到___________ ,证实了小组同学的猜想是正确的。
【查阅资料】
KSCN中的硫元素为
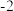 价,易被氧化为
价,易被氧化为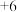 价。
价。【实验过程】
| 编号 | 实验操作 | 实验现象 |
| 实验Ⅰ |  | 无明显变化 |
| 实验Ⅱ |  | 溶液变红 |
(1)由实验Ⅰ可得出的结论是
(2)根据实验Ⅱ中的现象,可以断定该补铁口服液中铁元素的价态为
 价,滴加
价,滴加 溶液后
溶液后 发生反应的离子方程式为
发生反应的离子方程式为(3)一段时间后,发现实验Ⅱ中溶液红色褪去,可能的原因是
 KSCN溶液中加入足量5%
KSCN溶液中加入足量5%  溶液,再加入
溶液,再加入 溶液,观察到
溶液,观察到
您最近一年使用:0次
2021-06-20更新
|
599次组卷
|
5卷引用:北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题
北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题北京市第十一中学2021-2022学年高一下学期6月月考化学试题(已下线)周末培优4 金属及其化合物的实验题和工艺流程题-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)易错专题23 Fe2+和Fe3+的检验与转化-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
名校
9 . 某学习小组用下图所示实验检验浓硫酸与铜反应产生的二氧化硫(图中夹持装置已略去)。
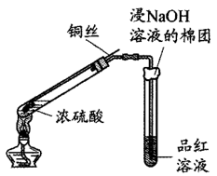
已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是___________ 。
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为___________ 。铜丝与浓硫酸反应的化学方程式为___________ 。
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是___________ 。

已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是
您最近一年使用:0次
2021-06-20更新
|
236次组卷
|
2卷引用:北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题
10 . 某学习小组用下图装置研究Cl2的性质。
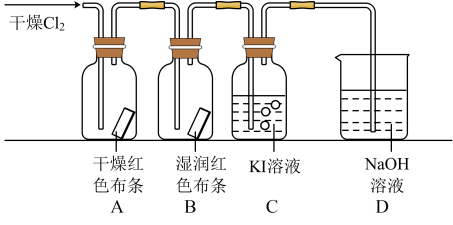
(1)观察到B中的现象是______ 。
(2)C中反应后的溶液遇淀粉变蓝,说明Cl2与KI溶液反应生成的物质有______ 。
(3)D中NaOH溶液的作用是______ 。
(4)A、B中现象不同,其原因是______ 。

(1)观察到B中的现象是
(2)C中反应后的溶液遇淀粉变蓝,说明Cl2与KI溶液反应生成的物质有
(3)D中NaOH溶液的作用是
(4)A、B中现象不同,其原因是
您最近一年使用:0次