解题方法
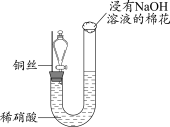
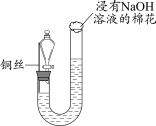
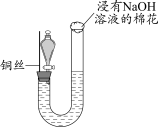
1 . 某同学研究铜与稀硝酸的反应,实验如下(夹持装置已略去,气密性良好)。
(1)HNO3中的氮元素为+5价,是氮元素的最高价态,HNO3具有_______ (填“氧化”或“还原”)性。
(2)步骤III中分液漏斗内的红棕色气体是_______ 。
(3)补全铜与稀硝酸反应的化学方程式:_______ 。_______ (写出一条即可)。
| 步骤I | 步骤II | 步骤III |
|
|
|
| 如图组装仪器并加入药品,分液漏斗旋塞关闭,U型管左侧无气体 | 将铜丝下移,一段时间后,U型管左侧产生无色气体,溶液逐渐变蓝,当液面低于铜丝时,反应逐渐停止 | 将铜丝上移,打开分液漏斗旋塞,U型管内气体进入分液漏斗立即变为红棕色,待气体全部进入分液漏斗后关闭旋塞 |
(2)步骤III中分液漏斗内的红棕色气体是
(3)补全铜与稀硝酸反应的化学方程式:
3Cu+8HNO3(稀)=3Cu(NO3)2+ _______↑+4H2O
_______↑+4H2O
您最近一年使用:0次
2 . 在实验室中,几位同学围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体。
(1)生成的黑色物质是_______ (填化学式)。
(2)有刺激性气味的气体的主要成分是_______ (填化学式)。
(3)上述实验现象表明浓硫酸具有_______(填字母)。
(1)生成的黑色物质是
(2)有刺激性气味的气体的主要成分是
(3)上述实验现象表明浓硫酸具有_______(填字母)。
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
您最近一年使用:0次
名校
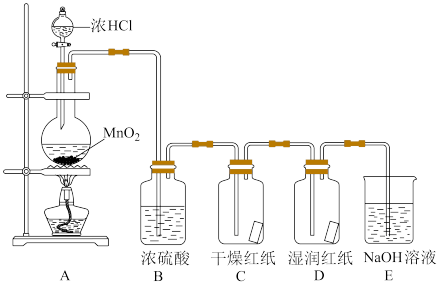
3 . 某校研究性学习小组,制取并验证氯气部分化学性质。
反应的方程式: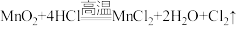 。实验装置如下图所示。
。实验装置如下图所示。
[实验探究]
(1)上述制取氯气的反应中,作氧化剂的物质是________ 。
(2)B装置中物质的作用是______ (填“干燥剂”或“氧化剂”)。
(3)E装置的作用是_______ ,反应的化学方程式为_______ 。
(4)若要制取标准状况下2.24L的 ,需要
,需要 的质量为
的质量为_______ g。
[实验讨论]
(5)有些同学对上述实验装置持有不同看法。
甲同学认为:B装置多余的
乙同学认为:B装置必需的
你认为_______ (填“甲”或“乙”)同学的看法是正确的。
[结论分析]
(6)实验现象表明,C装置中干燥的红纸不褪色,D装置中湿润的红纸褪色,说明起漂白作用的物质是_______ (填“ ”或“HClO”)
”或“HClO”)
[知识应用]
(7)氯气可用来制取很多重要化合物。写出有氯气制取盐酸的化学方程式_______ 。
反应的方程式:
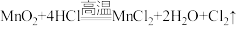 。实验装置如下图所示。
。实验装置如下图所示。
[实验探究]
(1)上述制取氯气的反应中,作氧化剂的物质是
(2)B装置中物质的作用是
(3)E装置的作用是
(4)若要制取标准状况下2.24L的
 ,需要
,需要 的质量为
的质量为[实验讨论]
(5)有些同学对上述实验装置持有不同看法。
甲同学认为:B装置多余的
乙同学认为:B装置必需的
你认为
[结论分析]
(6)实验现象表明,C装置中干燥的红纸不褪色,D装置中湿润的红纸褪色,说明起漂白作用的物质是
 ”或“HClO”)
”或“HClO”)[知识应用]
(7)氯气可用来制取很多重要化合物。写出有氯气制取盐酸的化学方程式
您最近一年使用:0次
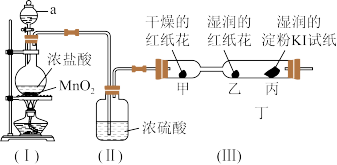
4 . 某兴趣小组用下图所示实验装置(部分夹持仪器已略去)制取并探究Cl2的性质,装置(I)中发生反应的化学方程式为: 。
。
[实验探究]
(1)装置(Ⅰ)中仪器a的名称是_______ 。
(2)装置(Ⅱ)中浓硫酸的作用是_______ 。
(3)实验进行一段时间后,装置(Ⅲ)中的实验现象与分析:
①对甲、乙两处红纸花颜色变化的描述正确的是_______ (填标号)。
A.甲不褪色,乙褪色 B.甲褪色,乙不褪色
②对比甲、乙两处实验现象,可知具有漂白性的物质是_______ (填“Cl2”或“HClO”)。
③丙处淀粉KI试纸变为_______ (填“蓝色”或“红色”),其中Cl2和KI发生反应,补充完整下面的化学方程式: _______。
_______。______
(4)从实验安全和环境保护的角度考虑,该实验存在的一个明显缺陷是_______ 。
(5)用8.7gMnO2固体与足量浓盐酸反应,可生成Cl2气体体积(标准状况下)理论上最多为_______ L。(已知MnO2的摩尔质量为87g/mol)
[知识应用]
Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。
(6)已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、 三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是_______ (填标号)。

A.3~5.5 B.5.5~7.5
 。
。
[实验探究]
(1)装置(Ⅰ)中仪器a的名称是
(2)装置(Ⅱ)中浓硫酸的作用是
(3)实验进行一段时间后,装置(Ⅲ)中的实验现象与分析:
①对甲、乙两处红纸花颜色变化的描述正确的是
A.甲不褪色,乙褪色 B.甲褪色,乙不褪色
②对比甲、乙两处实验现象,可知具有漂白性的物质是
③丙处淀粉KI试纸变为
 _______。
_______。(4)从实验安全和环境保护的角度考虑,该实验存在的一个明显缺陷是
(5)用8.7gMnO2固体与足量浓盐酸反应,可生成Cl2气体体积(标准状况下)理论上最多为
[知识应用]
Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。
(6)已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、
 三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
A.3~5.5 B.5.5~7.5
您最近一年使用:0次
2022-06-11更新
|
204次组卷
|
2卷引用:福建省福州第一中学2021-2022学年高二下学期5月学业模拟考试化学试题
5 . 干燥的氯气不能使有色布条褪色。按下图装置所示操作,观察到有色布条不褪色,则A中的试剂为
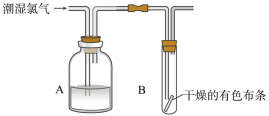

| A.水潮 | B.盐酸 | C.浓硫酸 | D.氯化钠溶液 |
您最近一年使用:0次
2022-05-23更新
|
182次组卷
|
2卷引用:海南省2020年普通高中学业水平合格性考试化学试题
解题方法
6 . 已知生石灰与水反应生成 并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
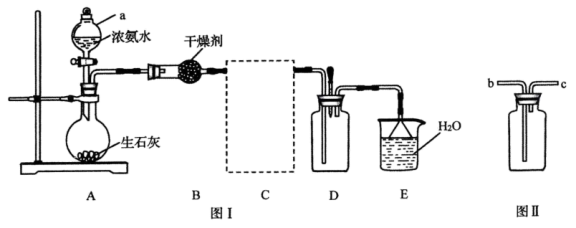
回答下列问题:
(1)仪器 的名称为
的名称为____________ ;装置 中的干燥剂为
中的干燥剂为___________ 。
(2)装置 如图Ⅱ所示,用于收集氨气,装置
如图Ⅱ所示,用于收集氨气,装置 应连接
应连接__________ (填“ ”或“
”或“ ”)。
”)。
(3)装置 中倒置漏斗的作用为
中倒置漏斗的作用为___________ 。
(4)实验进行一段时间后,挤压装置 中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为
中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为___________ ;向装置 中滴入1~2滴酚酞溶液,装置
中滴入1~2滴酚酞溶液,装置 中溶液颜色为
中溶液颜色为____________ 。
 并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
回答下列问题:
(1)仪器
 的名称为
的名称为 中的干燥剂为
中的干燥剂为(2)装置
 如图Ⅱ所示,用于收集氨气,装置
如图Ⅱ所示,用于收集氨气,装置 应连接
应连接 ”或“
”或“ ”)。
”)。(3)装置
 中倒置漏斗的作用为
中倒置漏斗的作用为(4)实验进行一段时间后,挤压装置
 中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为
中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为 中滴入1~2滴酚酞溶液,装置
中滴入1~2滴酚酞溶液,装置 中溶液颜色为
中溶液颜色为
您最近一年使用:0次
2021-10-09更新
|
540次组卷
|
3卷引用:山东省2021年普通高中合格考化学试题
7 . 应用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。某小同学通过实验探究Na2CO3和NaHCO3的性质,请你与他们一起完成实验探究过程,并回答问题。
[观察]
(1)Na2CO3和 NaHCO3均为_______ 色的固体,
(2)从物质的类别来看, Na2CO3和NaHCO3均属于化合物中的_______ 类,能溶于水,可与部分_______ 、_______ 、盐等类别的物质发生反应。
[实验过程]
(3)实验II试管B中的现象为_______ 。
[分析与解释]
(4)实验I所得实验数据证明,溶解时吸收热量的物质是_______ 。
(5)实验II中的现象证明,Na2CO3的热稳定性_______ (填“强”或“弱”)于NaHCO3
(6)实验III中的现象证明,Na2CO3盐酸反应是分步进行的,发生反应的离子方程式为:
第一步:CO + H+=HCO
+ H+=HCO ;第二步:
;第二步:_______ 。
[观察]
(1)Na2CO3和 NaHCO3均为
(2)从物质的类别来看, Na2CO3和NaHCO3均属于化合物中的
[实验过程]
| 编号 | 实验内容 | 实验数据或者现象 |
| 实验I | 利用传感器探究两种物质分别溶水时的温度变化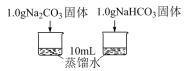 |  |
| 实验II | 探究两种物质得到热稳定性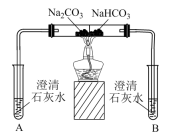 | 一段时间后,A中无明显现象,B中… |
| 实验III | 探究两种物质分别与盐酸反应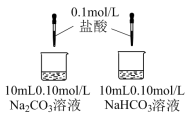 | A中开始无大量气泡,一段时间后产生大量气泡;B中立即产生大量气泡。 |
[分析与解释]
(4)实验I所得实验数据证明,溶解时吸收热量的物质是
(5)实验II中的现象证明,Na2CO3的热稳定性
(6)实验III中的现象证明,Na2CO3盐酸反应是分步进行的,发生反应的离子方程式为:
第一步:CO
 + H+=HCO
+ H+=HCO ;第二步:
;第二步:
您最近一年使用:0次
2021-07-11更新
|
639次组卷
|
5卷引用:云南省2020-2021学年高一下学期普通高中学业水平考试化学试题
名校
8 . 某学习小组用下图所示实验检验浓硫酸与铜反应产生的二氧化硫(图中夹持装置已略去)。
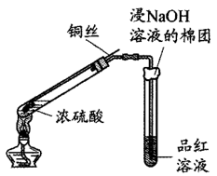
已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是___________ 。
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为___________ 。铜丝与浓硫酸反应的化学方程式为___________ 。
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是___________ 。

已知:浓硫酸的沸点为338℃,酒精灯外焰温度一般为500℃左右。
(1)浸有NaOH溶液的棉团作用是
(2)能证明铜丝与浓硫酸反应产生了SO2的实验现象为
(3)将品红溶液换为Ba(OH)2溶液,发现其中产生白色沉淀。小组同学认为此现象不足以说明Cu和浓硫酸反应产生了SO2,其原因是
您最近一年使用:0次
2021-06-20更新
|
236次组卷
|
2卷引用:北京市海淀区2020-2021学年高一下学期学业水平合格性考试适应练习化学试题
名校
9 . 研究性学习小组的同学们按下图装置进行SO2的制备及性质探究实验。(查阅资料得到SO2气体的制备原理:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O),回答问题:
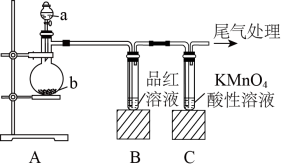
(1)图中a的仪器名称是_______ , 亚硫酸钠应放在_________ (填“a”或“b”)中。
(2)实验过程中,可以观察到装置B中品红溶液_______ (填实验现象),该现象说明SO2具有_____ 性(填“氧化”、“还原”或“漂白”)。
(3)酸性条件下,SO2与KMnO4在发生如下反应:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,使溶液褪色。反应中SO2是________ (填“氧化”、“还原”剂)。
(4)尾气可采用________ 溶液吸收。

(1)图中a的仪器名称是
(2)实验过程中,可以观察到装置B中品红溶液
(3)酸性条件下,SO2与KMnO4在发生如下反应:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,使溶液褪色。反应中SO2是
(4)尾气可采用
您最近一年使用:0次
2020-12-06更新
|
387次组卷
|
2卷引用:黑龙江省哈尔滨市南岗区哈尔滨市第三十二中学2020-2021学年高二上学期学业水平考试化学试题
10 . 某学习小组用下图装置研究Cl2的性质。
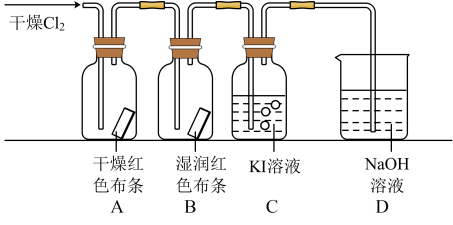
(1)观察到B中的现象是______ 。
(2)C中反应后的溶液遇淀粉变蓝,说明Cl2与KI溶液反应生成的物质有______ 。
(3)D中NaOH溶液的作用是______ 。
(4)A、B中现象不同,其原因是______ 。

(1)观察到B中的现象是
(2)C中反应后的溶液遇淀粉变蓝,说明Cl2与KI溶液反应生成的物质有
(3)D中NaOH溶液的作用是
(4)A、B中现象不同,其原因是
您最近一年使用:0次