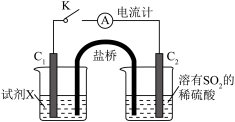
1 . 某同学用如图所示装置制备溴苯并验证其反应类型,下列说法错误的是
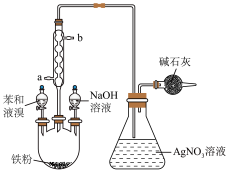
| A.将苯和液溴加入三颈烧瓶后,可观察到瓶内有红棕色气体产生 |
| B.冷凝管中冷凝水的流向为a口进,b口出 |
| C.AgNO3溶液中产生黄色沉淀即可证明该反应为取代反应 |
| D.实验结束后,应先向三颈烧瓶中加入NaOH溶液再拆卸装置 |
您最近一年使用:0次
名校
解题方法
2 . 氨是重要的化工原料,回答下列问题:
Ⅰ.制取并收集一瓶干燥氨气___________ →C→F(填大写字母)。
(2)A装置中发生反应的化学方程式为___________ 。
(3)C中盛放的试剂为___________ ,F装置的作用是___________ 。
(4)若把A装置改为B装置,以制备氨气,则分液漏斗中盛放的液体是___________ 。
Ⅱ.检验氨气的性质
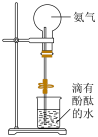
(5)装置如图,打开止水夹,用热毛巾将烧瓶捂热,松开后,水上喷形成红色喷泉,说明氨气具有___________ 等性质。
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。___________ 。
(7)实验尾气氮氧化物 折算成标准状况下的体积为a L,完全吸收时,烧杯中
折算成标准状况下的体积为a L,完全吸收时,烧杯中 至少是
至少是___________  (忽略溶液体积变化)。
(忽略溶液体积变化)。
Ⅰ.制取并收集一瓶干燥氨气
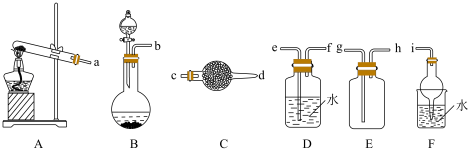
(2)A装置中发生反应的化学方程式为
(3)C中盛放的试剂为
(4)若把A装置改为B装置,以制备氨气,则分液漏斗中盛放的液体是
Ⅱ.检验氨气的性质
(5)装置如图,打开止水夹,用热毛巾将烧瓶捂热,松开后,水上喷形成红色喷泉,说明氨气具有
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。
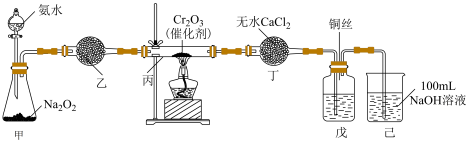
(7)实验尾气氮氧化物
 折算成标准状况下的体积为a L,完全吸收时,烧杯中
折算成标准状况下的体积为a L,完全吸收时,烧杯中 至少是
至少是 (忽略溶液体积变化)。
(忽略溶液体积变化)。
您最近一年使用:0次
名校
解题方法
3 . 学习了元素周期律可以把元素化合物知识系统地归纳起来,可以从物质的类别和元素的化合价两个方面在二维空间构造知识体系。例如:如图为S元素的价类二维图。回答下列问题:___________ ;图中所给出的物质属于含有共价键的离子化合物的是___________ (填化学式)。
(2)为验证 的相关性质,将
的相关性质,将 通入
通入 溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
(3)Y与氢氧化钠溶液反应的离子方程式为___________ 。
(4) 中各元素原子半径由大到小的顺序为
中各元素原子半径由大到小的顺序为___________ 。
(5)木炭与浓硫酸反应的化学方程式为___________ ,验证该反应的气体产物所需溶液依次为___________ 。
A.品红溶液、酸性高锰酸钾、澄清石灰水
B.澄清石灰水、澄清石灰水、品红溶液
C.澄清石灰水、氢氧化钠溶液、品红溶液

(2)为验证
 的相关性质,将
的相关性质,将 通入
通入 溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。| 滴加的溶液 | 氯水 | 氨水 |  溶液 溶液 |
| 沉淀的化学式 |
(3)Y与氢氧化钠溶液反应的离子方程式为
(4)
 中各元素原子半径由大到小的顺序为
中各元素原子半径由大到小的顺序为(5)木炭与浓硫酸反应的化学方程式为
A.品红溶液、酸性高锰酸钾、澄清石灰水
B.澄清石灰水、澄清石灰水、品红溶液
C.澄清石灰水、氢氧化钠溶液、品红溶液
您最近一年使用:0次
名校
解题方法
4 . 某小组按如下步骤探究二氧化硫与铜单质、Cu2+的反应:
ⅰ.按图示连接好装置。
ⅲ.关闭活塞b,打开活塞a.光亮的紫红色铜片很快变暗,并有黑色的Cu2S生成,同时溶液变为棕色,此时溶液中的铜元素以[CuCl3]2-(棕黄色)的形式存在。
ⅳ.静置后,取上层棕色的清液于试管中,加入一定量蒸馏水稀释,溶液中有白色沉淀CuCl析出。
(1)装置A中发生反应的化学方程式为___________ ,该反应中硫酸体现出的化学性质为___________ ;装置C的作用是___________ ,试剂m可选择___________ (填标号)。
a.饱和NaCl溶液 b.浓硫酸 c.NaOH浓溶液
(2)步骤ⅲ中,SO2在盐酸中与Cu反应的离子方程式为___________ ;步骤ⅳ中发生反应的离子方程式为[CuCl3]2-⇌CuCl↓+2Cl-,下列有关该反应的说法正确的是___________ (填标号)。
A.该反应中有电子的转移
B.反应经过足够长的时间后,[CuCl3]2-中的Cu元素能全部沉淀
C.溶液中,[CuCl3]2-和Cl-能同时存在
D.其他条件不变,当溶液的颜色不再改变时,表明该反应在该条件下达到最大限度
(3)在通风橱中利用如下装置进一步探究SO2与Cu2+的反应,盐桥(内有琼脂和饱和氯化钾溶液)用于连接两电极的电解质溶液。实验②中,闭合K后,C2电极上发生的电极反应为___________ ;不考虑其他副反应及Cu2+进入盐桥,实验②中,电路中转移0.02mole-时,左侧烧杯溶液中Cu2+的质量减少___________ g。
ⅰ.按图示连接好装置。
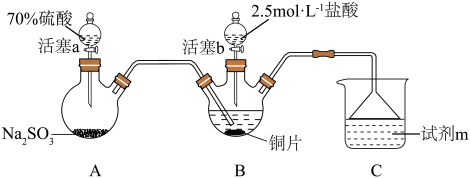
ⅲ.关闭活塞b,打开活塞a.光亮的紫红色铜片很快变暗,并有黑色的Cu2S生成,同时溶液变为棕色,此时溶液中的铜元素以[CuCl3]2-(棕黄色)的形式存在。
ⅳ.静置后,取上层棕色的清液于试管中,加入一定量蒸馏水稀释,溶液中有白色沉淀CuCl析出。
(1)装置A中发生反应的化学方程式为
a.饱和NaCl溶液 b.浓硫酸 c.NaOH浓溶液
(2)步骤ⅲ中,SO2在盐酸中与Cu反应的离子方程式为
A.该反应中有电子的转移
B.反应经过足够长的时间后,[CuCl3]2-中的Cu元素能全部沉淀
C.溶液中,[CuCl3]2-和Cl-能同时存在
D.其他条件不变,当溶液的颜色不再改变时,表明该反应在该条件下达到最大限度
(3)在通风橱中利用如下装置进一步探究SO2与Cu2+的反应,盐桥(内有琼脂和饱和氯化钾溶液)用于连接两电极的电解质溶液。实验②中,闭合K后,C2电极上发生的电极反应为
| 实验装置图 |
| ||
| 序号 | 试剂X | 实验现象 | |
| 电流计 | C1附近溶液 | ||
| ① | 0.1mol·L-1CuSO4溶液 | 指针几乎不偏转 | 无明显现象 |
| ② | 0.1mol·L-1NaCl和0.1mol·L-1CuSO4的混合溶液(足量) | 指针明显偏转 | 溶液变棕黄色 |
您最近一年使用:0次
5 . 某实验小组学习了 反应的相关知识后,欲探究镁是否与
反应的相关知识后,欲探究镁是否与 气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
(1)装置A中发生反应的化学反应方程式为___________ 。
(2)装置B中所盛放的药品是___________ (填名称),作用是___________ 。
(3)仪器a的名称是___________ ,装置D中NaOH溶液的作用是___________ 。
(4)实验完毕后观察到石棉绒上有黄色物质生成,将石棉绒及其附着物投入到稀盐酸中,会产生具有臭鸡蛋气味的H2S气体,则镁与SO2除了发生反应 外,还可能发生的反应方程式为
外,还可能发生的反应方程式为___________ 。
 反应的相关知识后,欲探究镁是否与
反应的相关知识后,欲探究镁是否与 气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
(1)装置A中发生反应的化学反应方程式为
(2)装置B中所盛放的药品是
(3)仪器a的名称是
(4)实验完毕后观察到石棉绒上有黄色物质生成,将石棉绒及其附着物投入到稀盐酸中,会产生具有臭鸡蛋气味的H2S气体,则镁与SO2除了发生反应
 外,还可能发生的反应方程式为
外,还可能发生的反应方程式为
您最近一年使用:0次
6 . 已知二氧化硫可使酸性高锰酸钾溶液褪色,化学反应方程式为:5SO2 + 2KMnO4 + 2H2O=K2SO4+ 2MnSO4 + 2H2SO4
用下图装置来验证浓硫酸与木炭在加热条件下反应后的非水产物______________
(2)实验时,反应产生的气体应从_____ 端通入;从_____ 端连接盛有澄清石灰水的实验装置(用 “a”或“b” 填空)。
(3)A瓶的实验现象是______________ 。
(4)C瓶溶液的作用是_____________ 。
用下图装置来验证浓硫酸与木炭在加热条件下反应后的非水产物
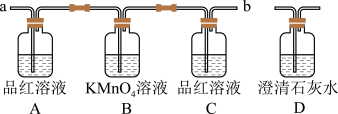
(2)实验时,反应产生的气体应从
(3)A瓶的实验现象是
(4)C瓶溶液的作用是
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
Ⅰ.自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:______________ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)Na2SO3溶液易被氧化成Na2SO4,检验Na2SO3溶液是否变质的试剂为_____________ 。
(4)铜和M的浓溶液反应生成Z的化学方程式为________________ 。
Ⅱ.氮氧化物(NOx)是大气污染物之一,处理NOx对于环境保护具有重要的意义。
在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。______________ 。
(6)在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,则该反应的化学方程式__________________ 。
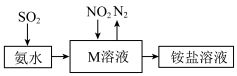
(7)工业生产中利用氨水吸收少量SO2和NO2,原理如图所示。NO2被吸收过程的离子方程式是_________________ 。
Ⅰ.自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:
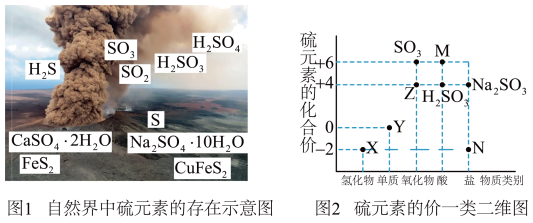
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)Na2SO3溶液易被氧化成Na2SO4,检验Na2SO3溶液是否变质的试剂为
(4)铜和M的浓溶液反应生成Z的化学方程式为
Ⅱ.氮氧化物(NOx)是大气污染物之一,处理NOx对于环境保护具有重要的意义。
在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
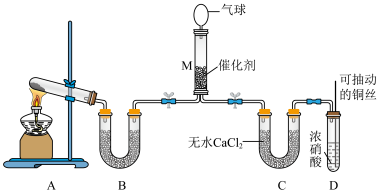
(6)在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,则该反应的化学方程式
(7)工业生产中利用氨水吸收少量SO2和NO2,原理如图所示。NO2被吸收过程的离子方程式是
您最近一年使用:0次
名校
8 . 某小组同学利用以下实验装置研究 的性质(经检验,装置的气密性良好)。
的性质(经检验,装置的气密性良好)。________ 。
(2)②中石蕊溶液变红,说明 与
与 反应生成了酸性物质。写出该反应的化学方程式:
反应生成了酸性物质。写出该反应的化学方程式:________ 。
(3)③中产生淡黄色浑浊,体现了 的
的________ (填字母)。
a.氧化性 b.还原性
(4)④中可选用________ 溶液吸收多余的 ,写出离子反应方程式
,写出离子反应方程式________ 。
 的性质(经检验,装置的气密性良好)。
的性质(经检验,装置的气密性良好)。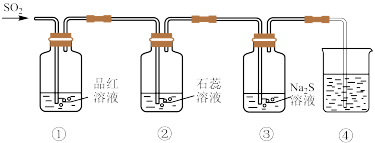
(2)②中石蕊溶液变红,说明
 与
与 反应生成了酸性物质。写出该反应的化学方程式:
反应生成了酸性物质。写出该反应的化学方程式:(3)③中产生淡黄色浑浊,体现了
 的
的a.氧化性 b.还原性
(4)④中可选用
 ,写出离子反应方程式
,写出离子反应方程式
您最近一年使用:0次
名校
解题方法
9 . 某学生配制浓硫酸与浓硝酸的混合酸,当将浓硫酸较快地加入到浓硝酸中时,在容器口产生大量白雾,下列叙述跟解释这一现象无关的是
| A.浓硫酸具有强氧化性 |
| B.硝酸具有挥发性 |
| C.浓硫酸与水作用放出大量的热使浓硝酸挥发 |
| D.硝酸蒸气容易和空气中的水蒸气结合形成白雾 |
您最近一年使用:0次
10 . 如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。_______________ 。
(2)写出实验室制取氯气的化学方程式:_________________ 。
(3)装置C中盛装的溶液是______ ,D中试剂的作用是_______ 。
(4)E中红色布条是否褪色?_______ ,F中的反应产物为______ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)______ 。
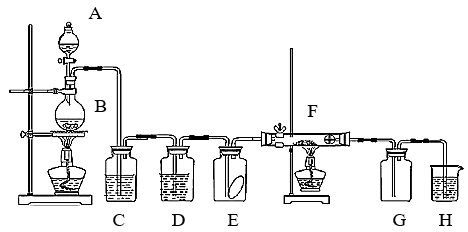
(2)写出实验室制取氯气的化学方程式:
(3)装置C中盛装的溶液是
(4)E中红色布条是否褪色?
(5)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)
您最近一年使用:0次