1 . 硫氰化钾( )俗称玫瑰红酸钾,是一种用途广泛的化学药品,主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等。实验室模拟工业生产以
)俗称玫瑰红酸钾,是一种用途广泛的化学药品,主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等。实验室模拟工业生产以 和
和 为原料制备
为原料制备 的实验装置如图所示:
的实验装置如图所示:
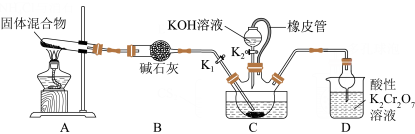
已知:① 不溶于
不溶于 ,
, 是一种密度比水大且难溶于水的液体;
是一种密度比水大且难溶于水的液体;
②三颈烧瓶内盛放 、水和催化剂,发生反应:
、水和催化剂,发生反应: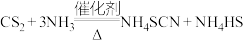 ,该反应比较缓慢,且
,该反应比较缓慢,且 在高于
在高于 下易分解。
下易分解。
(1) 装置中固体混合物是
装置中固体混合物是________ ; 中橡皮管的作用是
中橡皮管的作用是________ 。
(2)三颈烧瓶左侧导管口必须插入下层 中,其目的是使反应更充分且
中,其目的是使反应更充分且_______ 。
(3)待实验中观察到_______ 现象时,熄灭 处酒精灯,待
处酒精灯,待 中无气泡产生时关闭
中无气泡产生时关闭 。保持三颈烧瓶内液温
。保持三颈烧瓶内液温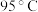 一段时间,使
一段时间,使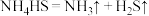 进行完全后,打开
进行完全后,打开 ,继续保持液温
,继续保持液温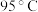 ,滴入适量的
,滴入适量的 溶液,写出生成
溶液,写出生成 的化学方程式:
的化学方程式:________ 。
(4)从 中制备得到
中制备得到 晶体,应先通过过滤除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有
晶体,应先通过过滤除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有_______ (填序号)。
①坩埚 ②蒸发皿 ③长颈漏斗 ④玻璃棒 ⑤烧杯
 )俗称玫瑰红酸钾,是一种用途广泛的化学药品,主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等。实验室模拟工业生产以
)俗称玫瑰红酸钾,是一种用途广泛的化学药品,主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等。实验室模拟工业生产以 和
和 为原料制备
为原料制备 的实验装置如图所示:
的实验装置如图所示:
已知:①
 不溶于
不溶于 ,
, 是一种密度比水大且难溶于水的液体;
是一种密度比水大且难溶于水的液体;②三颈烧瓶内盛放
 、水和催化剂,发生反应:
、水和催化剂,发生反应: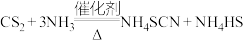 ,该反应比较缓慢,且
,该反应比较缓慢,且 在高于
在高于 下易分解。
下易分解。(1)
 装置中固体混合物是
装置中固体混合物是 中橡皮管的作用是
中橡皮管的作用是(2)三颈烧瓶左侧导管口必须插入下层
 中,其目的是使反应更充分且
中,其目的是使反应更充分且(3)待实验中观察到
 处酒精灯,待
处酒精灯,待 中无气泡产生时关闭
中无气泡产生时关闭 。保持三颈烧瓶内液温
。保持三颈烧瓶内液温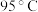 一段时间,使
一段时间,使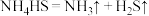 进行完全后,打开
进行完全后,打开 ,继续保持液温
,继续保持液温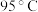 ,滴入适量的
,滴入适量的 溶液,写出生成
溶液,写出生成 的化学方程式:
的化学方程式:(4)从
 中制备得到
中制备得到 晶体,应先通过过滤除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有
晶体,应先通过过滤除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有①坩埚 ②蒸发皿 ③长颈漏斗 ④玻璃棒 ⑤烧杯
您最近一年使用:0次
名校
解题方法
2 . 三氯化碘(ICl3)在药物合成中用途广泛,实验室可用如下图装置(部分夹持装置已略去)制取。已知:①反应原理:I2+3Cl2=2ICl3;②ICl3遇水易反应。下列说法不正确 的是
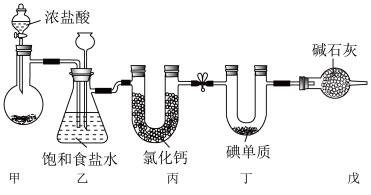

| A.ICl3中碘元素的化合价为+3 |
| B.ICl3在潮湿的空气中可能会产生白雾 |
| C.装置丙中氯化钙可用碱石灰代替 |
| D.装置戊的作用是吸收多余的氯气并防止空气中的水蒸气进入装置丁 |
您最近一年使用:0次
2022-02-20更新
|
158次组卷
|
2卷引用:浙江省桐乡市高级中学2021-2022学年高一12月阶段教学质量检测化学试题
19-20高一·浙江·阶段练习
解题方法
3 . 高铁酸钾(K2FeO4)是一种理想的绿色高效水处理剂。某小组用如图所示能置(夹持仪器略去)制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液反应制备K2FeO4。
查资料知K2FeO4的部分性质如下:
①可溶于水、微溶于浓KOH溶液;
②在0~5℃、强碱性溶液中比校稳定;
③在Fe3+和Fe(OH)3催化作用下发生分解;
④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。

请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是_________ 。
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0-5℃下进行,在不改变KOH溶液浓度前提下,实验中可以采取的措施是__________________ 。
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢加到KClO饱和溶液中可制取K2FeO4。写出该反应的化学方程式:_________ 。该操作不能将KClO饱和溶液滴加到Fe(NO3)3饱和溶液中,其原因是__________ 。
查资料知K2FeO4的部分性质如下:
①可溶于水、微溶于浓KOH溶液;
②在0~5℃、强碱性溶液中比校稳定;
③在Fe3+和Fe(OH)3催化作用下发生分解;
④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。

请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0-5℃下进行,在不改变KOH溶液浓度前提下,实验中可以采取的措施是
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢加到KClO饱和溶液中可制取K2FeO4。写出该反应的化学方程式:
您最近一年使用:0次
20-21高一上·浙江绍兴·阶段练习
名校
解题方法
4 . 氯化亚砜(SOCl2)是一种液态化合物,在农药、制药行业中用途广泛。实验室合成原理为:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,其中制取SOCl2在三颈烧瓶中进行。回答以下问题:
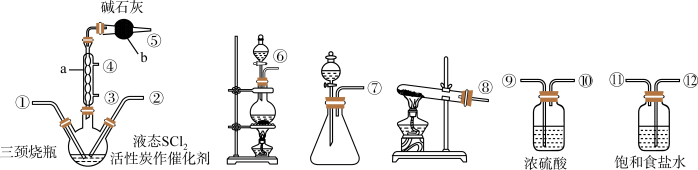
已知:①SOCl2沸点为78.8℃,SCl2的沸点为50℃,且两种液体可互溶。②SOCl2遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。
(1)部分所选仪器的连接顺序是:⑥→______ 、______ 、______ 、______ →①,制Cl2的离子方程式为______ 。
(2)仪器a的进水口为______ (填③或④),仪器b的作用是______ 。
(3)本实验中制取SO2在锥形瓶中进行,常用70%的硫酸和亚硫酸钠固体制取二氧化硫,而不是用98%的浓硫酸或稀硫酸的原因是______ 。
(4)SOCl2 与NaOH的水反应,生成三种盐,且其中两种含硫元素盐的物质的量相同,则反应的化学方程式为______ 。
(5)实验结束后,从三颈烧瓶回收活性炭催化剂的实验操作名称是______ ,获取纯净的 SOCl2的实验操作名称是______ , 若反应中消耗MnO2质量为3.48 g (设盐酸、SO2足量,生成的氯气全部逸出),最后得到纯净的SOCl2 6.00 g,则SOCl2的产率为______ 。

已知:①SOCl2沸点为78.8℃,SCl2的沸点为50℃,且两种液体可互溶。②SOCl2遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。
(1)部分所选仪器的连接顺序是:⑥→
(2)仪器a的进水口为
(3)本实验中制取SO2在锥形瓶中进行,常用70%的硫酸和亚硫酸钠固体制取二氧化硫,而不是用98%的浓硫酸或稀硫酸的原因是
(4)SOCl2 与NaOH的水反应,生成三种盐,且其中两种含硫元素盐的物质的量相同,则反应的化学方程式为
(5)实验结束后,从三颈烧瓶回收活性炭催化剂的实验操作名称是
您最近一年使用:0次



