1 . 某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2•3H2O晶体,并用滴定法测定Cu(NO3)2•3H2O晶体的纯度。
Ⅰ.设计的合成路线如图:
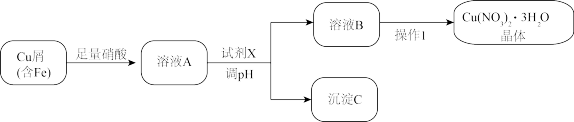
(1)试剂X是______ (填化学式),沉淀C为______ (填化学式)。
(2)操作Ⅰ的过程为______ 、过滤、洗涤等步骤。
Ⅱ.学习小组用“间接碘量法”测定Cu(NO3)2•3H2O (摩尔质量:242g•mol-1)晶体的纯度,过程如下:取0.4400g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL。
已知:I2+2S2O =S4O
=S4O +2I-
+2I-
(3)可选用______ 作滴定指示剂,滴定终点的现象是______ 。
(4)Cu(NO3)2溶液与KI反应的离子方程式为______ 。
(5)该试样中Cu(NO3)2•3H2O的质量百分数为_______ 。
(6)计算表明Cu(NO3)2•3H2O的质量百分数大于100%,可能原因是______ 。
Ⅰ.设计的合成路线如图:

(1)试剂X是
(2)操作Ⅰ的过程为
Ⅱ.学习小组用“间接碘量法”测定Cu(NO3)2•3H2O (摩尔质量:242g•mol-1)晶体的纯度,过程如下:取0.4400g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL。
已知:I2+2S2O
 =S4O
=S4O +2I-
+2I- (3)可选用
(4)Cu(NO3)2溶液与KI反应的离子方程式为
(5)该试样中Cu(NO3)2•3H2O的质量百分数为
(6)计算表明Cu(NO3)2•3H2O的质量百分数大于100%,可能原因是
您最近一年使用:0次
2 . 乙酸乙酯是应用非常广泛的有机溶剂,主要用于涂料、油墨、粘合剂、胶片、医药、化工、电子、化妆品及食品行业等。实验室可用乙酸与乙醇反应制备乙酸乙酯。
(1)为判断乙酸乙酯中与乙基(-CH2CH3)相连的氧原子的来源,请设计一种可进行判别的方案__________ 。(无需给 出实验装置实验步骤,只需给出设计思想)。
(2)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用下图所示装置进行以下四个实验,实验结束后充分振荡试管II再测有机层的厚度,实验记录如下:

①试管II中试剂的名称为_______ ,其作用是__________ 。
②分析比较实验_____ (填实验编号)的数据,可推测出浓硫酸的吸水性提高了乙酸乙酯的产率。
③分析比较实验C、D,证明对酯化反应具有催化作用的是H+。实验D中应加入盐酸的体积和浓度分别是_______ mL和_____ mol/L。
(3)现代化工生产探索以CH3CHO为原料,用(CH3CH2O)3Al作催化剂,合成乙酸乙酯:2CH3CHO CH3COOCH2CH3
CH3COOCH2CH3
在实验室中进行该实验时,不同条件下的实验结果如下表所示:
【注】选择性:转化的CH3CHO中生成CH3COOCH2CH3 的百分比。
下列说法正确的是_______ (填编号)。
A.用乙醛合成乙酸乙酯,可减少“工业三废”的排放
B.温度越高反应速率越快,乙醛的转化率越高
C.用乙醛合成乙酸乙酯的反应时间控制在12h为宜
D.催化剂用量不会影响合成反应的选择性转化率
E.(CH3CH2O)3Al是乙醛制乙酸乙酯的高效催化剂
(1)为判断乙酸乙酯中与乙基(-CH2CH3)相连的氧原子的来源,请设计一种可进行判别的方案
(2)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用下图所示装置进行以下四个实验,实验结束后充分振荡试管II再测有机层的厚度,实验记录如下:

| 编号 | 试管I中的试剂 | 有机层厚度/cm |
| A | 3 mL乙醇、2 mL乙酸、1 mL 18 mol/L浓硫酸 | 3.0 |
| B | 3 mL乙醇、2 mL乙酸 | 0.1 |
| C | 3 mL乙醇、2 mL乙酸、6 mL 3mol/L硫酸 | 1.2 |
| D | 3 mL乙醇、2 mL乙酸、盐酸 | 1.2 |
①试管II中试剂的名称为
②分析比较实验
③分析比较实验C、D,证明对酯化反应具有催化作用的是H+。实验D中应加入盐酸的体积和浓度分别是
(3)现代化工生产探索以CH3CHO为原料,用(CH3CH2O)3Al作催化剂,合成乙酸乙酯:2CH3CHO
 CH3COOCH2CH3
CH3COOCH2CH3在实验室中进行该实验时,不同条件下的实验结果如下表所示:
| 实验序号 | 催化剂用量/g | 反应温度/℃ | 反应时间/h | 副产物/% | 选择 性/% | 转化率/% |
| 1 | 0.368 | 6.5-2 | 52 | 0.35 | 99.9 | 99.6 |
| 2 | 0.278 | 10-0.5 | 52 | 0.12 | 99.81 | 95.39 |
| 3 | 0.368 | 6.5-2 | 12 | 0.1 | 99.8 | 99.7 |
| 4 | 0.368 | 10-0.5 | 52 | 0.8 | 99.5 | 97.3 |
【注】选择性:转化的CH3CHO中生成CH3COOCH2CH3 的百分比。
下列说法正确的是
A.用乙醛合成乙酸乙酯,可减少“工业三废”的排放
B.温度越高反应速率越快,乙醛的转化率越高
C.用乙醛合成乙酸乙酯的反应时间控制在12h为宜
D.催化剂用量不会影响合成反应的选择性转化率
E.(CH3CH2O)3Al是乙醛制乙酸乙酯的高效催化剂
您最近一年使用:0次
19-20高一·浙江绍兴·期末
名校
解题方法
3 . 某学习小组设计实验制备氮化锂(Li3N)并测定其纯度,装置如下所示:
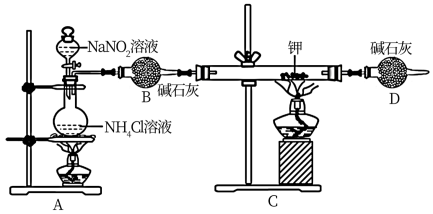
已知:i.Li3N遇水剧烈反应。
ii.实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
请回答:
(1)写出制备N2的化学方程式_______ 。
(2)仪器B的名称为_______ ;D装置的作用是_______ 。
(3)实验室将金属钠和理均可保仔在_______ 中(填相应的编号)。
a.乙醇(CH3CH2OH) b.煤油c.石蜡油d.苯
(4)测定Li3N产品纯度:取m gLi3N产品按下图所示装置进行实验。
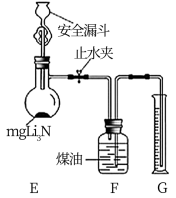
打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得气体体积为V L(已折合成标准状况下)。
①安全漏斗中“安全”含义是_______ 。
②Li3N与水反应的化学方程式_______ 。
③读数前调平F和G中液面的目的是_______ 。
④该Li3N产品的纯度为_______ %(只列出含m和V的计算式,不必计算化简)。
⑤若Li3N产品混有Li,则测得纯度_______ (选填“偏高”、“偏低”或“无影响")。(已知Li3N的相对分子质量为35)

已知:i.Li3N遇水剧烈反应。
ii.实验室用NH4Cl溶液和NaNO2溶液共热制备N2。
请回答:
(1)写出制备N2的化学方程式
(2)仪器B的名称为
(3)实验室将金属钠和理均可保仔在
a.乙醇(CH3CH2OH) b.煤油c.石蜡油d.苯
(4)测定Li3N产品纯度:取m gLi3N产品按下图所示装置进行实验。

打开止水夹,向安全漏斗中加入足量水,当Li3N完全反应后,调平F和G中液面,测得气体体积为V L(已折合成标准状况下)。
①安全漏斗中“安全”含义是
②Li3N与水反应的化学方程式
③读数前调平F和G中液面的目的是
④该Li3N产品的纯度为
⑤若Li3N产品混有Li,则测得纯度
您最近一年使用:0次



