1 . 化学来源于生活,且应用于生活。请根据题意填空:
(1)钠有多种化合物,其中加工馒头、面包等产品时,可作膨松剂的是___________ (填“ ”或“NaCl”)。
”或“NaCl”)。
(2)开盖后的铁强化酱油(铁元素以 表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由
表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由 价升高到
价升高到 价,此转化过程体现了
价,此转化过程体现了 的
的___________ (填“氧化性”或“还原性”)。
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有___________ (填“Fe2O3”或“Fe3O4”)。
(4)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于___________ (填“碱性”或“两性”)氧化物。
(5)我国发行的第五套人民币中,1角硬币的材质为铝合金。铝合金的硬度比纯铝的___________ (填“大”或“小”)。
(1)钠有多种化合物,其中加工馒头、面包等产品时,可作膨松剂的是
 ”或“NaCl”)。
”或“NaCl”)。(2)开盖后的铁强化酱油(铁元素以
 表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由
表示)久置于空气中易导致补铁效果不佳,主要原因是其中的铁元素由 价升高到
价升高到 价,此转化过程体现了
价,此转化过程体现了 的
的(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有
(4)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
(5)我国发行的第五套人民币中,1角硬币的材质为铝合金。铝合金的硬度比纯铝的
您最近半年使用:0次
名校
2 . 按要求填空或计算,(1)(2)小题为判断题。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。___________ (填“×”或“√”)
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。___________ (填“×”或“√”)
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性。
(4)Na与水反应,增大水的用量:反应速率___________ (选填“加快”、“减慢”、“不变”)。
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=___________ mol·L-1·min-1。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(4)Na与水反应,增大水的用量:反应速率
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=
您最近半年使用:0次
名校
解题方法
3 . 材料是人类赖以生存的重要物质基础。材料种类很多,通常可分为金属材料、无机非金属材料、高分子合成材料及复合材料。
(1)合金是被广泛应用的金属材料。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点_______ (填“高”或者“低”)。
②下列有关合金性质的说法不正确的是_______ (填字母)。
A.生铁和钢都属于铁碳合金,生铁的含碳量更高
B.不锈钢是在碳素钢中加入其他合金元素,改变钢的结构使其具有耐腐蚀性
C.硬铝的强度比纯铝小但耐腐蚀,可用于制造宇宙飞船等
D.储氢合金可有效解决氢能源的安全存储和运输等问题
E.铁在地壳中的含量比铜丰富,所以人类发展经历了从石器时代到铁器时代,再到青铜器时代
F.稀土元素被称为“冶金工业的维生素”,在合金中加入适量稀土金属,能大大改善合金的性能
(2)镁、铝、铁的单质及其化合物在生产和生活中有广泛的用途。回答下列问题:
①铁元素的常见化合价有 和
和 价,
价, 元素有
元素有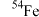 、
、 、
、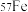 、
、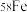 四种核素,它们互为
四种核素,它们互为_______ 。
② 、
、 、
、 、
、 、
、 (过氧化镁)中,属于碱性氧化物的有
(过氧化镁)中,属于碱性氧化物的有_______ 。
③纳米铁粉可以高效地去除被污染水体中的 等重金属离子,其本质是
等重金属离子,其本质是_______ (用离子方程式表示)。
④纳米铁粉还可用于处理含氧酸性废水中的 ,反应原理如图所示。
,反应原理如图所示。

该过程中体现了纳米铁粉的_______ 性(填“氧化”或“还原”);在铁粉总量一定的条件下,废水中的溶解氧过多不利于 的去除,原因是
的去除,原因是_______ 。
(1)合金是被广泛应用的金属材料。
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分金属的熔点
②下列有关合金性质的说法不正确的是
A.生铁和钢都属于铁碳合金,生铁的含碳量更高
B.不锈钢是在碳素钢中加入其他合金元素,改变钢的结构使其具有耐腐蚀性
C.硬铝的强度比纯铝小但耐腐蚀,可用于制造宇宙飞船等
D.储氢合金可有效解决氢能源的安全存储和运输等问题
E.铁在地壳中的含量比铜丰富,所以人类发展经历了从石器时代到铁器时代,再到青铜器时代
F.稀土元素被称为“冶金工业的维生素”,在合金中加入适量稀土金属,能大大改善合金的性能
(2)镁、铝、铁的单质及其化合物在生产和生活中有广泛的用途。回答下列问题:
①铁元素的常见化合价有
 和
和 价,
价, 元素有
元素有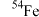 、
、 、
、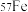 、
、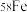 四种核素,它们互为
四种核素,它们互为②
 、
、 、
、 、
、 、
、 (过氧化镁)中,属于碱性氧化物的有
(过氧化镁)中,属于碱性氧化物的有③纳米铁粉可以高效地去除被污染水体中的
 等重金属离子,其本质是
等重金属离子,其本质是④纳米铁粉还可用于处理含氧酸性废水中的
 ,反应原理如图所示。
,反应原理如图所示。
该过程中体现了纳米铁粉的
 的去除,原因是
的去除,原因是
您最近半年使用:0次
2024-02-20更新
|
102次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
4 . 按要求回答下列问题
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:_______ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾)。取补铁剂少许溶于水配成溶液,_______ (填写实验操作、现象和结论)
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(3)镁铝合金的硬度比金属铝的硬度_______ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为_______ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3,合金中镁铝的物质的量之比为_______ 。
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾)。取补铁剂少许溶于水配成溶液,
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(3)镁铝合金的硬度比金属铝的硬度
您最近半年使用:0次
5 . 阅读下面一段材料并回答问题。
钪是一种稀土金属元素。天然稳定同位素为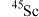 ,化合物常见价态为+3价。钪非常活泼,室温时表面被氧化形成薄膜。
,化合物常见价态为+3价。钪非常活泼,室温时表面被氧化形成薄膜。 溶于酸生成
溶于酸生成 ,溶于过量浓
,溶于过量浓 溶液生成
溶液生成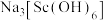 。在氮气保护下,将
。在氮气保护下,将 和金属
和金属 在高温下反应,再分离熔渣
在高温下反应,再分离熔渣 ,可制得纯度约为
,可制得纯度约为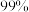 的金属钪。
的金属钪。
钪的熔点比铝的高 倍,而密度相近,适用于航空、火箭和宇宙飞船的结构材料。钪是有效的合金元素,加入镁或钛中形成合金,可使合金有较好的机械、电学和稳定性能。
倍,而密度相近,适用于航空、火箭和宇宙飞船的结构材料。钪是有效的合金元素,加入镁或钛中形成合金,可使合金有较好的机械、电学和稳定性能。
判断下列说法是否正确(填“对”或“错”)。
(1) 具有一定两性氧化物特征。
具有一定两性氧化物特征。______
(2) 与
与 制备
制备 的反应是复分解反应。
的反应是复分解反应。______
(3)制备 采用氮气保护可以防止
采用氮气保护可以防止 和
和 被空气氧化。
被空气氧化。______
(4)钪加入镁中形成合金后,合金的性能与纯金属有差异。______
钪是一种稀土金属元素。天然稳定同位素为
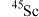 ,化合物常见价态为+3价。钪非常活泼,室温时表面被氧化形成薄膜。
,化合物常见价态为+3价。钪非常活泼,室温时表面被氧化形成薄膜。 溶于酸生成
溶于酸生成 ,溶于过量浓
,溶于过量浓 溶液生成
溶液生成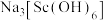 。在氮气保护下,将
。在氮气保护下,将 和金属
和金属 在高温下反应,再分离熔渣
在高温下反应,再分离熔渣 ,可制得纯度约为
,可制得纯度约为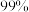 的金属钪。
的金属钪。钪的熔点比铝的高
 倍,而密度相近,适用于航空、火箭和宇宙飞船的结构材料。钪是有效的合金元素,加入镁或钛中形成合金,可使合金有较好的机械、电学和稳定性能。
倍,而密度相近,适用于航空、火箭和宇宙飞船的结构材料。钪是有效的合金元素,加入镁或钛中形成合金,可使合金有较好的机械、电学和稳定性能。判断下列说法是否正确(填“对”或“错”)。
(1)
 具有一定两性氧化物特征。
具有一定两性氧化物特征。(2)
 与
与 制备
制备 的反应是复分解反应。
的反应是复分解反应。(3)制备
 采用氮气保护可以防止
采用氮气保护可以防止 和
和 被空气氧化。
被空气氧化。(4)钪加入镁中形成合金后,合金的性能与纯金属有差异。
您最近半年使用:0次
名校
解题方法
6 . 按要求回答下列问题
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:___________ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),取补铁剂少许溶于水配成溶液,___________ (填写实验操作、现象和结论)
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是___________ ,反应的化学方程式是___________ 。
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度___________ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为___________ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3,合金中镁铝的物质的量之比为___________ 。
Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),取补铁剂少许溶于水配成溶液,
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度
您最近半年使用:0次
2024-01-08更新
|
52次组卷
|
2卷引用:吉林省长春外国语学校2023-2024学年高一上学期12月月考化学试题
7 . 合金材料在日常生活、工农业生产、国防建设等方面有重要用途。请回答下列问题:
(1)合金中至少有一种_______ (填“金属”或“非金属”)元素;目前使用量最大的合金是_______ 合金;取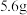 碳素钢与足量的稀盐酸充分反应后,生成氢气的体积
碳素钢与足量的稀盐酸充分反应后,生成氢气的体积_______ (填“>”“<”或“=”) (标准状况下)。
(标准状况下)。
(2)铝镁合金质优体轻,又不易锈蚀,被大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述正确的是_______(填字母)。
(3)一位收藏者有一枚表面是黑色且有少量绿色锈状物的金属货币,则这枚金属货币属于_______ 币,黑色物质是_______ (填名称),形成这种黑色物质的化学方程式为_______ ,绿色锈状物是_______ (填化学式)。
(1)合金中至少有一种
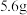 碳素钢与足量的稀盐酸充分反应后,生成氢气的体积
碳素钢与足量的稀盐酸充分反应后,生成氢气的体积 (标准状况下)。
(标准状况下)。(2)铝镁合金质优体轻,又不易锈蚀,被大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述正确的是_______(填字母)。
| A.此合金的熔点比镁和铝的熔点都高 | B.此合金能全部溶于稀盐酸中 |
| C.此合金能全部溶于氢氧化钠溶液中 | D.此合金的硬度比镁和铝的硬度都小 |
您最近半年使用:0次
解题方法
8 . 成都天府国际机场建设工程巨大,仅钢筋用量可修建11座法国埃菲尔铁塔。
(1)生铁和钢主要含铁和碳,生铁的含碳量比钢___________ 。(填“高”或“低”)
(2)铁制品锈蚀的实质是:铁与空气中的___________ 发生了化学反应。
(3)现代工业利用高炉炼铁,用赤铁矿石炼铁的原理是___________ 。(写化学方程式)
(4)某工厂利用铁与废硫酸反应制取硫酸亚铁。根据化学方程式计算,足量的铁与含 9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?________
(1)生铁和钢主要含铁和碳,生铁的含碳量比钢
(2)铁制品锈蚀的实质是:铁与空气中的
(3)现代工业利用高炉炼铁,用赤铁矿石炼铁的原理是
(4)某工厂利用铁与废硫酸反应制取硫酸亚铁。根据化学方程式计算,足量的铁与含
 9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
9.8t的废硫酸反应,可生产硫酸亚铁的质量是多少?
您最近半年使用:0次
名校
9 . 金属及金属材料广泛应用于生产、生活,其应用推动了社会的发展。
(1)下列金属应用的实例中,主要利用金属导电性的是_______(填标号)。
(2)钢铁是使用最多的金属材料。钢和生铁在性能上有较大差异的主要原因是_______ 。
(3)《天工开物》中记载“铁器淬于胆矾水中,即成铜色”,胆矾水即硫酸铜溶液,写出该反应的化学方程式_______ ,该反应的反应类型为_______ (填“氧化还原”或“非氧化还原”)反应。
(4)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是_______ (填标号)。
①Fe、Cu、Ag、稀盐酸 ②FeSO4溶液、Cu、AgNO3溶液 ③Fe、CuSO4溶液、Ag ④FeSO4溶液、CuSO4溶液、Ag ⑤FeSO4溶液、Cu、Ag
(5)将锌粉加入盛有一定量硝酸银和硝酸铜的混合溶液中,反应过程如图所示:

滤渣中一定含有_______ (填化学式)。
(1)下列金属应用的实例中,主要利用金属导电性的是_______(填标号)。
| A.铜导线 | B.银手镯 | C.铁锅 | D.金属乐器 |
(2)钢铁是使用最多的金属材料。钢和生铁在性能上有较大差异的主要原因是
(3)《天工开物》中记载“铁器淬于胆矾水中,即成铜色”,胆矾水即硫酸铜溶液,写出该反应的化学方程式
(4)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是
①Fe、Cu、Ag、稀盐酸 ②FeSO4溶液、Cu、AgNO3溶液 ③Fe、CuSO4溶液、Ag ④FeSO4溶液、CuSO4溶液、Ag ⑤FeSO4溶液、Cu、Ag
(5)将锌粉加入盛有一定量硝酸银和硝酸铜的混合溶液中,反应过程如图所示:

滤渣中一定含有
您最近半年使用:0次
10 . 合金是重要的金属材料。
(1)下列物品所使用的主要材料属于合金的是___________ (填字母)。
A.青花瓷瓶 B.橡胶充气艇 C.不锈钢锅
(2)生铁是常用的合金,生铁属于___________ (填“纯净物”或“混合物”)。
(3)黄铜是铜锌合金,将纯铜片和黄铜片互相刻划(如图所示),纯铜片上留下明显的划痕,说明___________ 。

(4)黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为不溶性杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
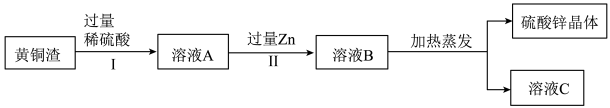
①Ⅱ中反应的化学方程式为___________ 。
②下列说法正确的是___________ (填字母)。
a.Ⅰ、Ⅱ中的操作均包含过滤
b.溶液A中ZnSO4的质量大于CuSO4
c.溶液A的质量小于溶液B
d.溶液C中溶质的质量分数小于溶液B
(1)下列物品所使用的主要材料属于合金的是
A.青花瓷瓶 B.橡胶充气艇 C.不锈钢锅
(2)生铁是常用的合金,生铁属于
(3)黄铜是铜锌合金,将纯铜片和黄铜片互相刻划(如图所示),纯铜片上留下明显的划痕,说明

(4)黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为不溶性杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):

①Ⅱ中反应的化学方程式为
②下列说法正确的是
a.Ⅰ、Ⅱ中的操作均包含过滤
b.溶液A中ZnSO4的质量大于CuSO4
c.溶液A的质量小于溶液B
d.溶液C中溶质的质量分数小于溶液B
您最近半年使用:0次



