23-24高一下·全国·课后作业
1 . 海洋中有丰富的资源,下图为海水资源利用的部分过程。下列有关说法正确的是
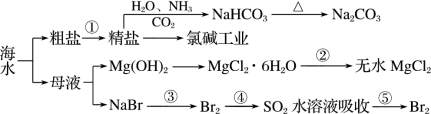
A.在第①步中除去粗盐中的 、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.操作④的目的是对溴进行富集 |
| C.工业上通过电解饱和 MgCl2溶液制取金属镁 |
D.反应④的离子方程式为:Br2+SO2+2H2O=2HBr+2H++SO |
您最近一年使用:0次
2 . 沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
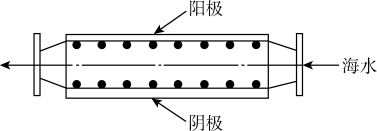
A.阳极发生将海水中的 氧化生成 氧化生成 的反应 的反应 |
B.管道中可以生成氧化灭杀附着生物的 |
C.阴极生成的 应及时通风稀释安全地排入大气 应及时通风稀释安全地排入大气 |
D.阳极表面形成的 等积垢需要定期清理 等积垢需要定期清理 |
您最近一年使用:0次
2021-06-09更新
|
24786次组卷
|
63卷引用:湖南省衡南县第一中学2022届高三下学期第二次模考化学试题
湖南省衡南县第一中学2022届高三下学期第二次模考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第一次月考化学试题湖南省株洲市九方中学2022-2023学年高三上学期第二次月考化学试题2021年高考全国乙卷化学真题(已下线)课时31 新型电解池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第17讲 电解池 金属的腐蚀与防护(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)福建省宁化第一中学2021-2022学年高二上学期开学考试化学试题江苏省苏州市2021~2022学年高二上学期期中调研化学试题(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题浙江省宁波市北仑中学2021-2022学年高二上学期期中考试化学(2-10班)试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题11 电化学-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习山西省晋城市第一中学2021-2022学年高二上学期12月月考化学试题山西省临汾市第一中学集团校2021-2022学年高二上学期期末联考化学试题(已下线)卷02 化学与STSE-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)上海市长宁区2022届高三二模考试化学试题上海市长宁区2022届高三下学期二模考试化学试题(已下线)卷05 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)押全国卷理综第11题 电化学基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点03 电化学-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题08电化学及其应用-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题08电化学及其应用-五年(2018~2022)高考真题汇编(全国卷)上海南汇中学2021-2022学年高三下学期阶段考试化学试题(已下线)第09练 以隔膜在电化学中的功能突破电解原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)微专题02 化学与STSE-备战2023年高考化学一轮复习考点微专题(已下线)考点19 电解池-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第35练 电解池-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第19讲 电解池 金属的电化学腐蚀与防护(讲)-2023年高考化学一轮复习讲练测(全国通用)福建省三明市第二中学2022-2023学年高二上学期开学适应性练习化学试题第四章 综合拔高练(已下线)第17讲 电解池 金属的腐蚀与防护 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)江苏省徐州市睢宁县第一中学2021-2022学年高二下学期第一次月考化学试题广东省东华高级中学2023届高三上学期模拟考试化学试题福建省莆田第七中学2021-2022学年高二下学期期中考试化学试题山东省青岛第十九中学2022-2023学年高二上学期期中考试化学试题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题05 化学能与电能的转化(练)-2023年高考化学二轮复习讲练测(新高考专用)辽宁省葫芦岛市兴城市高级中学等四校2022-2023学年高二上学期12月月考化学试题(已下线)化学(上海B卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)第一部分 二轮专题突破 专题11 新型电池和电解原理的应用(已下线)第六章 化学反应与能量 第37讲 电解池 金属的腐蚀与防护(已下线)题型110 惰性电极电解后溶液pH变化、电极产物的判断及探究福建省福州市八县(市、区)一中2022-2023学年高二上学期期末联考化学试题广东省茂名市电白区2021-2022学年高二下学期期中(选择性)考试化学试题(已下线)专题卷15 电解原理在工农业生产中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用(已下线)专题10 电化学及其应用-2023年高考化学真题题源解密(全国通用)作业(二十五) 电解原理的应用(已下线)考点20 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 电解池 金属的电化学腐蚀与防护吉林省长春市朝阳区长春外国语学校2022-2023学年高三上学期11月期中考试化学试题江苏省苏州市苏州高新区第一中学2023-2024学年高二上学期10月月考化学试题上海市曹杨第二中学2023-2024学年高二上学期第二次月考化学试题福建省龙岩第一中学2023-2024学年高二上学期第三次月考化学试题2024届河南省郑州市第一中学高三下学期考前全真模拟考试理科综合试题-高中化学
名校
解题方法
3 . 从海水中提取下列物质,可以不涉及到化学变化的是( )
| A.Mg | B.NaCl | C.Br2 | D.K |
您最近一年使用:0次
2020-08-15更新
|
112次组卷
|
8卷引用:2015-2016学年湖南省益阳市箴言中学高一下期末化学试卷
名校
解题方法
4 . 海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是
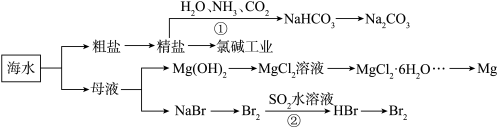
| A.由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3 |
| B.MgCl2溶液通过蒸发浓缩、冷却结晶可获得MgCl2·6H2O |
| C.反应②的离子方程式为:Br2+SO2+2H2O=SO42—+2Br—+4H+ |
| D.粗盐中含有的Mg2+、SO42—等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除 |
您最近一年使用:0次
2020-03-06更新
|
383次组卷
|
2卷引用:湖南省长沙市宁乡市2021-2022学年高一下学期期末考试化学试题
名校
5 . 海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是
| A.海水中含有钾元素,只需经过物理变化能得到钾单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Na |
| D.利用潮汐发电是将化学能转化为电能 |
您最近一年使用:0次
2019-06-20更新
|
528次组卷
|
11卷引用:湖南省长沙市铁路一中2017-2018学年高一上学期期末考试化学试题
湖南省长沙市铁路一中2017-2018学年高一上学期期末考试化学试题湖南省长沙市铁路一中2017-2018学年高一下学期期末考试化学试题湖南省张家界市2018-2019学年高一下学期期末考试化学试题【全国百强校】陕西省西安市长安区第一中学2017-2018学年高一下学期期末考试(文)化学试题四川省宜宾县第一中学校2018-2019学年高一上学期12月份考试化学试题广东省广州中大附中2018-2019学年高一下学期期末复习卷化学试题广东省第二师范学院番禺附属中学2018-2019学年高一下学期期末测试化学试题陕西省宝鸡市渭滨区2019-2020学年高一下学期期末考试化学试题新疆阿勒泰地区2019-2020学年高一下学期期末考试化学(A)试题模拟卷05(必考+选考)——2020年秋高三化学开学摸底考试卷(全国通用)课中-8.1.1 金属矿物 海水资源的开发利用-人教2019必修第二册
11-12高三·江西南昌·阶段练习
名校
6 . 海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示。下列说法不正确 的是( )
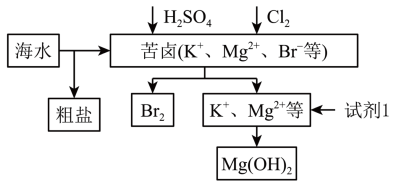

| A.可用BaCl2溶液除去粗盐中的SO42- |
| B.从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2===2Cl-+Br2 |
| C.试剂1可以选用石灰乳 |
| D.工业上,电解熔融Mg(OH)2冶炼金属镁 |
您最近一年使用:0次
2019-06-13更新
|
548次组卷
|
15卷引用:湖南省师范大学附属中学2016-2017学年高一下学期期末考试化学试题
湖南省师范大学附属中学2016-2017学年高一下学期期末考试化学试题(已下线)2013届江西省南昌二中高三第一次考试化学试卷(已下线)2013届福建省罗源县第一中学高三第一次月考化学试卷2015届山西大学附中高三12月月考化学试卷2015届北京市丰台区高三第一学期期末练习化学试卷2015-2016学年山东省淄博六中高一下学科竞赛化学试卷【全国百强校】甘肃省会宁县第一中学2017-2018学年高一下学期期末考试化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第2讲 氯及其化合物 (题型专练)【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题上海市交大附中高三2019-2020学年化学寒假自我反馈高一必修第二册(人教2019版)第八章 第一节 自然资源的开发利用 综合训练云南省楚雄市紫溪中学2019-2020学年高三上学期期末考试理综化学试题河北省安平中学2019--2020学年下学期高一第二次质量检测考试化学试题北京市西城区2021-2022学年高一下学期期末化学试题江苏省徐州市沛县歌风中学2021-2022学年高一12月学情检测化学试题
真题
名校
7 . 海水开发利用的部分过程如图所示。下列说法错误的是


| A.向苦卤中通入Cl2是为了提取溴 |
| B.粗盐可采用除杂和重结晶等过程提纯 |
| C.工业生产中常选用NaOH作为沉淀剂 |
| D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
您最近一年使用:0次
2019-01-30更新
|
7656次组卷
|
92卷引用:2016届湖南省浏阳第一中学高三上学期入学考试化学试卷
2016届湖南省浏阳第一中学高三上学期入学考试化学试卷2017届湖南省长沙市长郡中学高三上月考二化学试卷2015年全国普通高等学校招生统一考试化学(新课标II卷)2014-2015学年辽宁省沈阳二中高一下学期期末考试化学试卷2016届福建省仙游一中高三上学期10月月考化学试卷2015-2016学年西藏拉萨中学高二上第一次月考化学试卷2016届西藏拉萨中学高三上学期第二次月考化学试卷2016届黑龙江省绥化市第一中学高三上学期期中测试化学试卷2016届江西省高安市第二中学高三上学期第二次段考化学试卷2016届甘肃省张掖、嘉峪关、山丹部分高中高三上学期期中联考化学试卷2016届山东省实验中学高三上学期第二次诊断测试化学试卷2016届吉林省吉林大学附属中学高三上第一次摸底考试化学试卷2015-2016学年山西省忻州一中高二上学期期末理化学试卷2016届安徽省六安一中高三下综合训练九理综化学试卷2016届陕西省西安市长安区十中高三下学期第三次月考化学试卷2015-2016学年湖北沙市中学高一下第六次半月考化学卷2015-2016学年广东省广州市南沙区高一下学期期末考试化学试卷2015-2016学年黑龙江省实验中学高二下期末化学试卷天津市静海县第一中学2016-2017学年高一下学期期末终结性检测化学试题黑龙江省哈尔滨市第六中学2016-2017学年高二下学期期末考试化学试题辽宁省沈阳市东北育才学校2018届高三上学期第一次模拟考试化学试题2018届高三一轮复习化学:考点28-海水资源的开发利用河北省鸡泽县第一中学2018届高三上学期第一次月考化学试题广西柳州市城中区第二中学2016-2017学年高一下学期期末考试化学试题辽宁省沈阳市东北育才学校2018届高三10月月考化学试题黑龙江省牡丹江市第一高级中学2018届高三上学期期末考试化学试题2017-2018学年高中化学人教版必修2:第四章检测题(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密【全国百强校】江西省上高县第二中学2017-2018学年高一下学期期末考试化学试题【全国百强校】黑龙江省大庆中学2017-2018学年高一下学期期末考试化学试题西藏日喀则市南木林高级中学2017-2018学年高一下学期期末考试化学试题【全国百强校】广西壮族自治区桂林市第十八中学2019届高三上学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】甘肃省张掖市民乐县第一中学2019届高三上学期10月月考化学试题陕西省蓝田县焦岱中学2019届高三上学期第一次月考化学试题河南省杞县2018-2019学年高二上学期10月月考化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第2讲 氯及其化合物 (教学案)福建省莆田市第八中学2019届高三上学期期中考试化学试题【全国百强校】河北省邢台市第一中学2018-2019学年高一下学期期中考试化学试题江西省高安中学2018-2019学年高一下学期期末考试(B卷)化学试题西藏林芝一中2018-2019学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2018-2019学年高一下学期期末考试化学试题浙江省金华市2018-2019学年高一上学期期末考试化学试题云南省南华县一中2019-2020学年高二上学期开学考试化学试题福建省南安市侨光中学2020届高三上学期第一次阶段考化学试题甘肃省武威第十八中学2020届高三上学期第二次诊断考试化学试题福建省莆田市仙游县枫亭中学2020届高三上学期第二次月考化学试题8.1.1 金属矿物和海水资源的开发利用——2020年春高一新人教版第二册化学一课一练(已下线)《2020年新高考政策解读与配套资源》模拟试题06-2020年北京新高考化学模拟试题河北省承德市第一中学2019-2020学年高二下学期3月疫情期间直播课堂检测化学试题2020年春高一化学新人教版第二册课后同步:8.1.1 金属矿物和海水资源的开发利用吉林省长春市东北师大附中2020届高中毕业班四月份教学质量监测卷理科综合化学部分云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题湖北省应城市第一高级中学2019-2020学年高一下学期复学摸底测试化学试题甘肃省天水一中2020-2021学年高二上学期开学考试化学(理科)试题山西省忻州市第一中学2020-2021学年高二上学期开学考试化学试题(已下线)小题必刷16 金属元素为载体的化工流程选择题——2021年高考化学一轮复习小题必刷(通用版)吉林省洮南市第一中学2021届高三上学期期中考试化学试题高一必修第一册(苏教2019)专题3 第三单元 海洋化学资源的综合利用3黑龙江省实验中学2020-2021学年高二上学期期中考试化学试题河南省郑州市第一〇六高级中学2021届高三上学期9月月考化学试题内蒙古巴彦淖尔市临河三中2020-2021学年高二10月考化学试题江西省南昌十中2020-2021学年高二上学期开学考试化学试题陕西省西安市第一中学2021届高三上学期第五次模拟考试化学试题陕西省榆林市第十二中学2021届高三上学期第三次月考(12月)化学试题四川省南充市2019-2020学年度高二上学期期末考试化学试题江苏省沭阳县修远中学2020-2021学年高一上学期第二次月考化学试题(人教版2019)必修第二册 第八章 化学与可持续发展 第一节 自然资源的开发利用湖北省襄阳市第五中学2019-2020学年高一下学期6月月考化学试题(已下线)微专题20 海水资源的综合利用(提取溴和碘)-备战2022年高考化学考点微专题(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题(已下线)第10周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)3.3.1 粗盐提纯 从海水中提取溴(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)陕西省武功县普集高中2021-2022学年高三上学期期中考试化学试题四川省凉山宁南中学2021-2022学年高二上学期开学考试化学试题四川省凉山宁南中学2019-2020学年高二上学期开学考试化学试题福建省莆田第一中学2021-2022学年高一下学期期初学科素养能力竞赛化学试题(已下线)第26讲 海水资源的开发利用(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)(已下线)8.1.1 金属矿物和海水资源的开发利用-2021-2022学年高一化学课后培优练(人教版2019必修第二册)(已下线)考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古喀喇沁旗锦山蒙古族中学2021-2022学年高二下学期开学考试化学试题第四章 非金属及其化合物 第19讲 卤素的性质及提取四川省宜宾市叙州区第二中学校2022-2023学年高二下学期开学考试化学试题(已下线)题型46 从海水中提取氯、溴、碘(已下线)第八章 化学与可持续发展(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第02讲 氯气的性质及实验室制法-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)第07讲 氯气的性质和次氯酸-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)第八章 化学与可持续发展【单元测试A卷】河南省焦作市博爱县第一中学2023-2024学年高二下学期开学化学试题甘肃省武威市银科致远补习学校2023-2024学年高三上学期第三次调研化学试题
名校
8 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示;下列描述错误的是:


| A.淡化海水的方法主要有蒸馏法、电渗析法、离子交换法 |
| B.以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品 |
| C.步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小 |
| D.用SO2水溶液吸收Br2的离子反应方程式为:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣ |
您最近一年使用:0次
2018-08-19更新
|
647次组卷
|
12卷引用:湖南省醴陵市第一中学2017-2018学年高一下学期期末考试化学试题
湖南省醴陵市第一中学2017-2018学年高一下学期期末考试化学试题湖南省雅礼中学2019-2020学年高二上学期期中考试化学试题四川省成都市外国语学校2018-2019学年高二上学期入学考试化学试题【校级联考】湖北省孝感市六校2018-2019学年高二上学期12月月考化学试题2020届高三化学二轮对题必练——化学与STSE人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷1河北省石家庄市第二中学2019-2020学年高一下学期4月月考化学试题宁夏回族自治区银川一中2019-2020学年高一下学期期中考试化学试题江西省宜春市上高县第二中学2019-2020学年高一下学期期末考试化学试题山西省大同一中2019-2020学年高一下学期6月月考化学试题江西省新余市第四中学2021-2022学年高二上学期开学考试化学试题新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二8月分班考试化学试题
9-10高一下·广东广州·期末
名校
9 . 在开发利用金属矿物和海水资源过程中,下列说法不正确的是
| A.工业上可用电解法冶炼得到金属铝 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.海水淡化的方法主要有蒸馏法、离子交换法等 |
| D.海水中含有钾元素,需经过氧化还原反应才可得到钾单质 |
您最近一年使用:0次
2016-12-09更新
|
858次组卷
|
4卷引用:湖南省麓山国际学校人教版高中化学必修2检测第四章单元检测
湖南省麓山国际学校人教版高中化学必修2检测第四章单元检测(已下线)2009—2010学年广州市七区联考高一化学下学期期末监测福建省厦门市厦门英才学校中学部2021-2022学年高二上学期9月开学考试化学试题甘肃省兰州市第二十七中学2020-2021学年高一下学期期末考试化学试题



