解题方法
1 . Ⅰ.根据已学过的化学知识,回答下列问题:
(1)科学家称硅是“21世纪的能源”,硅在元素周期表中的位置是___________ 。
(2)常用硝酸银溶液检验氯离子,写出该反应的离子方程式___________ 。
(3)运用“纳米药物分子运输车”(如图所示)可提高治疗肿瘤的效果。回答下列问题:___________ (填“属于”或“不属于”)胶体。
②“有机物外充”中含有酒精、蔗糖、醋酸这三种有机物,其中属于电解质的是___________ 。
③Fe3O4是一种非常重要的磁性材料,可用还原铁粉与水蒸气高温制得,写出该反应的化学方程式___________ 。
(4)下列物质:N2、CO2、CH4、KOH、NaHCO3、CaO、H2SO4其中属于酸性氧化物的是___________ (写化学式,下同);属于有机物的是___________ 。
II.下表是元素周期表的一部分,除标出的元素外,表中每个序号代表一种元素,请根据要求回答问题:
(5)短周期中金属性最强的元素是___________ (填元素符号);其中形成的非金属单质不含化学键的是___________ (填化学式)。
(6)③、④、⑦三种元素按原子半径由大到小的顺序排列为___________ (用元素符号表达)。
(7)⑤、⑥的最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
(8)由H、①组成的最简单化合物所含化学键类型为___________ 写出该化合物的电子式___________ 。
(9)灼烧③、⑥形成的化合物,火焰呈___________ 。
(1)科学家称硅是“21世纪的能源”,硅在元素周期表中的位置是
(2)常用硝酸银溶液检验氯离子,写出该反应的离子方程式
(3)运用“纳米药物分子运输车”(如图所示)可提高治疗肿瘤的效果。回答下列问题:

②“有机物外充”中含有酒精、蔗糖、醋酸这三种有机物,其中属于电解质的是
③Fe3O4是一种非常重要的磁性材料,可用还原铁粉与水蒸气高温制得,写出该反应的化学方程式
(4)下列物质:N2、CO2、CH4、KOH、NaHCO3、CaO、H2SO4其中属于酸性氧化物的是
II.下表是元素周期表的一部分,除标出的元素外,表中每个序号代表一种元素,请根据要求回答问题:
| IA | 0 | ||||||||
| 1 | H | IIA | ⅢA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | Ar | ||||
| 4 | ⑦ | ||||||||
(5)短周期中金属性最强的元素是
(6)③、④、⑦三种元素按原子半径由大到小的顺序排列为
(7)⑤、⑥的最高价氧化物对应的水化物相互反应的离子方程式为
(8)由H、①组成的最简单化合物所含化学键类型为
(9)灼烧③、⑥形成的化合物,火焰呈
您最近一年使用:0次
解题方法
2 . 下列离子方程式书写正确的是
| A.Na与水反应:Na+2H2O=Na++2OH—+H2↑ |
B.碳酸氢钠溶液与稀盐酸反应:HCO +H+=H2O+CO2↑ +H+=H2O+CO2↑ |
| C.将稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
D.氯气和水反应:Cl2+H2O 2H++Cl-+ClO— 2H++Cl-+ClO— |
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 与冷的氢氧化钠溶液反应时,转移电子数为 与冷的氢氧化钠溶液反应时,转移电子数为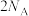 |
B.常温、常压下,7.8g过氧化钠中含有阴离子的数目为 |
C.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为 |
D.标准状况下,22.4L 与足量的铁充分反应,转移的电子数为 与足量的铁充分反应,转移的电子数为 |
您最近一年使用:0次
4 . 下列各组离子在指定的溶液中能大量共存的是
A.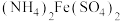 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.能使酚酞变红的溶液中: 、 、 、 、 、 、 |
C.使石蕊溶液变红色的溶液中: 、 、 、 、 、 、 |
D.0.1mol/L的 溶液中: 溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.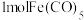 含配位键数为 含配位键数为 |
B.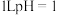 的硫酸溶液含质子数为 的硫酸溶液含质子数为 |
C.电解 溶液时阴极收集到 溶液时阴极收集到 气体(标准状况)时转移电子数为 气体(标准状况)时转移电子数为 |
D.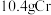 含未成对电子数为 含未成对电子数为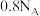 |
您最近一年使用:0次
6 . 超氧化钾( )可用作潜水或宇航装置的
)可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
吸收剂和供氧剂,反应为 ,
, 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 )可用作潜水或宇航装置的
)可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
吸收剂和供氧剂,反应为 ,
, 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.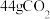 中σ键的数目为 中σ键的数目为 |
B.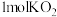 晶体中离子的数目为 晶体中离子的数目为 |
C.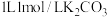 溶液中阴离子的数目大于 溶液中阴离子的数目大于 |
D.该反应中每转移1mol电子生成 的数目为 的数目为 |
您最近一年使用:0次
7 . 含氮废水进入水体中对环境造成的污染越来越严重。
(一)某校环保小组的同学认为可以用金属铝将水中的NO 还原成N2,从而消除氮污染.
还原成N2,从而消除氮污染.
(1)配平以下有关的离子反应方程式: NO
NO +
+ Al+
Al+ H2O→
H2O→ N2↑+
N2↑+ Al(OH)3+
Al(OH)3+ OH-
OH-_______ 。
(2)以上反应中失电子的物质是_______ ,还原产物是_______ ,每生成1mol还原产物,转移的电子数目为_______ 。
(3)现需除去1m3含氮0.3mol的废水中的NO (设氮元素都以NO
(设氮元素都以NO 的形式存在),则至少需要消耗金属铝的物质的量为
的形式存在),则至少需要消耗金属铝的物质的量为_______ 。
(二)2015年8月12日天津海瑞公司危险品爆炸导致NaCN泄漏,对周边的环境造成极大的威胁。
(4)NaCN遇水就会产生剧毒物质HCN,请写出其离子方程式_______ 。
(5)天津此次事故中是用双氧水来处理泄漏的NaCN,处理后产生有刺激性气味的氨气与NaHCO3,请写出该反应的化学方程式_______ 。
(6)此次事故中_______ (填“能”或“不能”)用酸性高锰酸钾来处理泄漏的NaCN。请用文字结合方程式解释_______ 。
(一)某校环保小组的同学认为可以用金属铝将水中的NO
 还原成N2,从而消除氮污染.
还原成N2,从而消除氮污染.(1)配平以下有关的离子反应方程式:
 NO
NO +
+ Al+
Al+ H2O→
H2O→ N2↑+
N2↑+ Al(OH)3+
Al(OH)3+ OH-
OH-(2)以上反应中失电子的物质是
(3)现需除去1m3含氮0.3mol的废水中的NO
 (设氮元素都以NO
(设氮元素都以NO 的形式存在),则至少需要消耗金属铝的物质的量为
的形式存在),则至少需要消耗金属铝的物质的量为(二)2015年8月12日天津海瑞公司危险品爆炸导致NaCN泄漏,对周边的环境造成极大的威胁。
(4)NaCN遇水就会产生剧毒物质HCN,请写出其离子方程式
(5)天津此次事故中是用双氧水来处理泄漏的NaCN,处理后产生有刺激性气味的氨气与NaHCO3,请写出该反应的化学方程式
(6)此次事故中
您最近一年使用:0次
8 . 下列实验现象描述正确的是
| A.碘水中加入少量裂化汽油振荡,静置后上层颜色变浅,下层颜色变为紫红色 |
| B.红热的铜丝在氯气中燃烧,产生了棕黄色的雾 |
| C.电解氯化钠饱和溶液,将阳极气体产物通入碘化钾淀粉溶液中,溶液变蓝 |
| D.溴化钠溶液中加入少量新制的氯水振荡,再加入少量四氯化碳溶液振荡,静置后上层颜色变浅,下层颜色变为橙红色 |
您最近一年使用:0次
9 . 解释下列反应原理的离子方程式正确的是
| A.用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+ |
B.用小苏打治疗胃酸过多:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| C.用氯化铁溶液腐蚀印刷线路板上的铜:Fe3++Cu=Fe2++Cu2+ |
D.含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO +Ba2++OH-=BaCO3↓+H2O +Ba2++OH-=BaCO3↓+H2O |
您最近一年使用:0次
10 . 已知下述三个实验均能发生化学反应.下列判断正确的是
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铜丝放入氯化铁溶液中 |
| A.上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
| B.实验①中铁钉只作还原剂 |
| C.实验②中Fe2+既显氧化性又显还原性 |
| D.实验③中发生的是置换反应 |
您最近一年使用:0次



