名校
1 . 下列说法正确的是
A.Cr原子结构示意图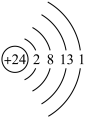 |
B.铍原子最外层的电子云图为 |
C.基态Cu原子的价层电子轨道表示式为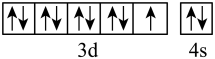 |
D.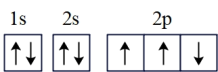 ,该轨道表示式违背了泡利不相容原理 ,该轨道表示式违背了泡利不相容原理 |
您最近一年使用:0次
名校
2 . X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、组成蛋白质的重要元素;Z的基态原子核外9个原子轨道上都填充了电子且有2个未成对电子;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1) 分子中存在的σ键和π键个数之比为
分子中存在的σ键和π键个数之比为___________ 。
(2)X的第一电离能比Y的___________ (填“大”或“小”)。
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液加热会反应会生成可以使品红溶液褪色的物质,写出化学方程式:___________ 。
(4)W的基态原子的价层电子排布式为___________ 。
(5)X、Y的最简单氢化物的VSEPR模型分别为___________ 、___________ 。
(1)
 分子中存在的σ键和π键个数之比为
分子中存在的σ键和π键个数之比为(2)X的第一电离能比Y的
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液加热会反应会生成可以使品红溶液褪色的物质,写出化学方程式:
(4)W的基态原子的价层电子排布式为
(5)X、Y的最简单氢化物的VSEPR模型分别为
您最近一年使用:0次
名校
3 . 用 粒子轰击
粒子轰击 可得到一个中子和一种放射性核素
可得到一个中子和一种放射性核素 ,即
,即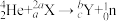 。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是
。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是
 粒子轰击
粒子轰击 可得到一个中子和一种放射性核素
可得到一个中子和一种放射性核素 ,即
,即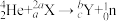 。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是
。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是| A.b=13 | B.最高价含氧酸的酸性:X<Y |
| C.XF3与YF3中X与Y的杂化方式相同 | D.Y的某种氢化物中含非极性键 |
您最近一年使用:0次
名校
4 . 第三周期元素的单质及其化合物具有重要用途。例如,在熔融状态下,可用金属钠制备金属钾;MgCl2可制备多种镁产品:铝-空气电池具有较高的比能量,在碱性电解液中总反应式为4Al+3O2+4OH-+6H2O=4[Al(OH)4]-,高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氟硅烷(SiHCl3),再经氢气还原得到高纯硅。下列说法正确的是
| A.钠燃烧时火焰呈黄色与电子跃迁有关,焰色反应是化学变化 |
| B.Mg2+基态核外电子排布式为1s22s22p63s2 |
| C.1mol[Al(OH)4]-中含有4molσ键 |
| D.Si-Si键的键能小于Si-O键的键能 |
您最近一年使用:0次
名校
5 . 下列说法正确的是
| A.电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理 |
| B.p轨道电子能量一定高于s轨道电子能量 |
| C.杂化轨道既可以形成σ键,也可以形成π键 |
| D.根据原子核外电子排布的特点,Zn在元素周期表中位于d区 |
您最近一年使用:0次
名校
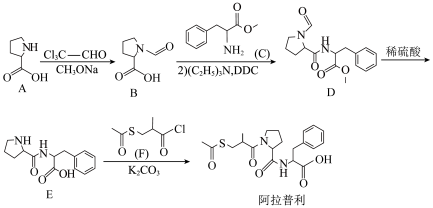
6 . 阿拉普利是治疗高血压的长效药,合成路线如图:
(1)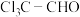 中官能团的名称为
中官能团的名称为_______ 。
(2)写出A→B的化学方程式:_______ ;制备E的过程中,设计A→B的目的是_______ 。
(3)E和F反应生成阿拉普利的反应类型是_______ ; 的作用是
的作用是_______ 。
(4)阿拉普利分子中含有_______ 个手性碳原子。
(5)C的芳香族同分异构体中,同时具备下列条件的结构有_______ 种(不包括立体异构体)。
①既能发生银镜反应,又能发生水解反应
②苯环上只有两种取代基,且其中一个为
其中核磁共振氢谱显示有五组峰,且峰面积比为6:2:2:2:1的结构简式为_______ 。
(1)
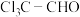 中官能团的名称为
中官能团的名称为(2)写出A→B的化学方程式:
(3)E和F反应生成阿拉普利的反应类型是
 的作用是
的作用是(4)阿拉普利分子中含有
(5)C的芳香族同分异构体中,同时具备下列条件的结构有
①既能发生银镜反应,又能发生水解反应
②苯环上只有两种取代基,且其中一个为

其中核磁共振氢谱显示有五组峰,且峰面积比为6:2:2:2:1的结构简式为
您最近一年使用:0次
7日内更新
|
393次组卷
|
4卷引用:2024届青海省海南藏族自治州高三下学期二模理综试题-高中化学
7 . 40Zr与22Ti同族,ZrO2有3种常见晶胞结构,最为常见的是立方ZrO2(晶胞为立方体)、四方ZrO2(晶胞为长方体,其底面为正方形),立方ZrO2性质与钻石接近,可加工为璀璨夺目的饰品。_______ 。
(2)如图所示立方ZrO2的晶胞中,位于顶点的原子是_______ 。
(3)如图所示四方ZrO2的晶胞中,每个O原子周围,距离“最近”的Zr原子与其距离为207pm或246pm,其余Zr原子距离明显远于300pm,距离每个O原子“最近”的Zr原子共_______ 个。

(2)如图所示立方ZrO2的晶胞中,位于顶点的原子是
(3)如图所示四方ZrO2的晶胞中,每个O原子周围,距离“最近”的Zr原子与其距离为207pm或246pm,其余Zr原子距离明显远于300pm,距离每个O原子“最近”的Zr原子共
您最近一年使用:0次
8 . 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Ni、Fe、Mn等元素。回答下列问题:
(1)下列不同状态的硼中,用光谱仪可捕捉到发射光谱的是_______ 。(填标号)
(2)镍能形成多种配合物,其中Ni(CO)4是无色挥发性液体,K2[Ni(CN)4]是红黄色单斜晶体。K2[Ni(CN)4]的熔点高于Ni(CO)4的原因是_______ 。
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。_______ 。
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为_______ 。
(4)FeSO4•7H2O的结构如图所示,FeSO4•7H2O中∠1、∠2、∠3由大到小的顺序是_______ 。_______ 。
②该锰的硅化物的化学式为_______ 。
(1)下列不同状态的硼中,用光谱仪可捕捉到发射光谱的是
A. |
B. |
C. |
D. |
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。

②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为
(4)FeSO4•7H2O的结构如图所示,FeSO4•7H2O中∠1、∠2、∠3由大到小的顺序是


②该锰的硅化物的化学式为
您最近一年使用:0次
名校
9 . 氮气可以作食品包装、灯泡等的填充气,也是合成纤维、合成橡胶的重要原料。实验室制备氮气的反应式:NH4Cl+NaNO2 NaCl+N2↑+2H2O。下列说法正确的是
NaCl+N2↑+2H2O。下列说法正确的是
 NaCl+N2↑+2H2O。下列说法正确的是
NaCl+N2↑+2H2O。下列说法正确的是| A.离子半径:r(Na+)>r(N3-)>r(O2-) |
| B.氮元素基态原子核外未成对电子数为1 |
C.钠电离最外层一个电子所需要的能量:① >② >② |
| D.水中的氢键可以表示为:O-H…O,其中H…O之间的距离即为该氢键的键长 |
您最近一年使用:0次
名校
解题方法
10 . 钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题:
① 具有强氧化性。
具有强氧化性。
② ,
, 。
。
(1)为提高含钴废料的浸出效率,可采取的措施是___________ (任写一条)。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ ;浸出渣的主要成分为___________ (填化学式)。
(3)向“浸出液”中加入适量的 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)①“除钙镁”后,滤液中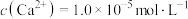 时,
时,
___________  。
。
②若“调pH”时溶液的pH偏低,将会导致 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
(5)将 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: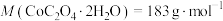 ,曲线中330℃及以上所得固体均为钴氧化物]
,曲线中330℃及以上所得固体均为钴氧化物] ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为___________ 。
 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题: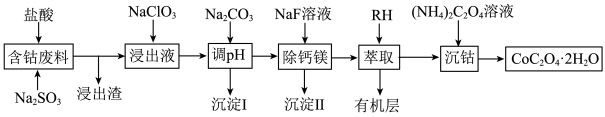
①
 具有强氧化性。
具有强氧化性。②
 ,
, 。
。(1)为提高含钴废料的浸出效率,可采取的措施是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)向“浸出液”中加入适量的
 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为(4)①“除钙镁”后,滤液中
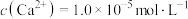 时,
时,
 。
。②若“调pH”时溶液的pH偏低,将会导致
 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是(5)将
 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: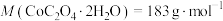 ,曲线中330℃及以上所得固体均为钴氧化物]
,曲线中330℃及以上所得固体均为钴氧化物]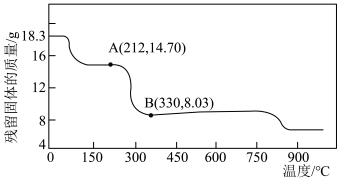
 ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为
您最近一年使用:0次
7日内更新
|
205次组卷
|
5卷引用:2024届青海省西宁市大通县高三下学期高考四模理科综合试卷-高中化学



