名校
1 . 根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将镁条用砂纸打磨过后,点燃,放入盛有 的集气瓶中,镁条燃烧。将铝条用砂纸打磨过后,点燃,放入盛有 的集气瓶中,镁条燃烧。将铝条用砂纸打磨过后,点燃,放入盛有 的集气瓶中,铝条不燃烧。 的集气瓶中,铝条不燃烧。 | Mg的金属性强于Al |
| B | 向盛有碳酸钙固体的锥形瓶中加入足量盐酸,将产生的气体通入到硅酸钠溶液中,产生白色沉淀 | C的非金属性强于Si |
| C | 将银和 溶液与铜和 溶液与铜和 溶液组成原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 溶液组成原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 | Cu的金属性比Ag强 |
| D | 往碘的 溶液中加入等体积浓KI溶液,振荡。分层,下层由紫红色变为浅粉红色,上层呈棕黄色。 溶液中加入等体积浓KI溶液,振荡。分层,下层由紫红色变为浅粉红色,上层呈棕黄色。 | 碘在浓KI溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 亚铁氰化钾 俗名黄血盐,在烧制青花瓷时用于绘画。一种制备方法为
俗名黄血盐,在烧制青花瓷时用于绘画。一种制备方法为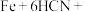
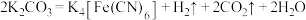 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 俗名黄血盐,在烧制青花瓷时用于绘画。一种制备方法为
俗名黄血盐,在烧制青花瓷时用于绘画。一种制备方法为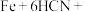
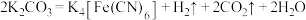 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.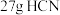 分子中含有 分子中含有 键的数目为 键的数目为 |
B.配合物 的中心离子为 的中心离子为 |
C.每生成 时,反应过程中转移电子的数目为 时,反应过程中转移电子的数目为 |
D. 中碳原子的价层电子对数目为4 中碳原子的价层电子对数目为4 |
您最近一年使用:0次
名校
解题方法
3 . 下列反应的离子方程式正确的是
A. 与 与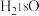 反应: 反应: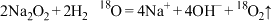 |
B.用 溶液吸收废气中的 溶液吸收废气中的 : : |
C. 与稀硝酸反应:当 与稀硝酸反应:当 时, 时,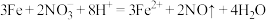 |
D. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
您最近一年使用:0次
解题方法
4 . 苯与 的反应机理及能量与反应进程的关系如图。已知
的反应机理及能量与反应进程的关系如图。已知 越小,该步反应速率越快。下列说法正确的是
越小,该步反应速率越快。下列说法正确的是
 的反应机理及能量与反应进程的关系如图。已知
的反应机理及能量与反应进程的关系如图。已知 越小,该步反应速率越快。下列说法正确的是
越小,该步反应速率越快。下列说法正确的是

A.反应过程中 为催化剂 为催化剂 |
| B.三步反应均为吸热反应 |
| C.反应过程中有碳碳双键的断裂和生成 |
D.苯和 反应的速率由反应②的速率决定 反应的速率由反应②的速率决定 |
您最近一年使用:0次
真题
解题方法
5 . 以不同材料修饰的 为电极,一定浓度的
为电极,一定浓度的 溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制
溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制 和
和 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
 为电极,一定浓度的
为电极,一定浓度的 溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制
溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制 和
和 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
| A.电极a连接电源负极 |
B.加入Y的目的是补充 |
C.电解总反应式为 |
D.催化阶段反应产物物质的量之比 |
您最近一年使用:0次
名校
解题方法
6 . CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料:
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量、有效地开发利用CO2,工业上可以用CO2来生产甲醇。在体积为2L的密闭容器中,充入1mol CO2和3molH2,一定条件下发生反应: 。测得
。测得 和CO2的物质的量随时间变化如图所示:
和CO2的物质的量随时间变化如图所示:___________ v逆(填“>”、“<”或“=”)。
②从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
③达到平衡时,H2的浓度为___________ mol⋅L-1。
(2)工业上也可以用CO和H2为原料制备CH3OH,反应的化学方程式为: ,在一定温度下,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________(填字母序号)。
,在一定温度下,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________(填字母序号)。
(3)某种甲烷燃料电池的工作原理如图所示。___________ 极,将上图中的甲烷改为二甲醚(CH3OCH3)就构成了碱性二甲醚燃料电池,通CH3OCH3的电极的电极反应式为:___________________ 。当电路中有2mol电子通过时,消耗标准状况下氧气的体积为___________ L。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量、有效地开发利用CO2,工业上可以用CO2来生产甲醇。在体积为2L的密闭容器中,充入1mol CO2和3molH2,一定条件下发生反应:
 。测得
。测得 和CO2的物质的量随时间变化如图所示:
和CO2的物质的量随时间变化如图所示: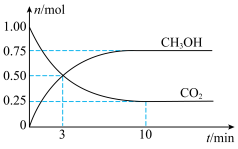
②从反应开始到平衡,CO2的平均反应速率v(CO2)=
③达到平衡时,H2的浓度为
(2)工业上也可以用CO和H2为原料制备CH3OH,反应的化学方程式为:
 ,在一定温度下,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________(填字母序号)。
,在一定温度下,在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________(填字母序号)。| A.反应体系中CO与CH3OH的物质的量之比为1∶1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1molCO、同时生成lmol CH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
(3)某种甲烷燃料电池的工作原理如图所示。

您最近一年使用:0次
今日更新
|
84次组卷
|
2卷引用:山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高一下学期期中考试化学试题
名校
7 . 下列说法中,正确的有个
①过氧化钠与水反应中,既有离子键、极性共价键和非极性共价键的断裂,也有这些化学键的生成
②同位素的性质完全相同
③两种原子构成的共价化合物分子中的化学键都是极性键
④气体单质分子中一定含有共价键
⑤5.6g铁粉与足量的稀盐酸反应,为了加快反应速率而不改变H2的产量,可以滴入几滴硫酸铜溶液
⑥决定反应速率的主要因素是反应物本性
⑦同温同压下,等物质的量的H2(g),Cl2(g),在光照和点燃条件下发生反应H2(g)+Cl2(g)=2HCl(g)时,放出的能量相同
①过氧化钠与水反应中,既有离子键、极性共价键和非极性共价键的断裂,也有这些化学键的生成
②同位素的性质完全相同
③两种原子构成的共价化合物分子中的化学键都是极性键
④气体单质分子中一定含有共价键
⑤5.6g铁粉与足量的稀盐酸反应,为了加快反应速率而不改变H2的产量,可以滴入几滴硫酸铜溶液
⑥决定反应速率的主要因素是反应物本性
⑦同温同压下,等物质的量的H2(g),Cl2(g),在光照和点燃条件下发生反应H2(g)+Cl2(g)=2HCl(g)时,放出的能量相同
| A.5 | B.4 | C.3 | D.2 |
您最近一年使用:0次
今日更新
|
46次组卷
|
2卷引用:山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高一下学期期中考试化学试题
8 . 以磁铁矿(主要含有 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备优良的吸附剂水合氧化铁(
等杂质)为原料制备优良的吸附剂水合氧化铁(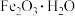 ),工艺流程如下。
),工艺流程如下。
(1)Fe在元素周期表中的位置为______________ 。
(2)“粉碎”的目的是______________ 。“碱浸”时发生反应的离子方程式为______________ 。
(3)“滤渣1”的主要成分有______________ 。“试剂X”的化学式为________________ 。
(4)“沉铁”时发生反应的离子方程式为_________________ 。
(5)以含铁60%的100t磁铁矿为原料生产水合氧化铁,生产过程中加入“试剂X”20t,“沉铁”时损耗铁元素3%,则可生产纯度为97%的水合氧化铁_________________ t(保留一位小数)。
 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备优良的吸附剂水合氧化铁(
等杂质)为原料制备优良的吸附剂水合氧化铁(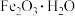 ),工艺流程如下。
),工艺流程如下。
(1)Fe在元素周期表中的位置为
(2)“粉碎”的目的是
(3)“滤渣1”的主要成分有
(4)“沉铁”时发生反应的离子方程式为
(5)以含铁60%的100t磁铁矿为原料生产水合氧化铁,生产过程中加入“试剂X”20t,“沉铁”时损耗铁元素3%,则可生产纯度为97%的水合氧化铁
您最近一年使用:0次
解题方法
9 . 为探究卤族元素单质及其化合物的性质设计了如下实验方案。由下列操作、现象能得出相应结论的是
操作 | 现象 | 结论 | |
| A | 向两份新制氯水中,分别滴加淀粉KI溶液和 溶液 溶液 | 前者溶液变蓝,后者溶液产生白色沉淀 | 氯气与水的反应存在限度 |
| B | 用玻璃棒蘸取“84”消毒液点在pH试纸上 | 试纸变白 | “84”消毒液呈中性 |
| C | 将少量 溶液滴入 溶液滴入 溶液中 溶液中 | 紫色很快褪去 | 氧化能力: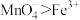 |
| D | 向碘的 溶液中加入等体积KI浓溶液,振荡、静置 溶液中加入等体积KI浓溶液,振荡、静置 | 分层,上层呈棕褐色,下层呈浅红色 | 碘在浓KI溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 汽车安全气囊可充入叠氮化钠( )、硝酸钾、
)、硝酸钾、 、
、 等物质,主要反应为
等物质,主要反应为 ,下列说法错误的是
,下列说法错误的是
 )、硝酸钾、
)、硝酸钾、 、
、 等物质,主要反应为
等物质,主要反应为 ,下列说法错误的是
,下列说法错误的是| A.叠氮化钠和硝酸钾均为含有共价键的离子化合物 |
B. 粉末可作冷却剂吸收产气过程中释放的热量 粉末可作冷却剂吸收产气过程中释放的热量 |
C.标准状况下产生 时转移 时转移 |
D. 可与产物 可与产物 、 、 反应生成无腐蚀性的硅酸盐,减少对人体的伤害 反应生成无腐蚀性的硅酸盐,减少对人体的伤害 |
您最近一年使用:0次



