名校
1 . 下图为元素周期表的一部分。请回答下列问题:
(1)C的最简单氢化物的分子式为____________ ;
(2)N的简单氢化物溶于水,所得溶液显____________ (填“酸性”或“碱性”);
(3)F和Cl的非金属性强弱:F____________ Cl(填“>”或“<”);
(4)Cl的氢化物的水溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为_____________ 。
C | N | F | |
Cl |
(2)N的简单氢化物溶于水,所得溶液显
(3)F和Cl的非金属性强弱:F
(4)Cl的氢化物的水溶液与
 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 乙醇和乙酸是生活中常见的有机化合物。请根据题意填空:
(1)乙酸的工业制法: ,该反应的类和属于
,该反应的类和属于____________ (填“取代”或“加成”)反应;
(2)乙醇在加热、催化剂(Cu或Ag)的条件下,能被空气中的氧气氧化为 ,产物
,产物 的官能团名称是
的官能团名称是____________ (填“羟基”或“醛基”);
(3)乙醇、乙酸和小苏打( )是生活中常见的物质,其中能与小苏打反应的物质是
)是生活中常见的物质,其中能与小苏打反应的物质是____________ (填“乙醇”或“乙酸”)。
(1)乙酸的工业制法:
 ,该反应的类和属于
,该反应的类和属于(2)乙醇在加热、催化剂(Cu或Ag)的条件下,能被空气中的氧气氧化为
 ,产物
,产物 的官能团名称是
的官能团名称是(3)乙醇、乙酸和小苏打(
 )是生活中常见的物质,其中能与小苏打反应的物质是
)是生活中常见的物质,其中能与小苏打反应的物质是
您最近一年使用:0次
名校
解题方法
3 . 金属元素在生产、生活中扮演着重要角色。请根据题意填空:
(1)钠有多种化合物,医疗上常用作抗酸药的是____________ (填“NaOH”或“ ”);
”);
(2)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是____________ (填“FeO”或“ ”);
”);
(3)铝热反应原理常用于金属的冶炼,制取金属钒的反应原理为 ,该反应的氧化剂是
,该反应的氧化剂是____________ 。
(1)钠有多种化合物,医疗上常用作抗酸药的是
 ”);
”);(2)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
 ”);
”);(3)铝热反应原理常用于金属的冶炼,制取金属钒的反应原理为
 ,该反应的氧化剂是
,该反应的氧化剂是
您最近一年使用:0次
名校
4 . 海水是人类的资源宝库。回答下列问题:
(1)仪器C的名称是_______ 。
(2)装置B中进水口应为_______ (填“a”或“b”)。
Ⅱ.空气吹出法是海水提溴的常用方法。其中一种工艺流程为
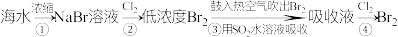
(3)在步骤③中发生反应: ,反应中
,反应中 是
是_______ (填“氧化”或“还原”)剂。
(4)在步骤③中,每吸收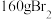 ,理论上需要通入
,理论上需要通入_______ (标准状况下)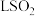 。
。
(5)步骤④发生的反应类型是_______ (填“置换”或“复分解”)反应。
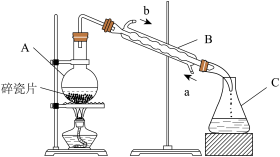
(1)仪器C的名称是
(2)装置B中进水口应为
Ⅱ.空气吹出法是海水提溴的常用方法。其中一种工艺流程为
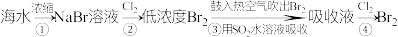
(3)在步骤③中发生反应:
 ,反应中
,反应中 是
是(4)在步骤③中,每吸收
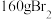 ,理论上需要通入
,理论上需要通入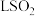 。
。(5)步骤④发生的反应类型是
您最近一年使用:0次
昨日更新
|
118次组卷
|
2卷引用:湖南省普通高中2023-2024学年高一下学期学业水平合格性考试模拟化学试卷四
5 . 工业上以海水为原料富集镁并冶炼金属镁,其流程如图:
(1)海水中含有大量MgCl2、NaCl和CaCl2,它们属于______ (填“酸”或“盐”)。
(2)熟石灰溶于水,所得的溶液呈______ (填“酸性”或“碱性”)。
(3)冶炼镁(操作Ⅱ)的方法属于______ (填“电解法”或“热分解法”)。
(4)工业上制取光气(COCl2)的反应: 。某体积为2 L的恒容反应器中发生上述反应,Cl2的物质的量与时间的关系如图。则:
。某体积为2 L的恒容反应器中发生上述反应,Cl2的物质的量与时间的关系如图。则:______  ;
;
②其他条件不变时,往反应器中通入氩气(不参与反应),该反应的反应速率______ (填“增大”或“不变”)。

(1)海水中含有大量MgCl2、NaCl和CaCl2,它们属于
(2)熟石灰溶于水,所得的溶液呈
(3)冶炼镁(操作Ⅱ)的方法属于
(4)工业上制取光气(COCl2)的反应:
 。某体积为2 L的恒容反应器中发生上述反应,Cl2的物质的量与时间的关系如图。则:
。某体积为2 L的恒容反应器中发生上述反应,Cl2的物质的量与时间的关系如图。则: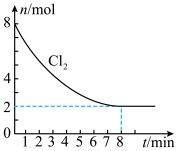
 ;
;②其他条件不变时,往反应器中通入氩气(不参与反应),该反应的反应速率
您最近一年使用:0次
名校
6 . 菱铁矿主要成分是碳酸亚铁( ),以菱铁矿为原料制取铁的一种流程如图:
),以菱铁矿为原料制取铁的一种流程如图:
(1)“氧化”和“沉淀”是将“酸浸”过程中产生的 全部转化为
全部转化为 ,
, 为一种
为一种______ (填“白”或“红褐”)色沉淀。
(2)“分解”过程的产物为水和______ (填“FeO”或“ ”)。
”)。
(3)利用金属活动性的不同,可以采取不同的冶炼方法,上述流程中的“过程Ⅰ”属于______ (填“热还原法”或“热分解法”)。
(4)氨水由氨气溶于水制备,工业合成氨的化学方程式为 。一定条件下,在2L密闭容器中,充入3mol
。一定条件下,在2L密闭容器中,充入3mol  和1mol
和1mol  发生反应,2min时测得生成了0.4mol
发生反应,2min时测得生成了0.4mol  。则:
。则:
①用 表示2min内该反应的速率为
表示2min内该反应的速率为______  。
。
②其他条件不变,将容器的容积压缩为1L,则该反应的速率______ (填“增大”“减小”或“不变”)。
 ),以菱铁矿为原料制取铁的一种流程如图:
),以菱铁矿为原料制取铁的一种流程如图: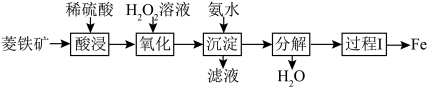
(1)“氧化”和“沉淀”是将“酸浸”过程中产生的
 全部转化为
全部转化为 ,
, 为一种
为一种(2)“分解”过程的产物为水和
 ”)。
”)。(3)利用金属活动性的不同,可以采取不同的冶炼方法,上述流程中的“过程Ⅰ”属于
(4)氨水由氨气溶于水制备,工业合成氨的化学方程式为
 。一定条件下,在2L密闭容器中,充入3mol
。一定条件下,在2L密闭容器中,充入3mol  和1mol
和1mol  发生反应,2min时测得生成了0.4mol
发生反应,2min时测得生成了0.4mol  。则:
。则:①用
 表示2min内该反应的速率为
表示2min内该反应的速率为 。
。②其他条件不变,将容器的容积压缩为1L,则该反应的速率
您最近一年使用:0次
7 . 乙烯( )是重要的有机化合物。请根据下列转化关系,回答下列问题:
)是重要的有机化合物。请根据下列转化关系,回答下列问题:______ 。
(2)A分子的结构简式是______ 。
(3)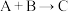 反应的类型属于
反应的类型属于______ 反应(填“取代”或“加成”)。
 )是重要的有机化合物。请根据下列转化关系,回答下列问题:
)是重要的有机化合物。请根据下列转化关系,回答下列问题:
(2)A分子的结构简式是
(3)
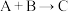 反应的类型属于
反应的类型属于
您最近一年使用:0次
名校
8 . 已知: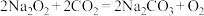 ,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。
,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。
(1)仪器a的名称为______ 。
(2)A为制取 的装置,锥形瓶中盛放石灰石,则a中盛放的药品为
的装置,锥形瓶中盛放石灰石,则a中盛放的药品为______ (填“盐酸”或“硫酸”)。
(3)B中盛放饱和 溶液,其作用为
溶液,其作用为______ 。
(4)D中盛放NaOH溶液,其作用为______ 。
(5)若有7.8g 参加反应,则理论上可收集到气体的体积为
参加反应,则理论上可收集到气体的体积为______ L(标准状况)。
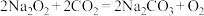 ,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。
,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。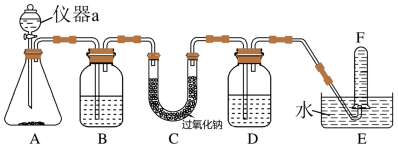
(1)仪器a的名称为
(2)A为制取
 的装置,锥形瓶中盛放石灰石,则a中盛放的药品为
的装置,锥形瓶中盛放石灰石,则a中盛放的药品为(3)B中盛放饱和
 溶液,其作用为
溶液,其作用为(4)D中盛放NaOH溶液,其作用为
(5)若有7.8g
 参加反应,则理论上可收集到气体的体积为
参加反应,则理论上可收集到气体的体积为
您最近一年使用:0次
名校
9 . 化学来源于生活,且应用于生活。请根据题意填空:
(1)钠盐有多种,其中常用作食用碱的是______ (填“ ”或“NaOH”)
”或“NaOH”)
(2)电子工业中用覆铜板制作印刷电路板的原理为 。该反应中
。该反应中 作
作______ (填“氧化剂”或“还原剂”)。
(3)铝制品表面有一层氧化铝( )薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
)薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
______ 。
(1)钠盐有多种,其中常用作食用碱的是
 ”或“NaOH”)
”或“NaOH”)(2)电子工业中用覆铜板制作印刷电路板的原理为
 。该反应中
。该反应中 作
作(3)铝制品表面有一层氧化铝(
 )薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
)薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:
您最近一年使用:0次
名校
10 . 非金属元素在生产生活中扮演着重要角色。请根据题意填空:
(1) 是一种无色有刺激性气味的气体,若任意排放,带来的最主要影响是会形成
是一种无色有刺激性气味的气体,若任意排放,带来的最主要影响是会形成______ (填“温室效应”或“酸雨”)。
(2)将 通入冷的石灰乳
通入冷的石灰乳 中,可制得漂白粉,漂白粉的有效成分为
中,可制得漂白粉,漂白粉的有效成分为______ (填“ ”或“NaClO”)。
”或“NaClO”)。
(3)液氨汽化时吸收大量的热,使周围温度急剧降低,故液氨可作______ (填“制冷剂”或“催化剂”)。
(1)
 是一种无色有刺激性气味的气体,若任意排放,带来的最主要影响是会形成
是一种无色有刺激性气味的气体,若任意排放,带来的最主要影响是会形成(2)将
 通入冷的石灰乳
通入冷的石灰乳 中,可制得漂白粉,漂白粉的有效成分为
中,可制得漂白粉,漂白粉的有效成分为 ”或“NaClO”)。
”或“NaClO”)。(3)液氨汽化时吸收大量的热,使周围温度急剧降低,故液氨可作
您最近一年使用:0次



