1 .  是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
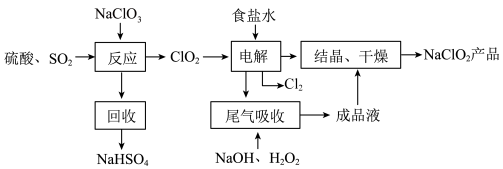
回答下列问题:
(1) 中
中 的化合价为
的化合价为_________ 。
(2)写出“反应”步骤中生成 的化学方程式
的化学方程式___________________________ 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和
和 和
和 ,需要加入的试剂有:①
,需要加入的试剂有:① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液,则加入试剂的先后顺序为
溶液,则加入试剂的先后顺序为_________ ,检验所加入的 溶液已过量的实验方法是
溶液已过量的实验方法是______________________ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_________ ,该反应中氧化产物是_________ 。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_________ 。(计算结果保留两位小数)
 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)
 中
中 的化合价为
的化合价为(2)写出“反应”步骤中生成
 的化学方程式
的化学方程式(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 和
和 和
和 ,需要加入的试剂有:①
,需要加入的试剂有:① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液,则加入试剂的先后顺序为
溶液,则加入试剂的先后顺序为 溶液已过量的实验方法是
溶液已过量的实验方法是(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
解题方法
2 . 海洋是巨大的资源宝库,从海洋中获取部分资源的流程图如下:

回答下列问题:
Ⅰ.海水提溴
溴被称为“海洋元素”,空气吹出法从海水中提取溴单质的流程如下图所示:

(1)过程③中 所起的作用为
所起的作用为___________ (用离子方程式表示)
(2)上图过程①②③④中含Br元素的物质发生的变化依次为___________ ,___________ ,___________ ,___________ 。(选填字母标号并排序,选项可重复使用,也可不选用)
A.被氧化 B.被还原 C.未参与氧化还原反应
(3)步骤①已经获得 ,步骤②③④的目的是
,步骤②③④的目的是___________
Ⅱ.海水提镁
(4)该工业生产过程中,为了使 转化为
转化为 ,应加入的试剂为
,应加入的试剂为___________ (填化学式)。
(5)写出冶炼金属Mg的化学方程式___________ 。
Ⅲ.产品应用
(6)以下属于纯碱在日常生活或工业生产中的用途的有___________(填标号)。

回答下列问题:
Ⅰ.海水提溴
溴被称为“海洋元素”,空气吹出法从海水中提取溴单质的流程如下图所示:

(1)过程③中
 所起的作用为
所起的作用为(2)上图过程①②③④中含Br元素的物质发生的变化依次为
A.被氧化 B.被还原 C.未参与氧化还原反应
(3)步骤①已经获得
 ,步骤②③④的目的是
,步骤②③④的目的是Ⅱ.海水提镁
(4)该工业生产过程中,为了使
 转化为
转化为 ,应加入的试剂为
,应加入的试剂为(5)写出冶炼金属Mg的化学方程式
Ⅲ.产品应用
(6)以下属于纯碱在日常生活或工业生产中的用途的有___________(填标号)。
| A.抗酸药 | B.制玻璃 | C.去油污 | D.抗氧化剂 |
您最近一年使用:0次
解题方法
3 . 海水中含有丰富的自然资源,溶解着大量的 、
、 、
、 、
、 、
、 元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取
元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取 晶体的流程如下:
晶体的流程如下:
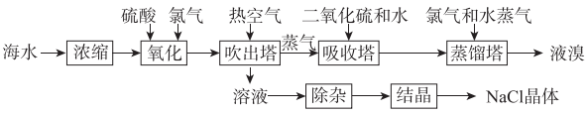
回答下列问题:
(1)“浓缩”的目的是___________ (任答1条即可)。
(2)流程中可用热空气吹出溴的原因为___________ (填选项字母)。
A.溴的氧化性较强 B.溴的熔点较低 C.溴的挥发性较强 D.溴在水中的溶解度较低
(3)上述流程中涉及的氧化还原反应有___________ 个。
(4)“吸收塔”中发生反应的离子方程式为___________ 。
(5)根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期除去的离子。
(6)制取 晶体的“结晶”操作为
晶体的“结晶”操作为___________ 。
 、
、 、
、 、
、 、
、 元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取
元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取 晶体的流程如下:
晶体的流程如下:
回答下列问题:
(1)“浓缩”的目的是
(2)流程中可用热空气吹出溴的原因为
A.溴的氧化性较强 B.溴的熔点较低 C.溴的挥发性较强 D.溴在水中的溶解度较低
(3)上述流程中涉及的氧化还原反应有
(4)“吸收塔”中发生反应的离子方程式为
(5)根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期除去的离子。
| 实验步骤 | 试剂 | 预期除去的离子 |
| 步骤1 |  |  |
| 步骤2 | ① | ② |
| 步骤3 |  | ③ |
| 步骤4 | ④ |  |
(6)制取
 晶体的“结晶”操作为
晶体的“结晶”操作为
您最近一年使用:0次
2021-07-10更新
|
330次组卷
|
3卷引用:湖北省黄冈市2021-2022学年高一下学期期末考试化学试题
湖北省黄冈市2021-2022学年高一下学期期末考试化学试题广东省肇庆市2020-2021学年高一下学期期末教学质量检测化学试题(已下线)【期末复习】必刷题(4)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
解题方法
4 . 海水的综合利用是一个重要的研究课题。实验室模拟从海水晒盐后的母液中提取镁的工艺流程如下,回答下列问题。

(1)上述工艺流程中包含_______ 次过滤操作。
(2)用化学沉淀法去除粗盐中的 、
、 和
和 ,以下所加试剂及顺序均可行的是
,以下所加试剂及顺序均可行的是_______ (填字母)。
A. 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸
B. 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸
C. 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸
D. 溶液、
溶液、 溶液、
溶液、 溶液、稀硫酸
溶液、稀硫酸
(3)实验室高温煅烧贝壳使用的主要仪器有酒精喷灯、三脚架、_______ 。
(4)写出步骤③发生反应的主要离子方程式_______ 。
(5)步骤④中向 加入盐酸后的操作为
加入盐酸后的操作为_______ 。
(6)在步骤⑥的电解中,发生氧化反应的电极方程式为_______ 。
(7)上述步骤①~⑥中,没有涉及到的基本反应类型是_______ 。

(1)上述工艺流程中包含
(2)用化学沉淀法去除粗盐中的
 、
、 和
和 ,以下所加试剂及顺序均可行的是
,以下所加试剂及顺序均可行的是A.
 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸B.
 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸C.
 溶液、
溶液、 溶液、
溶液、 溶液、稀盐酸
溶液、稀盐酸D.
 溶液、
溶液、 溶液、
溶液、 溶液、稀硫酸
溶液、稀硫酸(3)实验室高温煅烧贝壳使用的主要仪器有酒精喷灯、三脚架、
(4)写出步骤③发生反应的主要离子方程式
(5)步骤④中向
 加入盐酸后的操作为
加入盐酸后的操作为(6)在步骤⑥的电解中,发生氧化反应的电极方程式为
(7)上述步骤①~⑥中,没有涉及到的基本反应类型是
您最近一年使用:0次
名校
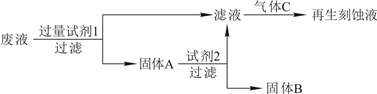
5 . Ⅰ.在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(含有Fe2+、Fe3+、Cu2+)处理和资源回收很有意义。分析下面处理方案,回答下列问题:
(1)试剂2是_______ ,固体B是_______ ,通往的气体C是______ 。(填化学式)。
(2)写出加入试剂1发生反应的离子方程式:________ 、_________ 。
Ⅱ.综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:
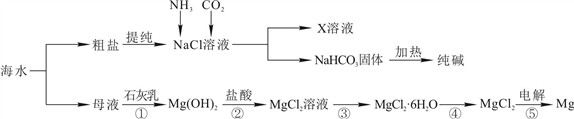
(1)反应①-⑤中,属于氧化还原反应的是_________ (填符号)。
(2)写出反应②的离子方程式____________ 。
(3)X溶液中的主要阳离子是Na+和__________ 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③________ ;④加适量盐酸;⑤_________ (请补全缺少的实验步骤)。
(5)检验纯碱样品中是否含NaCl应选用的试剂是________ 。
(1)试剂2是
(2)写出加入试剂1发生反应的离子方程式:
Ⅱ.综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:

(1)反应①-⑤中,属于氧化还原反应的是
(2)写出反应②的离子方程式
(3)X溶液中的主要阳离子是Na+和
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③
(5)检验纯碱样品中是否含NaCl应选用的试剂是
您最近一年使用:0次
6 . 21世纪是海洋世纪,海洋经济专属区的开发受到广泛重视,下列有关说法正确的是
| A.海水含镁,将金属钠放入海水中可以制取金属镁 |
| B.从海水中提取溴的过程涉及氧化还原反应 |
| C.利用海水制取精盐不涉及化学反应 |
| D.海底多金属结核矿含有Fe、Mn、Co、B等金属 |
您最近一年使用:0次
7 . 从海水中提取金属镁的生产步骤有:①浓缩结晶脱水 ②加熟石灰 ③加盐酸 ④过滤 ⑤熔融电解,正确的生产顺序是
| A.①②③④⑤ | B.⑤④③①② | C.②④③①⑤ | D.③④②①⑤ |
您最近一年使用:0次



