上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
上海
高三
一模
2024-03-18
230次
整体难度:
适中
考查范围:
有机化学基础、物质结构与性质、常见无机物及其应用、化学反应原理、化学实验基础
上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
上海
高三
一模
2024-03-18
230次
整体难度:
适中
考查范围:
有机化学基础、物质结构与性质、常见无机物及其应用、化学反应原理、化学实验基础
一、填空题 添加题型下试题
填空题
|
适中(0.65)
1. 工业排放的某些烟气中含有二氧化硫等大气污染物,对其进行脱硫治理不仅可以防止有害物质排放,还可以生产其他有用的产品。
(1) 分子的空间结构和分子的极性分别为___________。
分子的空间结构和分子的极性分别为___________。
(2)第一电离能: ,结合核外电子排布相关知识,说明其原因
,结合核外电子排布相关知识,说明其原因___________ 。
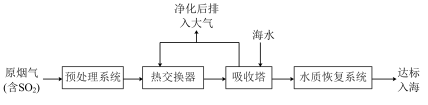
沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示:
25℃时 ,
, 的电离常数如下表所示:
的电离常数如下表所示:
(3)在吸收塔内,烟气应从吸收塔的___________ 通入,与塔顶喷淋的海水充分接触。
A.上部 B.中部 C.下部
(4)吸收塔内温度不宜过高,原因可能是___________ 。(列举1条)吸收塔内 和海水中
和海水中 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(5)若煤电厂排放烟气量为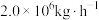 ,其中含
,其中含 为0.15%,该烟气经海水脱硫处理后
为0.15%,该烟气经海水脱硫处理后 为
为 ,则脱硫率
,则脱硫率
___________ 。( )
)
(6)离子液体(ILs)也可以用来处理工业烟气。ILs的负离子吸收 后生成
后生成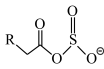 。欲确定
。欲确定 中虚线框内基团的结构,可采用的分析方法有___________。
中虚线框内基团的结构,可采用的分析方法有___________。
工业上还可用 溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
(7)为使 再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
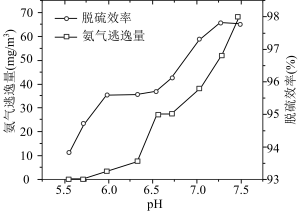
(8)使用 溶液脱硫时,溶液的pH通常需控制在
溶液脱硫时,溶液的pH通常需控制在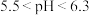 。结合
。结合 的性质和下图,分析pH不宜过小和过大的原因
的性质和下图,分析pH不宜过小和过大的原因___________ 。
(1)
 分子的空间结构和分子的极性分别为___________。
分子的空间结构和分子的极性分别为___________。| A.直线形,非极性 | B.直线形,极性 | C.角形,非极性 | D.角形,极性 |
(2)第一电离能:
 ,结合核外电子排布相关知识,说明其原因
,结合核外电子排布相关知识,说明其原因沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示:

25℃时
 ,
, 的电离常数如下表所示:
的电离常数如下表所示:| 弱酸 |  |  |
 | 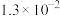 | 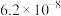 |
 | 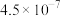 | 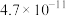 |
(3)在吸收塔内,烟气应从吸收塔的
A.上部 B.中部 C.下部
(4)吸收塔内温度不宜过高,原因可能是
 和海水中
和海水中 发生反应的离子方程式为
发生反应的离子方程式为(5)若煤电厂排放烟气量为
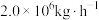 ,其中含
,其中含 为0.15%,该烟气经海水脱硫处理后
为0.15%,该烟气经海水脱硫处理后 为
为 ,则脱硫率
,则脱硫率
 )
)(6)离子液体(ILs)也可以用来处理工业烟气。ILs的负离子吸收
 后生成
后生成 。欲确定
。欲确定 中虚线框内基团的结构,可采用的分析方法有___________。
中虚线框内基团的结构,可采用的分析方法有___________。| A.原子发射光谱 | B.红外光谱 | C.核磁共振氢谱 | D.晶体X射线衍射 |
工业上还可用
 溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。(7)为使
 再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。A. | B.CaO | C. | D.NaOH |
(8)使用
 溶液脱硫时,溶液的pH通常需控制在
溶液脱硫时,溶液的pH通常需控制在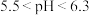 。结合
。结合 的性质和下图,分析pH不宜过小和过大的原因
的性质和下图,分析pH不宜过小和过大的原因
您最近一年使用:0次
2024-01-13更新
|
224次组卷
|
2卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
2. 盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
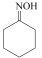 (环己酮肟)
(环己酮肟)
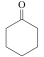 (环己酮)
(环己酮)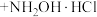
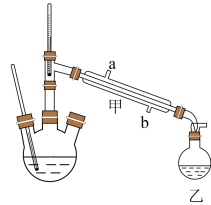
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵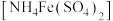 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①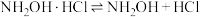
②
③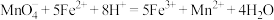
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)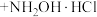
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(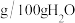 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
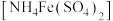 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
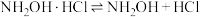
②

③
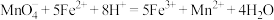
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 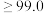 |  |  |

您最近一年使用:0次
2024-01-13更新
|
359次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
解答题-有机推断题
|
适中(0.65)
3. 肾上腺素是一种脂溶性激素,常用于临床抢救。肾上腺素注射液说明书的部分内容如下:
(1)对肾上腺素分子结构分析正确的是___________。
(2)肾上腺素注射液中盐酸的作用是___________ ;肾上腺素注射液接触空气变色的原因是___________ 。
人工合成肾上腺素(D)的某种路线如下所示:
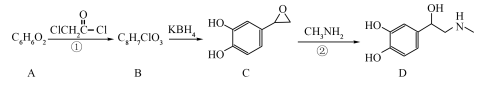
(3)A中含有的官能团为___________。
(4)步骤①的反应类型为___________。
(5)步骤②会产生一种副产物。在质谱图中,该副产物分子离子峰的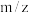 值与肾上腺素的相同,其结构简式为
值与肾上腺素的相同,其结构简式为___________ (不考虑立体异构)。
(6)写出一种符合下列条件的C的同分异构体的结构简式___________ 。
i)能发生银镜反应,也能与 溶液发生显色反应
溶液发生显色反应
ii)核磁共振氢谱图中有4组峰,且峰面积之比为3:2:2:1
(7)上述方法最终得到的D是一对对映体的混合物。
①在下图中用“*”标出D中的不对称碳原子___________ 。

②生产肾上腺素注射液时,须对D的一对对映体进行分离,才能用于生产肾上腺素注射液,原因可能是___________ 。
(8)已知: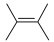
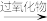
 。结合题示信息,设计以环己烷(
。结合题示信息,设计以环己烷(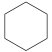 )和
)和 为主要原料合成
为主要原料合成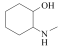 的路线
的路线___________ (无机试剂任选)。
(合成路线可表示为: )
)
| 肾上腺素注射液说明书 【成分】本品为加盐酸的肾上腺素灭菌水溶液。 【性状】本品为几乎无色的澄清液体;与空气接触,会近渐变为淡红色,最后变成棕色。 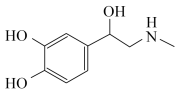 肾上腺素分子的结构 |
(1)对肾上腺素分子结构分析正确的是___________。
A.碳原子采取 、 、 杂化 杂化 | B.所有原子共平面 |
| C.N原子有3对价层电子对 | D.分子中含有肽键 |
(2)肾上腺素注射液中盐酸的作用是
人工合成肾上腺素(D)的某种路线如下所示:

(3)A中含有的官能团为___________。
| A.醛基 | B.醇羟基 | C.酚羟基 | D.羧基 |
(4)步骤①的反应类型为___________。
| A.取代反应 | B.消去反应 | C.氧化反应 | D.还原反应 |
(5)步骤②会产生一种副产物。在质谱图中,该副产物分子离子峰的
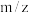 值与肾上腺素的相同,其结构简式为
值与肾上腺素的相同,其结构简式为(6)写出一种符合下列条件的C的同分异构体的结构简式
i)能发生银镜反应,也能与
 溶液发生显色反应
溶液发生显色反应ii)核磁共振氢谱图中有4组峰,且峰面积之比为3:2:2:1
(7)上述方法最终得到的D是一对对映体的混合物。
①在下图中用“*”标出D中的不对称碳原子

②生产肾上腺素注射液时,须对D的一对对映体进行分离,才能用于生产肾上腺素注射液,原因可能是
(8)已知:

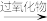
 。结合题示信息,设计以环己烷(
。结合题示信息,设计以环己烷( )和
)和 为主要原料合成
为主要原料合成 的路线
的路线(合成路线可表示为:
 )
)
您最近一年使用:0次
2024-01-13更新
|
321次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷(已下线)专题11 有机推断综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
三、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
4. 含铁化合物在生产、生活中有广泛的应用。下图是一种太阳能电池工作原理的示意图,其中电解质溶液为 和
和 的混合溶液。
的混合溶液。 中,中心离子为
中,中心离子为___________ 。
(2)电池工作时,下列描述正确的是___________。
(3)正极上发生的电极反应为___________ 。
氮化铁晶体可应用于磁记录材料领域,其晶胞结构如下图所示:
(5)该氮化铁晶体的化学式为___________ 。
A.FeN B.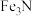 C.
C. D.
D.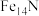
结合图中数据,计算该晶胞的密度
___________  。(设
。(设 为阿伏加德罗常数,用含r和
为阿伏加德罗常数,用含r和 的代数式表示,
的代数式表示, )
)
向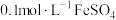 溶液中持续通入
溶液中持续通入 至饱和,有微量黑色的FeS沉淀生成,该溶液中
至饱和,有微量黑色的FeS沉淀生成,该溶液中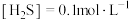 。(忽略
。(忽略 浓度的变化和溶液体积的变化)
浓度的变化和溶液体积的变化)
已知常温下,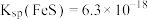 ,
, 的电离常数分别为:
的电离常数分别为: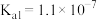 、
、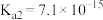 。
。
(6)写出生成黑色沉淀的离子方程式___________ 。溶液中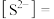
___________  ;溶液中
;溶液中
___________  。
。
 和
和 的混合溶液。
的混合溶液。
 中,中心离子为
中,中心离子为(2)电池工作时,下列描述正确的是___________。
| A.电极a为正极 | B. 向电极a移动 向电极a移动 |
| C.电子由电极a经导线流向电极b | D.电极b上发生氧化反应 |
(3)正极上发生的电极反应为
氮化铁晶体可应用于磁记录材料领域,其晶胞结构如下图所示:

| A.2 | B.4 | C.6 | D.8 |
(5)该氮化铁晶体的化学式为
A.FeN B.
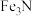 C.
C. D.
D.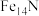
结合图中数据,计算该晶胞的密度

 。(设
。(设 为阿伏加德罗常数,用含r和
为阿伏加德罗常数,用含r和 的代数式表示,
的代数式表示, )
)向
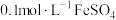 溶液中持续通入
溶液中持续通入 至饱和,有微量黑色的FeS沉淀生成,该溶液中
至饱和,有微量黑色的FeS沉淀生成,该溶液中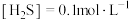 。(忽略
。(忽略 浓度的变化和溶液体积的变化)
浓度的变化和溶液体积的变化)已知常温下,
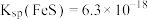 ,
, 的电离常数分别为:
的电离常数分别为: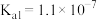 、
、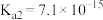 。
。(6)写出生成黑色沉淀的离子方程式
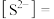
 ;溶液中
;溶液中
 。
。
您最近一年使用:0次
2024-01-13更新
|
256次组卷
|
2卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
四、解答题 添加题型下试题
解答题-原理综合题
|
较难(0.4)
解题方法
5. 杭州亚运会主火炬塔燃料使用的甲醇被誉为绿色燃料。在以往的运动会中,丙烷、煤油也曾作为燃料使用。上述燃料的热值和 排放量如下表所示:
排放量如下表所示:
(1)根据上表数据,计算 的燃烧热为___________
的燃烧热为___________ 。
。
(2)根据上表,从 排放量和燃料储存两个角度分析,选用甲醇作为主火炬塔燃料的可能原因
排放量和燃料储存两个角度分析,选用甲醇作为主火炬塔燃料的可能原因___________ 。
以 和
和 为原料制备甲醇是实现
为原料制备甲醇是实现 资源化利用的方式之一、其反应原理为:
资源化利用的方式之一、其反应原理为:
(3)下图中,曲线___________ 能表示该反应的平衡常数K与温度T的关系。
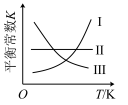
A.I B.II C.III
(4)某温度下,向容积为2.0L的恒容密闭容器中充入 和
和 模拟上述反应。反应达到平衡状态时,测得
模拟上述反应。反应达到平衡状态时,测得 。该温度下,平衡常数
。该温度下,平衡常数 ___________。
___________。
在不同温度下,向等容积的反应器中,分别通入等量、相同比例的 和
和 的混合气体,反应相同时间后,测得甲醇产率与催化剂活性、温度关系如下图所示。除生成甲醇外,还会生成副产物CO:
的混合气体,反应相同时间后,测得甲醇产率与催化剂活性、温度关系如下图所示。除生成甲醇外,还会生成副产物CO: 。
。

(5)图中一定不处于化学平衡状态的点是___________。
(6)已知催化剂对副反应没有影响。图中当温度高于500K,甲醇产率逐渐下降,原因可能有___________ 、___________ 。
光催化可以加快合成甲醇的反应速率,下图是该反应的部分历程,其中吸附在催化剂表面的物质用*表示。

(7)上图虚线框中的基元反应,主要决定总反应速率快慢的是___________。
上海某研究团队研制出了一种具有反应和分离“双功能分子师催化膜”反应器,使用该反应器制甲醇时,能大幅度提高二氧化碳转化率,其原理如下图所示:
CO2+3H2 CH3OH+H2O
CH3OH+H2O
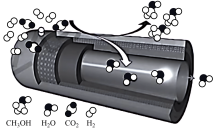
在不同反应器中, 平衡转化率和甲醇选择性
平衡转化率和甲醇选择性 的相关实验数据如下表所示:
的相关实验数据如下表所示:
(8)从绿色化学的角度,分析该双功能分子筛催化膜反应器的优点有:
① 平衡转化率明显升高;
平衡转化率明显升高;
②___________ ;
③___________ 。
 排放量如下表所示:
排放量如下表所示:| 燃料 |  |  | 煤油 |
热值 | 22.7 | 50.4 | 29.0 |
 排放量 排放量 | 16.5 | 16.2 | 22.9 |
(1)根据上表数据,计算
 的燃烧热为___________
的燃烧热为___________ 。
。| A.22.7 | B. | C. | D. |
(2)根据上表,从
 排放量和燃料储存两个角度分析,选用甲醇作为主火炬塔燃料的可能原因
排放量和燃料储存两个角度分析,选用甲醇作为主火炬塔燃料的可能原因以
 和
和 为原料制备甲醇是实现
为原料制备甲醇是实现 资源化利用的方式之一、其反应原理为:
资源化利用的方式之一、其反应原理为:
(3)下图中,曲线

A.I B.II C.III
(4)某温度下,向容积为2.0L的恒容密闭容器中充入
 和
和 模拟上述反应。反应达到平衡状态时,测得
模拟上述反应。反应达到平衡状态时,测得 。该温度下,平衡常数
。该温度下,平衡常数 ___________。
___________。| A.3.00 | B.0.33 | C.0.15 | D.0.59 |
在不同温度下,向等容积的反应器中,分别通入等量、相同比例的
 和
和 的混合气体,反应相同时间后,测得甲醇产率与催化剂活性、温度关系如下图所示。除生成甲醇外,还会生成副产物CO:
的混合气体,反应相同时间后,测得甲醇产率与催化剂活性、温度关系如下图所示。除生成甲醇外,还会生成副产物CO: 。
。
(5)图中一定不处于化学平衡状态的点是___________。
| A.点A | B.点B | C.点C | D.点D |
(6)已知催化剂对副反应没有影响。图中当温度高于500K,甲醇产率逐渐下降,原因可能有
光催化可以加快合成甲醇的反应速率,下图是该反应的部分历程,其中吸附在催化剂表面的物质用*表示。

(7)上图虚线框中的基元反应,主要决定总反应速率快慢的是___________。
A. | B. |
C. | D. |
上海某研究团队研制出了一种具有反应和分离“双功能分子师催化膜”反应器,使用该反应器制甲醇时,能大幅度提高二氧化碳转化率,其原理如下图所示:
CO2+3H2
 CH3OH+H2O
CH3OH+H2O
在不同反应器中,
 平衡转化率和甲醇选择性
平衡转化率和甲醇选择性 的相关实验数据如下表所示:
的相关实验数据如下表所示:| 实验组 | 反应器 | 压强/MPa | 温度/K | 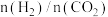 |  平衡转化率/% 平衡转化率/% | 甲醇选择性/% |
| ① | 普通催化反应器 | 3 | 533 | 3 | 21.9 | 67.3 |
| ② | 双功能分子筛催化膜反应器 | 36.1 | 100 |
(8)从绿色化学的角度,分析该双功能分子筛催化膜反应器的优点有:
①
 平衡转化率明显升高;
平衡转化率明显升高;②
③
您最近一年使用:0次
2024-01-13更新
|
361次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷
试卷分析
整体难度:适中
考查范围:有机化学基础、物质结构与性质、常见无机物及其应用、化学反应原理、化学实验基础
试卷题型(共 5题)
题型
数量
填空题
2
解答题
3
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、填空题 | |||
| 1 | 0.65 | 有机物结构式的确定 极性分子和非极性分子 亚硫酸及其盐 弱电解质的电离平衡常数 | |
| 4 | 0.65 | 沉淀的溶解与生成 原电池正负极判断 原电池电极反应式书写 晶胞的有关计算 | |
| 二、解答题 | |||
| 2 | 0.65 | 浓度对化学平衡移动的影响 酸碱中和滴定实验基本操作及步骤 化学键与分子间作用力 氧化还原原理滴定 | 实验探究题 |
| 3 | 0.65 | 有机推断综合考查 | 有机推断题 |
| 5 | 0.4 | 化学平衡的移动及其影响因素 化学平衡图像分析 化学平衡常数的有关计算 | 原理综合题 |



