2016届贵州省黔南州高三上学期期末联考理综化学试卷
贵州
高三
期末
2017-07-27
240次
整体难度:
适中
考查范围:
化学与STSE、有机化学基础、认识化学科学、物质结构与性质、化学实验基础、化学反应原理、常见无机物及其应用
2016届贵州省黔南州高三上学期期末联考理综化学试卷
贵州
高三
期末
2017-07-27
240次
整体难度:
适中
考查范围:
化学与STSE、有机化学基础、认识化学科学、物质结构与性质、化学实验基础、化学反应原理、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
适中(0.64)
1. 化学与环境、材料、信息、能源关系密切,下列说法正确的是
| A.氟利昂(CCl2F2)会破坏大气臭氧层从而导致“温室效应” |
| B.开发高效氢能、太阳能灯新能源汽车,可以减缓城市机动车尾气污染 |
| C.PM2.5是指大气中直径接近2.5×10-6m的颗粒物,它分散在空气中形成胶体 |
| D.海水淡化可以解决淡水危机,向海水中加入明矾可以使海水淡化 |
【知识点】 化学与环境保护
您最近一年使用:0次
单选题
|
适中(0.64)
2. 丙烯酸(CH2=CH-COOH)可发生的化学反应类型有
①加成②氧化③酯化④加聚⑤取代
①加成②氧化③酯化④加聚⑤取代
| A.只有①②③ | B.只有①②③④ | C.只有①③④ | D.全部 |
【知识点】 烃的衍生物
您最近一年使用:0次
2016-12-09更新
|
135次组卷
|
3卷引用:2016届贵州省黔南州高三上学期期末联考理综化学试卷
单选题
|
较难(0.4)
3. 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.2.24LNH3和CH4的混合气体,所含电子总数为2NA |
| B.1mol乙醇(CH3CH2OH)分子中含有共价键总数为8NA |
| C.1mol/LNa2CO3溶液中,含有CO32-离子数为NA |
| D.6.4gCu与足量浓硝酸反应,用排水法收集的气体分子数为0.2NA |
【知识点】 化学计量
您最近一年使用:0次
单选题
|
适中(0.64)
4. X、Y、Z、W、R五种短周期元素,原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其原子的电子层数等于主族序数,W单质是一种常见的半导体材料。下列说法正确的是
| A.R的气态氢化物比W的气态氢化物更稳定 |
| B.Z的氧化物能与盐酸反应,不能与NaOH溶液反应 |
| C.原子半径按X、R、W、Z、Y的顺序依次增大 |
| D.X、Y、Z的最高化合价数值均等于其主族序数 |
【知识点】 元素周期表 元素周期律
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 海洋中有丰富的“食品、矿产、能源、药物和水产资源”等,下列说法正确的是


| A.第①步中除去泥沙及Ca2+、Mg2+等杂质时,不涉及化学变化过程 |
| B.工业上,通过电解“精盐”水溶液可以制取金属钠 |
| C.第②步的反应条件是“在空气中直接加热” |
| D.第③、④、⑤步中均涉及氧化还原反应 |
您最近一年使用:0次
2016-12-09更新
|
441次组卷
|
3卷引用:2016届贵州省黔南州高三上学期期末联考理综化学试卷
单选题
|
容易(0.94)
6. 纳米级Cu2O由于具有优良的催化性能而受到关注。采用离子交换膜控制阳极电解液中OH-的浓度制备纳米级Cu2O的装置如图所示,总反应为2Cu+H2O Cu2O+H2↑。下列说法不正确的是
Cu2O+H2↑。下列说法不正确的是

 Cu2O+H2↑。下列说法不正确的是
Cu2O+H2↑。下列说法不正确的是
| A.钛(Ti)电极表面发生氧化反应 |
| B.阳极附近溶液的pH逐渐减小 |
| C.离子交换膜宜采用阴离子交换膜 |
| D.阳极表面总反应式是:2Cu+2OH--2e-=Cu2O+H2O |
【知识点】 电解池
您最近一年使用:0次
单选题
|
容易(0.94)
7. 现取mg镁铝合金在一定量的稀硝酸中恰好完全溶解(硝酸的还原产物只有NO),向反应后的溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值ng。下列有关该实验的说法中不正确的是
| A.沉淀中OH-的质量为(n-m)g |
B.反应过程中转移电子的物质的量为 mol mol |
C.标准状况下生成NO的体积为 |
D.与合金反应的硝酸的物质的量为 |
【知识点】 化学计量
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
8. 实验室常用的几种气体发生装置如图1所示:
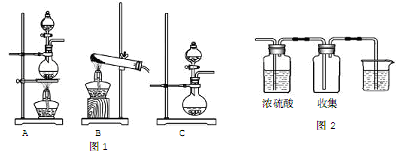
(1)若实验室选用A装置,由乙醇和浓硫酸共热制取乙烯,应该在此装置上作何改进即可完成该实验?__________ 。
(2)实验室可选用B装置,由氯化铵和碱石灰共热制取NH3。若实验室仅有浓氨水与生石灰,可选用__________ 装置来制取氨气,下列叙述与后者制取NH3的原理不相关的是_____________ 。
A.浓氨水易挥发
B.Ca(OH)2随温度上升溶解度降低
C.生石灰与水反应放热
D.气态物质的溶解性随温度的升高而降低
(3)请用两种方法制取氧气,可供选用的药品有:KClO3、H2O2、NaOH、MnO2。若选择B装置,可选用的试剂为______________ ;若选择C装置,可选用的试剂为_____________ 。
(4)若把“图1”中的“A装置”与“图2”相连,可用来制取下列气体中的____________ (填序号)。
①H2②Cl2③CO2④NH3写出实验室制取该气体的化学方程式:___________ ,烧杯中应盛放___________ 溶液,为了获得较纯净的产物,应在A与“图2”间增加____________ 装置。

(1)若实验室选用A装置,由乙醇和浓硫酸共热制取乙烯,应该在此装置上作何改进即可完成该实验?
(2)实验室可选用B装置,由氯化铵和碱石灰共热制取NH3。若实验室仅有浓氨水与生石灰,可选用
A.浓氨水易挥发
B.Ca(OH)2随温度上升溶解度降低
C.生石灰与水反应放热
D.气态物质的溶解性随温度的升高而降低
(3)请用两种方法制取氧气,可供选用的药品有:KClO3、H2O2、NaOH、MnO2。若选择B装置,可选用的试剂为
(4)若把“图1”中的“A装置”与“图2”相连,可用来制取下列气体中的
①H2②Cl2③CO2④NH3写出实验室制取该气体的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
9. 氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为:7.1×10-6,2.98×10-9。HNO2的酸性比HClO_______ (填“强”、“弱”);将0.1mol/L的亚硝酸加水稀释100倍,c(H+)_______ (填“不变”、“增大”或“减小”),Ka值________ (同上)
(2)NaNO2与NaCl都是白色粉末且都有咸味,但NaNO2有毒,具有致癌性。通常它们可以通过加入热的白醋(CH3COOH)鉴别,NaNO2遇到白醋会产生一种红棕色气体和一种无色气体,它们的组成元素相同。该反应的离子方程式为____________ 。
(3)磷及部分重要化合物的相互转化如图甲所示。

①“步骤Ⅰ”为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,焦炭的作用是__________ 。
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,“步骤Ⅱ”涉及的反应中氧化剂是_________ 。
(4)若处理后的废水中c(PO43-)=4×10-7mol/L,则溶液中c(Ca2+)不会超过________ mol/L。(Ksp[Ca2(PO4)3]=2×10-29)
(5)某“液氨—液氧”燃料电池装置示意图如图乙所示,该燃料电池以NaOH为电解质。该电池在工作时,“电极2”为_______ 极(填“正”或“负”);“电极1”表面发生的电极反应式为_________ 。
(1)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为:7.1×10-6,2.98×10-9。HNO2的酸性比HClO
(2)NaNO2与NaCl都是白色粉末且都有咸味,但NaNO2有毒,具有致癌性。通常它们可以通过加入热的白醋(CH3COOH)鉴别,NaNO2遇到白醋会产生一种红棕色气体和一种无色气体,它们的组成元素相同。该反应的离子方程式为
(3)磷及部分重要化合物的相互转化如图甲所示。

①“步骤Ⅰ”为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,焦炭的作用是
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,“步骤Ⅱ”涉及的反应中氧化剂是
(4)若处理后的废水中c(PO43-)=4×10-7mol/L,则溶液中c(Ca2+)不会超过
(5)某“液氨—液氧”燃料电池装置示意图如图乙所示,该燃料电池以NaOH为电解质。该电池在工作时,“电极2”为
您最近一年使用:0次
2016-12-09更新
|
112次组卷
|
2卷引用:2016届贵州省黔南州高三上学期期末联考理综化学试卷
三、填空题 添加题型下试题
填空题
|
困难(0.15)
10. 我国是钢铁大国,高炉炼铁是最为普遍的炼铁方法,下面是炼铁的有关反应。
Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g)∆H=-566kJ/mol
②2Fe(s)+ O2(g)=Fe2O3(g)∆H=-825.5kJ/mol
O2(g)=Fe2O3(g)∆H=-825.5kJ/mol
反应:③Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)∆H=
2Fe(s)+3CO2(g)∆H=___________ kJ/mol
Ⅱ.反应:④ Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) 
 Fe(s)+CO2(g);1000℃时,在一个容积为10L的恒容密闭容器中,加入Fe(s)、Fe2O3(s)、CO(g)、CO2(g)各10mol,反应经过10min后达到平衡。(已知:在1000℃,反应④的平衡常数等于4.0)。
Fe(s)+CO2(g);1000℃时,在一个容积为10L的恒容密闭容器中,加入Fe(s)、Fe2O3(s)、CO(g)、CO2(g)各10mol,反应经过10min后达到平衡。(已知:在1000℃,反应④的平衡常数等于4.0)。
(1)反应④的平衡常数表达式是___________ ,平衡时CO的转化率=___________ %。
(2)欲提高平衡时CO的转化率,可采取的措施是___________ 。
A.适当降低反应温度 B.增大反应体系的压强
C.选取合适的催化剂 D.及时吸收或移出部分CO2
Ⅲ.对高炉炼铁废气中的CO进行回收,使其在一定条件下和H2反应合成甲醇:CO(g)+2H2(g) CH3OH(g)∆H=-391kJ/mol。有关物质的浓度和反应过程中的能量变化如图一、图二所示。
CH3OH(g)∆H=-391kJ/mol。有关物质的浓度和反应过程中的能量变化如图一、图二所示。

(1)“图一”中:A线表示___________ 的浓度变化,0-10分钟,用H2浓度变化表示的平均反应速率v(H2)=___________ 。
(2)“图二”中:a=___________ kJ/mol。
(3)向恒温、恒压的密闭容器中充入1molCO(g)、2molH2(g)和1molCH3OH(g)开始反应,达到平衡时,测得混合气体的密度是起始时的1.6倍。起始时该反应的速率v(正)___________ v(逆)(填“>”、“<”或“=”)。
Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g)∆H=-566kJ/mol
②2Fe(s)+
 O2(g)=Fe2O3(g)∆H=-825.5kJ/mol
O2(g)=Fe2O3(g)∆H=-825.5kJ/mol反应:③Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)∆H=
2Fe(s)+3CO2(g)∆H=Ⅱ.反应:④
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) 
 Fe(s)+CO2(g);1000℃时,在一个容积为10L的恒容密闭容器中,加入Fe(s)、Fe2O3(s)、CO(g)、CO2(g)各10mol,反应经过10min后达到平衡。(已知:在1000℃,反应④的平衡常数等于4.0)。
Fe(s)+CO2(g);1000℃时,在一个容积为10L的恒容密闭容器中,加入Fe(s)、Fe2O3(s)、CO(g)、CO2(g)各10mol,反应经过10min后达到平衡。(已知:在1000℃,反应④的平衡常数等于4.0)。(1)反应④的平衡常数表达式是
(2)欲提高平衡时CO的转化率,可采取的措施是
A.适当降低反应温度 B.增大反应体系的压强
C.选取合适的催化剂 D.及时吸收或移出部分CO2
Ⅲ.对高炉炼铁废气中的CO进行回收,使其在一定条件下和H2反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)∆H=-391kJ/mol。有关物质的浓度和反应过程中的能量变化如图一、图二所示。
CH3OH(g)∆H=-391kJ/mol。有关物质的浓度和反应过程中的能量变化如图一、图二所示。
(1)“图一”中:A线表示
(2)“图二”中:a=
(3)向恒温、恒压的密闭容器中充入1molCO(g)、2molH2(g)和1molCH3OH(g)开始反应,达到平衡时,测得混合气体的密度是起始时的1.6倍。起始时该反应的速率v(正)
【知识点】 化学平衡
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
11. 下面是自来水生产的流程示意图:

(1)混凝剂除去杂质的过程__________ (填写序号)。
①只有物理变化②只有化学变化③既有物理变化也有化学变化FeSO4·7H2O是常用的混凝剂,在水体中最终生成_____________ (填“Fe(OH)2”或“Fe(OH)3”),请用离子方程式表示这一过程__________ 。
(2)要除去水体中含有的Ca2+、Mg2+。可选择生石灰和纯碱作沉淀剂,应向水体中先投放__________ ,后投放____________ ,理由是______________ 。
(3)次氯酸的强氧化性能杀死水体中的病菌,但不能直接用次氯酸为自来水消毒,这时因为次氯酸易分解,且毒性较大。已知:Cl2+H2O HCl+HClO K=4.5×10-6,使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合信息解释:使用Cl2为自来水消毒的理由:
HCl+HClO K=4.5×10-6,使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合信息解释:使用Cl2为自来水消毒的理由:____________ 。下列物质中,可以代替氯气用作自来水消毒剂的是_________ (填写序号)。①臭氧 ②酒精 ③K2FeO4④SO2

(1)混凝剂除去杂质的过程
①只有物理变化②只有化学变化③既有物理变化也有化学变化FeSO4·7H2O是常用的混凝剂,在水体中最终生成
(2)要除去水体中含有的Ca2+、Mg2+。可选择生石灰和纯碱作沉淀剂,应向水体中先投放
(3)次氯酸的强氧化性能杀死水体中的病菌,但不能直接用次氯酸为自来水消毒,这时因为次氯酸易分解,且毒性较大。已知:Cl2+H2O
 HCl+HClO K=4.5×10-6,使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合信息解释:使用Cl2为自来水消毒的理由:
HCl+HClO K=4.5×10-6,使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合信息解释:使用Cl2为自来水消毒的理由:
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
较易(0.85)
12. “可燃冰”是蕴藏于海底的一种潜在能源。它由盛有“甲烷、氦气、氧气、硫化氢”等分子的“水分子笼”构成。
(1)水分子间通过_________ 作用相互结合构成水分子笼。N、O、S元素第一电离能由大到小的顺序为________ (填元素符号)。
(2)从海底取得的“多金属结核”样本中含“铁、锰、铬”等多种金属。
①基态个原子(Cr)的电子排布式为__________ 。
②金属铁的晶体在不同温度下由两种堆积方式,晶胞分别如图1所示。在面心立方晶胞和体心立方晶胞中试剂含有的Fe原子个数之比为____________ ;已知,铁原子的半径为1.27×10-8cm,请计算金属铁的面心立方晶胞的晶体密度为__________ g/cm3(结果保留一位小数)。

(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,图2是[Cu(H2O)4]SO4·H2O的结构示意图。

①写出基态Cu2+的核外电子排布式______________ 。
②胆矾晶体中不存在的作用力类型有__________ (填序号)。
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
(1)水分子间通过
(2)从海底取得的“多金属结核”样本中含“铁、锰、铬”等多种金属。
①基态个原子(Cr)的电子排布式为
②金属铁的晶体在不同温度下由两种堆积方式,晶胞分别如图1所示。在面心立方晶胞和体心立方晶胞中试剂含有的Fe原子个数之比为

(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,图2是[Cu(H2O)4]SO4·H2O的结构示意图。

①写出基态Cu2+的核外电子排布式
②胆矾晶体中不存在的作用力类型有
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
【知识点】 元素周期表 元素周期律
您最近一年使用:0次
六、解答题 添加题型下试题
解答题-有机推断题
|
困难(0.15)
解题方法
13. 香豆素是一种天然香料,常存在于黑香豆、兰花等植物中。

(1)以上是两种常见香豆素,关于香豆素和双香豆素,下列说法正确的是________(填序号)。
(2)写出香豆素与足量NaOH溶液反应的化学方程式____________。
(3)以甲苯为原料生产香豆素流程如下:

已知:
(i) B与FeCl3溶液发生显色反应;
(ii)同一个碳原子上连两个羟基通常不稳定,易脱水形成羰基。
①A的名称是________,C的结构简式是___________,A→B的反应类型是___________。
②D中含有的官能团名称是____________,D与乙酸酐(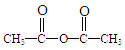 )反应,除生成
)反应,除生成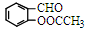 外,同时生成的另一种产物的结构简式是________________。
外,同时生成的另一种产物的结构简式是________________。
③与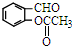 互为同分异构体,且具有以下特点:
互为同分异构体,且具有以下特点:
(a)含有苯环(b)能发生银镜反应(c)与NaHCO3溶液反应可放出气体
符合上述条件的同分异构体共有____________种。

(1)以上是两种常见香豆素,关于香豆素和双香豆素,下列说法正确的是________(填序号)。
| A.双香豆素能与FeCl3溶液发生显色反应 |
| B.都属于芳香烃 |
| C.分子中均含有酯基 |
| D.1mol香豆素含碳碳双键数为4NA |
(3)以甲苯为原料生产香豆素流程如下:

已知:
(i) B与FeCl3溶液发生显色反应;
(ii)同一个碳原子上连两个羟基通常不稳定,易脱水形成羰基。
①A的名称是________,C的结构简式是___________,A→B的反应类型是___________。
②D中含有的官能团名称是____________,D与乙酸酐(
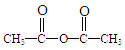 )反应,除生成
)反应,除生成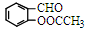 外,同时生成的另一种产物的结构简式是________________。
外,同时生成的另一种产物的结构简式是________________。③与
 互为同分异构体,且具有以下特点:
互为同分异构体,且具有以下特点:(a)含有苯环(b)能发生银镜反应(c)与NaHCO3溶液反应可放出气体
符合上述条件的同分异构体共有____________种。
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、有机化学基础、认识化学科学、物质结构与性质、化学实验基础、化学反应原理、常见无机物及其应用
试卷题型(共 13题)
题型
数量
单选题
7
解答题
4
填空题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.64 | 化学与环境保护 | |
| 2 | 0.64 | 烃的衍生物 | |
| 3 | 0.4 | 化学计量 | |
| 4 | 0.64 | 元素周期表 元素周期律 | |
| 5 | 0.65 | 物质分离、提纯综合应用 海水资源综合利用 海水提取溴 海水提取镁 | |
| 6 | 0.94 | 电解池 | |
| 7 | 0.94 | 化学计量 | |
| 二、解答题 | |||
| 8 | 0.65 | 氯气的实验室制法 氨气的制备 乙醇的消去反应 常见气体的制备与收集 | 实验探究题 |
| 9 | 0.65 | 氧化还原反应的规律 弱电解质的电离平衡 溶度积常数相关计算 原电池电极反应式书写 | 原理综合题 |
| 11 | 0.4 | 离子反应在混合物分离、除杂中的应用 Fe2+的还原性 化学平衡常数的影响因素及应用 | 工业流程题 |
| 13 | 0.15 | 有机合成综合考查 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 10 | 0.15 | 化学平衡 | |
| 12 | 0.85 | 元素周期表 元素周期律 | |



