31. 焦亚硫酸钠(Na
2S
2O
5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:

实验一焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na
2S
2O
5。装置II中有Na
2S
2O
5晶体析出,发生的反应为:
Na
2SO
3+SO
2=Na
2S
2O
5(1)装置I中产生气体的化学方程式为
_______。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是
__________。
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为
__。(填序号)。
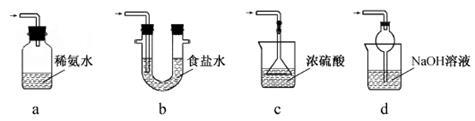
实验二焦亚硫酸钠的性质
Na
2S
2O
5溶于水即生成NaHSO
3。
(4)检验Na
2S
2O
5晶体在空气中已被氧化的实验方案是
___________。
实验三葡萄酒中抗氧化剂残留量的测定
(5)葡萄酒常用Na
2S
2O
5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO
2计算)的方案如下:

(已知:馏分中的二氧化硫在滴入碘水时发生的反应为
SO
2+I
2+2H
2O=H
2SO
4+2HI)在测定时消耗了0.01mol·L
-1的I
2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO
2计算)为
__g·L
-1。在上述实验过程中,若有部分HI被空气氧化,则测得结果
_____(填“偏高”“偏低”或“不变”)。