专题2 本专题达标检测-高中化学苏教2019版必修第一册
全国
高一
课后作业
2021-02-14
215次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用
专题2 本专题达标检测-高中化学苏教2019版必修第一册
全国
高一
课后作业
2021-02-14
215次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
解题方法
1. 用 固体配制
固体配制 溶液。下列图示的实验操作中,不需要进行的操作是
溶液。下列图示的实验操作中,不需要进行的操作是
 固体配制
固体配制 溶液。下列图示的实验操作中,不需要进行的操作是
溶液。下列图示的实验操作中,不需要进行的操作是| A | B | C | D |
 |  |  |  |
| 溶解 | 蒸发 | 转移 | 定容 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-26更新
|
1240次组卷
|
15卷引用:河北省唐山市第十一中学2019-2020学年高二上学期期中考试化学(文)试题1
河北省唐山市第十一中学2019-2020学年高二上学期期中考试化学(文)试题1江苏省淮安市高中教学协作体2019-2020学年高一上学期期中考试化学试题江苏省南京市2019—2020学年高一上学期期末统测化学试题人教版(2019)高一必修第一册 模块综合测评-A卷甘肃省武威八中2020-2021学年高一上学期10月月考化学试题江苏省镇江市吕叔湘中学2019-2020学年高二下学期期中考试(再选班)化学试题福建省三明市三地三校2020-2021学年高一上学期期中联考化学试题安徽省蚌埠市第二中学2020-2021学年高一上学期期中考试化学(文科)试题黑龙江省哈尔滨市呼兰区第一中学校等三校2020-2021学年高一上学期期末联考化学试题江苏省淮安市涟水县第一中学2020-2021学年高一上学期第二次阶段检测化学试题江苏省无锡市普通高中2020-2021学年高一上学期期终教学质量抽测化学试题专题2 本专题达标检测-高中化学苏教2019版必修第一册江苏省马坝高级中学2021-2022学年高二上学期期中考试化学(必修)试题天津市河东区普通高中2020届高三学业水平合格性模拟考试化学试题黑龙江省齐齐哈尔市龙沙区2022-2023学年高一上学期12月期末考试化学试题
单选题
|
较易(0.85)
解题方法
2. 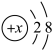 表示某微粒的结构示意图,下列说法不正确的是( )
表示某微粒的结构示意图,下列说法不正确的是( )
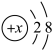 表示某微粒的结构示意图,下列说法不正确的是( )
表示某微粒的结构示意图,下列说法不正确的是( )| A.表示的原子只能为Ne |
| B.表示的金属阳离子有3种 |
| C.表示的微粒对应的元素一定为非金属元素 |
| D.表示的微粒有2个电子层 |
您最近一年使用:0次
2020-04-30更新
|
138次组卷
|
3卷引用:辽宁省朝阳市喀左县蒙古族第四高级中学2019-2020学年高一下学期线上考试化学试题
辽宁省朝阳市喀左县蒙古族第四高级中学2019-2020学年高一下学期线上考试化学试题专题2 本专题达标检测-高中化学苏教2019版必修第一册(已下线)专题04 物质结构 元素周期律-2023年高考化学一轮复习小题多维练(全国通用)
单选题
|
较易(0.85)
解题方法
3. 下列分离四氯化碳与水最合适的装置是( )
A. | B. | C. | D. |
您最近一年使用:0次
2019-11-27更新
|
88次组卷
|
2卷引用:江苏省淮安市高中教学协作体2019-2020学年高一上学期期中考试化学试题
单选题
|
适中(0.65)
名校
4. 下列实验操作或结论正确的是
| A.配制溶液的操作中,转移溶液后,玻璃棒、烧杯未洗涤会使得所配熔液浓度偏高 |
| B.洗涤沉淀的操作是将沉淀置于过滤器中,边用玻璃棒搅拌边加蒸馏水冲洗 |
| C.制备Fe (OH)3胶体时,将饱和FeCl3溶液滴入沸水中,边加热边搅拌,直到得到红褐色溶液 |
| D.实验室配制950 mL 0.2 mol/L 的CuSO4溶液时,需称取胆矾质量为50.0 g |
您最近一年使用:0次
2018-01-16更新
|
157次组卷
|
2卷引用:山东省济南市历城第二中学2017-2018学年高一上学期第三次调研化学试题
单选题
|
较易(0.85)
名校
5. 下列实验中,所选装置不合理的是


| A.粗盐提纯,选①和② |
| B.用CCl4提取碘水中的碘,选③ |
| C.用NaOH溶液吸收少量CO2,选⑤ |
| D.分离Na2CO3溶液和油,选④ |
【知识点】 物质的分离、提纯 物质分离、提纯的常见物理方法
您最近一年使用:0次
2019-10-20更新
|
334次组卷
|
12卷引用:2017届四川省双流中学高三12月月考化学卷
2017届四川省双流中学高三12月月考化学卷江西省南昌市八一中学、洪都中学、麻丘高中等六校2017-2018学年高一10月联考化学试题福建省南安市侨光中学2019-2020学年高一上学期第一次月考化学试题2020届高三化学二轮冲刺新题专练——其他气体除杂分离方式福建省莆田第一中学2019-2020学年高一上学期期中考试化学试题河北省保定市高碑店市高碑店一中2019-2020学年高一上学期第二次月考化学试题专题2 本专题达标检测-高中化学苏教2019版必修第一册福建省泉州市培元中学2020-2021学年高一上学期期中考试化学试题江苏省宿迁市沭阳县2021-2022学年高一上学期期中调研测试化学试题福建省莆田第一中学2021-2022学年高一上学期期末考试化学试题福建省晋江市第一中学2021-2022学年高一上学期期中考试化学试题福建省福州第二中学2023-2024学年高一上学期期中考试化学试题
单选题
|
容易(0.94)
6. 从100 mL0.5 mol·L-1NaOH 溶液中取出1mL,并加水稀释到50mL,关于稀释后的溶液下列叙述正确的是
| A.含NaOH的质量为2 g | B.含NaOH的物质的量为0.005 mol |
| C.浓度为 0.01 mol • L-1 | D.浓度为 0.5 mol • L-1 |
您最近一年使用:0次
2019-12-02更新
|
371次组卷
|
7卷引用:河南省开封市优质高中2019-2020学年高一上学期9月月考化学试题
河南省开封市优质高中2019-2020学年高一上学期9月月考化学试题专题2 本专题达标检测-高中化学苏教2019版必修第一册(已下线)2.3.3 物质的量浓度-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)必考点10 以物质的量为中心的化学计算-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)黑龙江省饶河县高级中学2021-2022学年高一上学期第二次月考化学试题青海省西宁市大通回族土族自治县2022-2023学年高一上学期期末考试化学试题新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高一上学期第二次月考化学试题
单选题
|
适中(0.65)
名校
7. 下列说法正确的是
| A.CH4的摩尔质量为16 g |
| B.在常温常压下等质量的O2和SO2气体的体积比为2:1 |
| C.在标准状况下1 mol CCl4和1 molH2的体积都约为22.4 L |
| D.将40 g NaOH溶于1 L水所得溶液的物质的量浓度为1 mol/L |
您最近一年使用:0次
2019-11-28更新
|
103次组卷
|
2卷引用:四川省威远中学2019-2020学年高一上学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
8. 下列有关实验操作的叙述正确的是
| A.用量筒量取5.00mL1.00mol/盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100mol/L盐酸 |
| B.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| C.用铂丝做焰色反应实验,每次做完后都要用硫酸洗涤 |
| D.过滤操作中,为了加快过滤速度可用玻璃棒在漏斗中轻轻搅拌 |
【知识点】 焰色试验解读 一定物质的量浓度的溶液的配制 化学实验基础操作解读
您最近一年使用:0次
2019-11-25更新
|
165次组卷
|
2卷引用:江苏省常州高级中学2018-2019学年高一上学期期中考试化学试题
单选题
|
容易(0.94)
9. 要配制1 mol·L-1的NaOH溶液100 mL,下面操作正确的是( )
| A.称取4gNaOH固体,放入烧杯里,用量筒量取100mL蒸馏水倒入烧杯中,搅拌充分溶解 |
| B.称取4gNaOH固体,放入100 mL量筒中,加水,充分溶解并稀释至100mL |
| C.称取4gNaOH固体,放入100mL容量瓶中,加蒸馏水溶解,再加水至刻度线,盖好瓶塞,反复摇匀 |
| D.称取4gNaOH固体,放入烧杯里,加适量水溶解,将溶液转移到容量瓶中,洗涤烧杯和玻璃棒,把洗液一并转移到容量瓶中,再加水将溶液体积调至100mL |
【知识点】 配制一定物质的量浓度的溶液的步骤、操作解读
您最近一年使用:0次
2019-11-25更新
|
84次组卷
|
2卷引用:陕西省西安电子科技大学附属中学2019-2020学年高一上学期第一次月考化学试题
单选题
|
适中(0.65)
10. 某盐酸试剂瓶上的标签如图所示。下列有关说法正确的是(设 NA为阿伏加德罗常数的值)


| A.该浓度的盐酸可用广口瓶盛装 |
| B.该盐酸的物质的量浓度为1.19 g/mL |
| C.用该盐酸配制250 mL 2.0 mol/L的稀盐酸时需选用100 mL的量筒 |
| D.该盐酸中所含 Cl-的数目为 5.95NA |
您最近一年使用:0次
二、多选题 添加题型下试题
多选题
|
适中(0.65)
11. 下列基本实验操作中,不合理 的是
| A.配制一定物质的量浓度的溶液,向容量瓶中加水至距离刻度线1~2 cm 时,改用胶头滴管定容 |
| B.除去 KNO3中少量的 NaCl 可用结晶法 |
| C.用洁净的铂丝蘸取待测液,置于酒精灯火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色,该溶液中一定含有钾离子,不含有钠离子 |
| D.用蒸发的方法使 NaCl 从溶液中析出时,应边加热边搅拌直至溶液蒸干 |
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
较易(0.85)
12. 某校化学兴趣小组在实验中发现一瓶溶液,标签上标有 “CaCl2 0.1 mol·L-1”的字样,下面是该小组成员对溶液的叙述,正确的是( )
| A.配制1 L该溶液,可将0.1 mol CaCl2溶于1 L水中 |
| B.Ca2+和Cl-的物质的量浓度都是0.1 mol·L-1 |
| C.从试剂瓶中取该溶液的一半,则所取溶液的物质的量浓度为0.05 mol·L-1 |
| D.将该瓶溶液稀释一倍,则所得溶液的c(Ca2+)为 0.05 mol·L-1 |
您最近一年使用:0次
2019-11-27更新
|
89次组卷
|
2卷引用:黑龙江省绥化市青冈县第一中学2019-2020学年高一上学期期中考试(B班)化学试题
四、多选题 添加题型下试题
多选题
|
较易(0.85)
13. 下列关于物质的量浓度表述正确的是
A.0.3 mol/L的 Na2SO4溶液中含有Na+和  的总物质的量为 0.9mol 的总物质的量为 0.9mol |
| B.当22.4L氨气完全溶于水制得1L氨水时,其物质的量浓度是1mol/L |
C.在K2SO4和 NaCl的中性混合溶液中,如果 Na+和 的物质的量相等,则 K+的浓度必定大于Cl-的浓度 的物质的量相等,则 K+的浓度必定大于Cl-的浓度 |
| D.10 ℃时,100 mL0.35 mol/L的KCl饱和溶液蒸发掉5g水,冷却到10℃时,其体积小于100 mL,溶液中溶质的物质的量浓度仍为 0.35 mol/L |
您最近一年使用:0次
五、单选题 添加题型下试题
单选题
|
较难(0.4)
名校
14. 在T ℃时将a g NH3完全溶于水得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中正确的是
A.溶质的质量分数为w =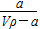 ×100% ×100% |
| B.溶质的物质的量浓度c=a/17V mol·L-1 |
| C.溶液中c(OH-)=1000b/V mol·L-1 |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数小于0.5w |
【知识点】 物质的量浓度的计算
您最近一年使用:0次
2017-12-02更新
|
163次组卷
|
2卷引用:黑龙江省齐齐哈尔市实验中学2017-2018学年高一上学期期中考试化学试题
单选题
|
较易(0.85)
名校
解题方法
15. 下列溶液中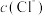 和
和 与
与
 的
的 溶液中
溶液中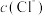 和
和 分别相等的是
分别相等的是
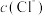 和
和 与
与
 的
的 溶液中
溶液中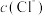 和
和 分别相等的是
分别相等的是A.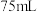  的 的 溶液 溶液 | B.  的 的 溶液 溶液 |
C.  的 的 溶液 溶液 | D.  的 的 溶液 溶液 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
您最近一年使用:0次
2020-09-04更新
|
336次组卷
|
7卷引用:人教版(2019)高一必修第一册第二章 海水中的重要元素 第三节 物质的量 课时3 物质的量浓度
六、填空题 添加题型下试题
填空题
|
较易(0.85)
16. 选择下列实验方法分离物质,将分离方法的字母代号填在横线上。
A.萃取、分液 B.分液C.蒸馏 D.过滤 E.蒸发
(1)分离水和乙酸乙酯(二者不互溶)的混合物,可采用_______ 的方法。
(2)提取碘水中的碘,可采用_______ 的方法。
(3)除去食盐溶液中的水,可采用_______ 的方法。
(4)淡化海水,可采用_______ 的方法。
(5)丙酮是一种常用的有机溶剂,可与水以任意比互溶,密度小于水,沸点约为55℃,分离水和丙酮的混合物时可采用_______ 的方法。
A.萃取、分液 B.分液C.蒸馏 D.过滤 E.蒸发
(1)分离水和乙酸乙酯(二者不互溶)的混合物,可采用
(2)提取碘水中的碘,可采用
(3)除去食盐溶液中的水,可采用
(4)淡化海水,可采用
(5)丙酮是一种常用的有机溶剂,可与水以任意比互溶,密度小于水,沸点约为55℃,分离水和丙酮的混合物时可采用
【知识点】 物质分离、提纯的常见物理方法 蒸馏与分馏解读 萃取和分液解读
您最近一年使用:0次
填空题
|
较易(0.85)
17. 某实验室需要 480 mL0.5 mol/L的NaOH溶液,请回答下列问题:
(1)应称取 NaOH 的质量为_______ g,应选用_______ mL 容量瓶。
(2)除容量瓶外还需要的其他玻璃仪器有_______ 、_______ 及玻璃棒。
(3)配制溶液时,其正确的操作顺序是(用字母表示,每个操作只能用一次)_______ 。
A.将容量瓶盖紧,振荡、摇匀
B.用托盘天平准确称量所需的 NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
C.用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将已冷却的溶液沿玻璃棒注入容量瓶中
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm 处
(1)应称取 NaOH 的质量为
(2)除容量瓶外还需要的其他玻璃仪器有
(3)配制溶液时,其正确的操作顺序是(用字母表示,每个操作只能用一次)
A.将容量瓶盖紧,振荡、摇匀
B.用托盘天平准确称量所需的 NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
C.用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将已冷却的溶液沿玻璃棒注入容量瓶中
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm 处
您最近一年使用:0次
七、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
18. 某工厂的工业废水中含有大量的 FeSO4、较多的 Cu2+和少量的 Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图完成回收硫酸亚铁和铜的简单实验方案,回答下列问题:(流程图中无需填写)
(1)操作②的名称为__________ ,所需要的玻璃仪器为________ 、___________ 、烧杯。
(2)试剂⑤的化学式为___________ ,所发生的化学方程式为__________ 。
(3) 对④和⑧的混合溶液,不选用蒸发(余热蒸干)获得FeSO4·7H2O,原因是_________ 、___________ 。(说出两点原因)

(1)操作②的名称为
(2)试剂⑤的化学式为
(3) 对④和⑧的混合溶液,不选用蒸发(余热蒸干)获得FeSO4·7H2O,原因是
【知识点】 亚铁盐 物质分离、提纯综合应用解读 常见无机物的制备解读
您最近一年使用:0次
2017-10-18更新
|
309次组卷
|
2卷引用:湖南省长郡中学2017-2018学年高一上学期第一次模块检测理科综合化学试题
八、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
19. 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_________ mol·L -1 。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________ 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生取上述浓盐酸100mL,
①若加水稀释到500 mL,所得盐酸的物质的量浓度为________ mol·L -1 。
②若需使该溶液的质量分数变为原来的 ,应该加
,应该加______ mL蒸馏水。
③若需使该溶液的物质的量浓度变为原来的 ,需加蒸馏水的体积
,需加蒸馏水的体积______ 119mL(该空填“>”“<”或“=”)。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19 g·cm-3 HCl的质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生取上述浓盐酸100mL,
①若加水稀释到500 mL,所得盐酸的物质的量浓度为
②若需使该溶液的质量分数变为原来的
 ,应该加
,应该加③若需使该溶液的物质的量浓度变为原来的
 ,需加蒸馏水的体积
,需加蒸馏水的体积
您最近一年使用:0次
2018-04-01更新
|
293次组卷
|
2卷引用:湖北省黄冈中学2017-2018学年高一上学期第一次月考化学试题
九、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
20. 欲提纯混有硫酸钠、碳酸氢铵的氯化钠固体,某学生设计了如下方案∶
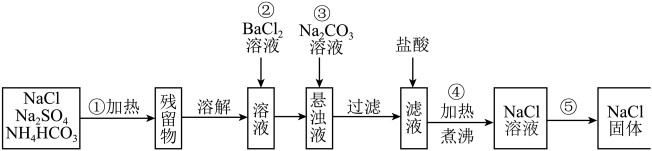
请根据上述操作流程回答下列问题:
(1)操作①在加热时应选择_______ (填仪器名称)盛装混合物。
(2)进行操作②后,判断SO 已沉淀完全的方法是
已沉淀完全的方法是_______ 。
(3)操作④的目的是_______ 。
(4)实验室进行操作⑤的具体步骤是_______ 。
(5)某同学欲用制得的氣化钠固体配制100mL 0.2mol•L-1的氯化钠溶液。
①配制NaCl溶液时需要用到的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、_______ 。
②下列操作会使所配制的氯化钠溶液浓度偏低的是_______ (填字母)。
A.加水定容时俯视刻度线
B.容量瓶内壁附有水珠而未进行干燥处理
C.在溶解过程中有少量液体溅出烧杯
D.颠倒摇匀后发现溶液凹液面低于刻度线又加水补上

请根据上述操作流程回答下列问题:
(1)操作①在加热时应选择
(2)进行操作②后,判断SO
 已沉淀完全的方法是
已沉淀完全的方法是(3)操作④的目的是
(4)实验室进行操作⑤的具体步骤是
(5)某同学欲用制得的氣化钠固体配制100mL 0.2mol•L-1的氯化钠溶液。
①配制NaCl溶液时需要用到的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、
②下列操作会使所配制的氯化钠溶液浓度偏低的是
A.加水定容时俯视刻度线
B.容量瓶内壁附有水珠而未进行干燥处理
C.在溶解过程中有少量液体溅出烧杯
D.颠倒摇匀后发现溶液凹液面低于刻度线又加水补上
您最近一年使用:0次
2021-01-11更新
|
146次组卷
|
3卷引用:专题2 本专题达标检测-高中化学苏教2019版必修第一册
试卷分析
整体难度:适中
考查范围:化学实验基础、认识化学科学、物质结构与性质、有机化学基础、常见无机物及其应用
试卷题型(共 20题)
题型
数量
单选题
13
多选题
2
填空题
3
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 | |
| 2 | 0.85 | 原子结构示意图、离子结构示意图 根据原子结构进行元素种类推断 “位构性”关系理解及应用 | |
| 3 | 0.85 | 有机物分离提纯的几种常见操作 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 | |
| 4 | 0.65 | 胶体的制备 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液实验的误差分析 | |
| 5 | 0.85 | 物质的分离、提纯 物质分离、提纯的常见物理方法 | |
| 6 | 0.94 | 物质的量浓度概念、含义 物质的量浓度与溶液稀释的计算 | |
| 7 | 0.65 | 摩尔质量 22.4L/mol适用条件 阿伏加德罗定律的应用 某溶液与物质的量浓度相关的物理量的判断 | |
| 8 | 0.65 | 焰色试验 一定物质的量浓度的溶液的配制 化学实验基础操作 | |
| 9 | 0.94 | 配制一定物质的量浓度的溶液的步骤、操作 | |
| 10 | 0.65 | 物质的量浓度的计算 物质的量浓度计算-溶液稀释的有关计算 常用仪器及使用 | |
| 12 | 0.85 | 物质的量浓度计算-溶液配制有关计算 一定物质的量浓度的溶液的配制 | |
| 14 | 0.4 | 物质的量浓度的计算 | |
| 15 | 0.85 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 二、多选题 | |||
| 11 | 0.65 | 焰色试验 配制一定物质的量浓度的溶液的步骤、操作 蒸发与结晶 | |
| 13 | 0.85 | 物质的量浓度概念、含义 物质的量浓度的计算 物质的量浓度计算-与溶质成分有关的计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 三、填空题 | |||
| 16 | 0.85 | 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 | |
| 17 | 0.85 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的仪器 | |
| 19 | 0.65 | 物质的量浓度的计算 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液配制有关计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 四、解答题 | |||
| 18 | 0.65 | 亚铁盐 物质分离、提纯综合应用 常见无机物的制备 | 实验探究题 |
| 20 | 0.65 | 离子反应在生活、生产中的应用 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | 实验探究题 |



