一定温度下,在容积为2L的密闭容器中进行反应:aN(g) bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
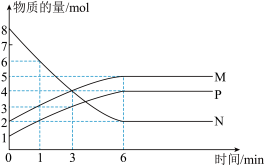
(1)反应化学方程式中各物质的系数比为a:b:c=______ 。
(2)1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:_____ 。
(3)下列叙述中能说明上述反应达到平衡状态的是______ 。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗amolN,同时消耗bmolM
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
 bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
(1)反应化学方程式中各物质的系数比为a:b:c=
(2)1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:
(3)下列叙述中能说明上述反应达到平衡状态的是
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗amolN,同时消耗bmolM
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
更新时间:2020/04/19 15:16:30
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)对于下列反应:2SO2(g) + O2(g) 2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为
2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为 __________________ 。
(2)下图表示在密闭容器中反应:2SO2+O2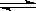 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是___________________ ; 请将增大压强时的反应速率变化情况画在c~d处:___________
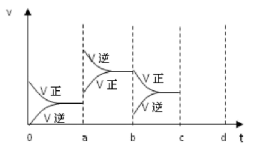
(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内混合气体的平均相对分子质量比原平衡时___________ (填“增大”、“减小”或“相等”)。
 2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为
2SO3(g),如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的反应速率为 (2)下图表示在密闭容器中反应:2SO2+O2
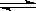 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是
(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内混合气体的平均相对分子质量比原平衡时
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】CH3OH 是一种无色有刺激性气味的液体,在生产生活中有重要用途。
Ⅰ.目前工业上有一种方法是用 CO2生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:
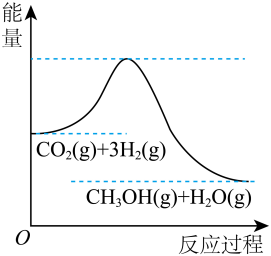
(1)你认为该反应为_____ (填放热或吸热)反应.
(2)恒容容器中,对于以上反应,能加快反应速率的是_____ 。
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=_____ 。
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是_____ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:____________________________ 。
Ⅰ.目前工业上有一种方法是用 CO2生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:

(1)你认为该反应为
(2)恒容容器中,对于以上反应,能加快反应速率的是
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学反应速率和限度与生产、生活密切相关。请回答下列问题。
(1)在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正、逆反应速率大小
时刻,正、逆反应速率大小
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②若 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率为
时刻用M的浓度变化表示的平均反应速率为___________ 。
③能使逆反应速率增大的措施有___________ (任写两点)。
(2)在2L密闭容器内,800℃时仅发生反应 ,体系中开始仅含有NO和
,体系中开始仅含有NO和 ,且物质的量之比为1:1,
,且物质的量之比为1:1, 随时间的变化如下表所示:
随时间的变化如下表所示:
①3s时,生成 的物质的量为
的物质的量为___________ mol,在第5s时,NO的转化率为___________ 。
②如图中表示 变化曲线的是
变化曲线的是___________ (填字母)。___________ (填字母)
a.每消耗1mol ,生成2mol的
,生成2mol的
b.各物质组分的物质的浓度不再改变
c.混合气体的平均相对分子质量不变
d.容器内密度保持不变
(1)在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
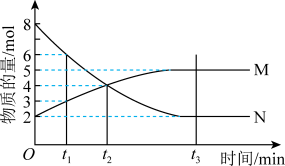
 时刻,正、逆反应速率大小
时刻,正、逆反应速率大小
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②若
 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率为
时刻用M的浓度变化表示的平均反应速率为③能使逆反应速率增大的措施有
(2)在2L密闭容器内,800℃时仅发生反应
 ,体系中开始仅含有NO和
,体系中开始仅含有NO和 ,且物质的量之比为1:1,
,且物质的量之比为1:1, 随时间的变化如下表所示:
随时间的变化如下表所示:| 时间/s | 0 | 1 | 2 | 3 | 4 |
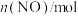 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 |
 的物质的量为
的物质的量为②如图中表示
 变化曲线的是
变化曲线的是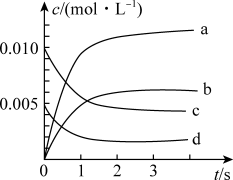
a.每消耗1mol
 ,生成2mol的
,生成2mol的
b.各物质组分的物质的浓度不再改变
c.混合气体的平均相对分子质量不变
d.容器内密度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ. CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+1/2O2(g) CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______ (填字母)。
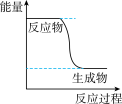
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=________________ ,则CH3OH的转化率为___________ 。
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
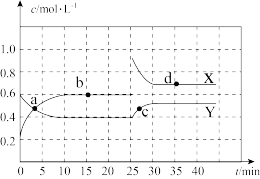
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)______________________________ 。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是___________ 。
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为________ ,负极的电极反应式为_______________________________ 。当反应中收集到标准状况下224 mL气体时,消耗的a电极质量为________ g。
(1)已知CH3OH(g)+1/2O2(g)
 CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】298K时,将一定物质的量浓度的Na3AsO3、I2和NaOH三种溶液混合,发生反应:AsO (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq) AsO
AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
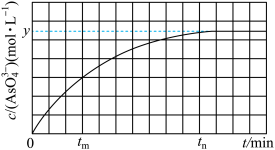
(1)tm时,v(正)_____ v(逆)(填“>”“<”或“=”)。
(2)从0到tn时,v(OH-)=_____ 。
(3)下列可判断反应达到平衡的是_____ (填标号)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO )
)
c.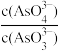 不再变化
不再变化
 (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq) AsO
AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
(1)tm时,v(正)
(2)从0到tn时,v(OH-)=
(3)下列可判断反应达到平衡的是
a.溶液的pH不再变化
b.v(I-)=2v(AsO
 )
)c.
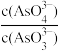 不再变化
不再变化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图:
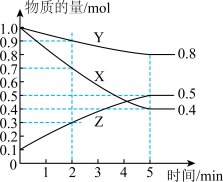
①该反应的化学方程式是_______ 。
②2min内X的转化率为_______ 。
(2)KMnO4是实验室中常用的一种试剂。回答下列问题:
①在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4弱酸)溶液,振荡,溶液紫色变无色。发生的化学反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+1OCO2↑+ 8H2O,若将该反应设计成原电池,则正极反应式为_______ 。
②在10mL 0.1 mol/L KMnO4溶液(含稀硫酸)中加入15 mL0.5 mol/L草酸溶液,收集到的CO2的量与时间的关系如图所示。AB段反应速率增大的原因可能是_______ (填字母)。
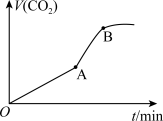
A.该反应是放热反应 B.反应物浓度增大
C.K2SO4起催化作用 D.MnSO4起催化作用
(1)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图:

①该反应的化学方程式是
②2min内X的转化率为
(2)KMnO4是实验室中常用的一种试剂。回答下列问题:
①在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4弱酸)溶液,振荡,溶液紫色变无色。发生的化学反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+1OCO2↑+ 8H2O,若将该反应设计成原电池,则正极反应式为
②在10mL 0.1 mol/L KMnO4溶液(含稀硫酸)中加入15 mL0.5 mol/L草酸溶液,收集到的CO2的量与时间的关系如图所示。AB段反应速率增大的原因可能是

A.该反应是放热反应 B.反应物浓度增大
C.K2SO4起催化作用 D.MnSO4起催化作用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上常用氮气与氢气来合成氨气,温度控制在500℃,采用铁催化剂,压强控制在20~50 MPa。
(1)该反应的化学方程式为_______ 。
(2)它的平衡常数表达式为_______ 。
(3)工业合成氨时,采用氮氢循环操作的主要目的是_______。
(4)在一体积10 L的密闭容器中充入了280 g  、100 g
、100 g  ,反应10分钟后,测得有34 g
,反应10分钟后,测得有34 g  生成,则用
生成,则用 表示该反应的速率为
表示该反应的速率为_______ 。
(5)下列判断可以作为该反应达到平衡的标志的是_______。
(6)氨气常用来生产化肥 ,铵态氮肥不宜长期施用,请结合化学用语解释
,铵态氮肥不宜长期施用,请结合化学用语解释_______ 。
(7)工业上常用氨气来制备硝酸,其中第1步是用氨气与纯氧在 的催化作用加热下制得NO和水。请写出这个反应的化学方程式并配平
的催化作用加热下制得NO和水。请写出这个反应的化学方程式并配平_______ 。该反应中,还原剂是_______ 。
(1)该反应的化学方程式为
(2)它的平衡常数表达式为
(3)工业合成氨时,采用氮氢循环操作的主要目的是_______。
| A.加快反应速率 | B.提高氨气的平衡浓度 |
| C.降低氨气的沸点 | D.提高 和 和 的利用率 的利用率 |
 、100 g
、100 g  ,反应10分钟后,测得有34 g
,反应10分钟后,测得有34 g  生成,则用
生成,则用 表示该反应的速率为
表示该反应的速率为(5)下列判断可以作为该反应达到平衡的标志的是_______。
| A.单位时间内每消耗1摩尔氮气的同时消耗3摩尔氢气 |
| B.混合气体的平均分子量不再发生变化 |
| C.混合气体的密度保持不变 |
| D.体系的温度不再变化 |
 ,铵态氮肥不宜长期施用,请结合化学用语解释
,铵态氮肥不宜长期施用,请结合化学用语解释(7)工业上常用氨气来制备硝酸,其中第1步是用氨气与纯氧在
 的催化作用加热下制得NO和水。请写出这个反应的化学方程式并配平
的催化作用加热下制得NO和水。请写出这个反应的化学方程式并配平
您最近一年使用:0次
【推荐2】已知2X2(g)+Y2(g) 2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
(1)此反应平衡常数表达式为___ ;若将温度降低到300℃,则反应平衡常数将___ (填增大、减少或不变)。
(2)能说明反应已达平衡状态的是___
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内的密度保持不变
(3)若将上述容器改为恒压容器 反应器开始体积相同
反应器开始体积相同 ,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将
,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将____ (填变大、变小或不变)。
 2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。(1)此反应平衡常数表达式为
(2)能说明反应已达平衡状态的是
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内的密度保持不变
(3)若将上述容器改为恒压容器
 反应器开始体积相同
反应器开始体积相同 ,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将
,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在2L密闭容器内,800℃时反应2NO(g)+O2(g)→2NO2(g)体系中,n(NO)随时间的变化如表:
(1)上述反应_____ (填“是”或“不是”)可逆反应。
(2)如图所示,表示NO2变化曲线的是____ 。用O2表示0~1s内该反应的平均速率v=____ 。
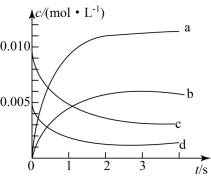
(3)能说明该反应已达到平衡状态的是____ (填字母)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应
(2)如图所示,表示NO2变化曲线的是

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
您最近一年使用:0次



