根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的 ,其外围电子排布图是
,其外围电子排布图是__________ 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是____ ,价层电子排布式_________ ,在元素周期表中的位置是____________ 。
(3)C元素基态原子的电子排布图是下图中的____ (填序号),另一个不能作为基态原子的电子排布图因为它不符合__ (填序号)。
①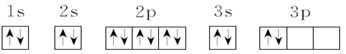
②
A.能量最低原理 B.泡利原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为E)。如图所示:
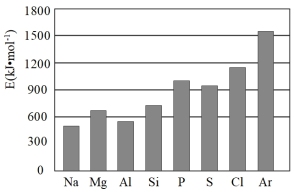
①同周期内,随着原子序数的增大,E值变化的总趋势是____ ;
②根据图中提供的信息,可推断出E氧____ E氟(填“>”“<”或“=”,下同);
③根据第一电离能的含义和元素周期律,可推断出E镁___ E钙。
(5)判断BCl3分子的空间构型、中心原子成键时采取的杂化轨道类型及分子中共价键的键角:________ 、___________ 、____________ 。
(1)A元素次外层电子数是最外层电子数的
 ,其外围电子排布图是
,其外围电子排布图是(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是
(3)C元素基态原子的电子排布图是下图中的
①

②

A.能量最低原理 B.泡利原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为E)。如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是
②根据图中提供的信息,可推断出E氧
③根据第一电离能的含义和元素周期律,可推断出E镁
(5)判断BCl3分子的空间构型、中心原子成键时采取的杂化轨道类型及分子中共价键的键角:
更新时间:2020/04/28 18:48:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】完成下列问题
(1)基态 的核外电子排布式
的核外电子排布式___________ 。
(2)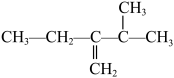 的系统命名法为
的系统命名法为___________ ,
(3)苯酚钠溶液中通入少量二氧化碳反应的离子方程式___________ 。
(4)肉桂醛(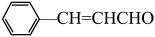 )发生银镜反应的化学方程式
)发生银镜反应的化学方程式___________ 。
(1)基态
 的核外电子排布式
的核外电子排布式(2)
 的系统命名法为
的系统命名法为(3)苯酚钠溶液中通入少量二氧化碳反应的离子方程式
(4)肉桂醛(
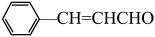 )发生银镜反应的化学方程式
)发生银镜反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图所示是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
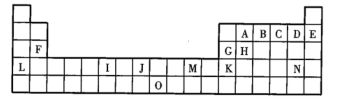
试回答下列问题:(涉及字母的均用元素符号作答)
(1)I的元素符号为______ ,在周期表中位于______ 区。
(2)写出基态A原子核外电子的轨道表示式______ ,写出J元素基态原子的价电子排布式______ ,J在周期表中的位置是______ 。
(3)A、B、G、H的原子半径由大到小的顺序是______ ;A、B、C、D的第一电离能由大到小的顺序是______ ;A、B、C、D的电负性由大到小的顺序是______ 。

试回答下列问题:(涉及字母的均用元素符号作答)
(1)I的元素符号为
(2)写出基态A原子核外电子的轨道表示式
(3)A、B、G、H的原子半径由大到小的顺序是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表是学习物质结构和性质的重要工具,元素周期律反映了元素性质的周期性变化规律。
(1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有______ 种不同运动状态的电子,该原子核外共有______ 种能量不同的电子。元素A与氢元素形成的分子,其空间结构可能是(填序号)________________ 。
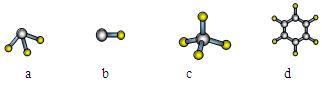
(2)下列变化规律中正确的是______ 。
A.金属K、Na、Mg的熔沸点由低到高
B.C1-、Br-、I-的失电子能力由弱到强
C.H+、Li+、H-的半径由大到小
D.H3PO4、HClO4、H2SO4的酸性由弱到强
(3)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中A的电子式为______ ,E的化学式为______ 。
(1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有

(2)下列变化规律中正确的是
A.金属K、Na、Mg的熔沸点由低到高
B.C1-、Br-、I-的失电子能力由弱到强
C.H+、Li+、H-的半径由大到小
D.H3PO4、HClO4、H2SO4的酸性由弱到强
(3)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中A的电子式为
| 氢化物 | A | B | HF | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 | -33 | -164 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】硼及其化合物在制造、化工等领域都有广泛应用,回答下列问题:
(1)基态硼原子的价电子排布图为__________ ,其占据最高能级电子的电子云轮廓图形状为__________ ,基态硼原子比基态氮原子的第一电离能 小,其原因为
小,其原因为__________ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:
① 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为__________ 。
② 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为__________ 。
③ 的键角为
的键角为__________ 。
(3)写出B与 溶液反应的离子方程式:
溶液反应的离子方程式:__________ 。
(4) 为一元弱酸[常温下,
为一元弱酸[常温下,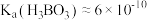 ]:
]:
① 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为__________ 。
②常温下, 的硼酸的pH约为
的硼酸的pH约为__________ (已知: ,
, )。
)。
(1)基态硼原子的价电子排布图为
 小,其原因为
小,其原因为(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:①
 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为②
 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为③
 的键角为
的键角为(3)写出B与
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)
 为一元弱酸[常温下,
为一元弱酸[常温下,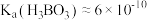 ]:
]:①
 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为②常温下,
 的硼酸的pH约为
的硼酸的pH约为 ,
, )。
)。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】碱金属的电离能与碱金属的活泼性存在什么联系?___________
您最近半年使用:0次
【推荐3】按要求回答下列问题:
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
A通常显___________ 价,B的基态原子核外电子排布式为___________ 。
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:___________ (填元素符号)。
②同主族内不同元素的X值变化的特点是___________ ;同周期内,随着原子序数的增大,X值的变化总趋势是___________ 。周期表中X值的这种变化特点体现了元素性质的___________ 变化规律。
③X值较小的元素集中在元素周期表的___________ (填字母)。
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是___________ (填字母)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
电离能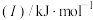 |  | 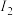 | 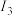 |  |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:
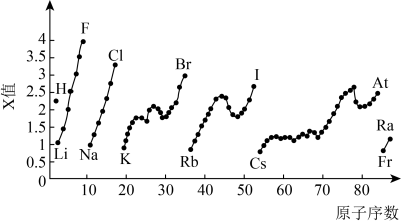
②同主族内不同元素的X值变化的特点是
③X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 、
、 、
、 是重要的
是重要的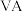 族化合物。回答下列问题:
族化合物。回答下列问题:
(1)固体 属于
属于_______ 晶体, 的VSEPR模型是
的VSEPR模型是_______ 。
(2)乙二胺( )易溶于水,可用于制造燃料、药物等。
)易溶于水,可用于制造燃料、药物等。
①C、N、O元素的电负性由大到小的顺序为_______ 。
②乙二胺易溶于水的原因是_______ ,其分子中采取 杂化的原子是
杂化的原子是_______ (填元素符号)。
(3) 分子中含有σ键的数目为
分子中含有σ键的数目为_______ ,其晶体中含有的作用力为_______ (填标号)。
a.氢键 b.离子键 c.极性键 d.范德华力
 、
、 、
、 是重要的
是重要的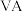 族化合物。回答下列问题:
族化合物。回答下列问题:(1)固体
 属于
属于 的VSEPR模型是
的VSEPR模型是(2)乙二胺(
 )易溶于水,可用于制造燃料、药物等。
)易溶于水,可用于制造燃料、药物等。①C、N、O元素的电负性由大到小的顺序为
②乙二胺易溶于水的原因是
 杂化的原子是
杂化的原子是(3)
 分子中含有σ键的数目为
分子中含有σ键的数目为a.氢键 b.离子键 c.极性键 d.范德华力
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ,Sm的价层电子排布式4f66s2,Sm3+的价层电子排布式为___________ 。
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子占据最高能级的电子云轮廓图为___________ 形。
②离子半径Li+___________ H-(填“>”“=”或“<”)。
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是___________ (填“金属”或“非金属”),该化合物中显负价的是___________ (填“X”或“Y”)。
(4) 的空间构型为
的空间构型为___________ ;O3是___________ 分子(填“极性”或“非极性”)。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为
②离子半径Li+
(3)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是
(4)
 的空间构型为
的空间构型为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知运送卫星的火箭所需燃料除液态过氧化氢外,还有另一种液态氮氢化合物。已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键。
(1)该氮氢化合物的结构式为______ ,其中N原子采取_____ 杂化方式,该分子是_____ (填“极性”或“非极性”)分子。
(2)若该物质与液态过氧化氢恰好完全反应,产生两种无毒又不污染环境的气态物质,在该反应的反应物和生成物中既含有极性键又含有非极性键的是______ ,只含有非极性键的是_____ ,只含有极性键的是______ 。
(1)该氮氢化合物的结构式为
(2)若该物质与液态过氧化氢恰好完全反应,产生两种无毒又不污染环境的气态物质,在该反应的反应物和生成物中既含有极性键又含有非极性键的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮元素在有机化学中有很重要的地位。请回答下列问题:
(1)基态氮原子的价层电子排布图为___________ 。
(2)2022年11月发射搭载神舟十五号载人飞船的长征二号火箭燃料为偏二甲肼 ,其中所含元素电负性从大到小的顺序为
,其中所含元素电负性从大到小的顺序为___________ 。
(3)N-甲基咪唑( )用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是
)用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是___________ 。
(4)吡啶( )在水中的溶解度远大于苯,可能原因是①
)在水中的溶解度远大于苯,可能原因是①___________ ;②___________ 。
(5)有机物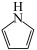 常用作医药原料、有机合成等,分子中
常用作医药原料、有机合成等,分子中 键与
键与 键之比为
键之比为___________ 。
(1)基态氮原子的价层电子排布图为
(2)2022年11月发射搭载神舟十五号载人飞船的长征二号火箭燃料为偏二甲肼
 ,其中所含元素电负性从大到小的顺序为
,其中所含元素电负性从大到小的顺序为(3)N-甲基咪唑(
 )用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是
)用作有机合成中间体和树脂固化剂、粘合剂等,分子中碳原子的杂化轨道类型是(4)吡啶(
 )在水中的溶解度远大于苯,可能原因是①
)在水中的溶解度远大于苯,可能原因是①(5)有机物
 常用作医药原料、有机合成等,分子中
常用作医药原料、有机合成等,分子中 键与
键与 键之比为
键之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】臭氧有强氧化性能在一定条件下将烟气中的 、
、 分别氧化为
分别氧化为 和
和 。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
(1) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_______ ; 的空间构型为
的空间构型为_______ (用文字描述)。
(2) 基态核外外层电子排布式为
基态核外外层电子排布式为_______ 。
(3)臭氧可用于含 碱性电镀废水的处理。第ⅰ步:
碱性电镀废水的处理。第ⅰ步: 转化为
转化为 ;第ⅱ步:
;第ⅱ步: 继续转化为
继续转化为 及两种单质气体。若第ⅱ步转化时,
及两种单质气体。若第ⅱ步转化时, 与
与 物质的量之比为3:2,该步反应的离子方程式为
物质的量之比为3:2,该步反应的离子方程式为_______ 。
(4)为测定大气中臭氧( )含量,将0℃、
)含量,将0℃、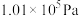 的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L
的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L 溶液进行滴定恰好到达终点。(已知:
溶液进行滴定恰好到达终点。(已知: )
)
① 与KI溶液反应生成两种单质,则反应的化学方程式
与KI溶液反应生成两种单质,则反应的化学方程式_______ 。
②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是_______ ;
③该实验中可选用_______ (填物质名称)作指示剂。空气中臭氧的体积分数为_______ 。
④甲同学认为在滴定前应微热溶液、以排除溶液中溶解的 和
和 ,不然会使滴定结果偏
,不然会使滴定结果偏_______ (填“低”或“高”)。
 、
、 分别氧化为
分别氧化为 和
和 。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。(1)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为(2)
 基态核外外层电子排布式为
基态核外外层电子排布式为(3)臭氧可用于含
 碱性电镀废水的处理。第ⅰ步:
碱性电镀废水的处理。第ⅰ步: 转化为
转化为 ;第ⅱ步:
;第ⅱ步: 继续转化为
继续转化为 及两种单质气体。若第ⅱ步转化时,
及两种单质气体。若第ⅱ步转化时, 与
与 物质的量之比为3:2,该步反应的离子方程式为
物质的量之比为3:2,该步反应的离子方程式为(4)为测定大气中臭氧(
 )含量,将0℃、
)含量,将0℃、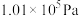 的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L
的空气V L慢慢通过足量KI溶液,使臭氧完全反应:然后将所得溶液用a mL的c mol/L 溶液进行滴定恰好到达终点。(已知:
溶液进行滴定恰好到达终点。(已知: )
)①
 与KI溶液反应生成两种单质,则反应的化学方程式
与KI溶液反应生成两种单质,则反应的化学方程式②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是
③该实验中可选用
④甲同学认为在滴定前应微热溶液、以排除溶液中溶解的
 和
和 ,不然会使滴定结果偏
,不然会使滴定结果偏
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】图一是Na、Cu、Si、H、C、N等元素单质的熔点高低顺序,其中c、d均为热和电的良导体。
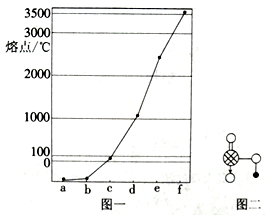
(1)单质d对应元素的基态原子M层电子排布式为_____ ,该元素位于元素周期表的____ 区。
(2)单质a、f对应的元素以原子个数比1 : 1形成的分子(相同条件下对H2的相对密度为13)中含σ键和π键的个数比为____ ,该分子中心原子的杂化轨道类型为________ 。
(3)单质b对应元素原子的最高能级电子云轮廓图形状为____ 形,将b的简单氢化 物溶于水后的溶液滴加到AgNO3溶液中至过量,所得络离子的结构可用示意图表示为_______ 。
(4)图二是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的两个原因_____________ 。

(1)单质d对应元素的基态原子M层电子排布式为
(2)单质a、f对应的元素以原子个数比1 : 1形成的分子(相同条件下对H2的相对密度为13)中含σ键和π键的个数比为
(3)单质b对应元素原子的最高能级电子云轮廓图形状为
(4)图二是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的两个原因
您最近半年使用:0次



