(1)氯酸是一种强酸,氯酸的浓度超过40%就会迅速分解,生成有毒气体,反应的化学方程式为8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O。所得混合气体的平均相对分子质量为________ 。
(2)实验室可用软锰矿(主要成分为MnO2)制取KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3 (s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为________ 。
(3)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、 、
、 、
、 。
。
①该反应的离子方程式为________________________ 。在锰离子转化为高锰酸根离子的反应中,如果把反应后的溶液稀释到1 L,测得溶液的pH=2,则在反应中转移电子的物质的量为________ mol。(结果写成小数,保留三位有效数字)
②在测定锰离子浓度的实验中,需要配制250 mL 0.10mol/L KIO4的标准溶液,应用托盘天平称取______ g KIO4固体。
③下列有关配制溶液的操作或判断正确的是( )
A.使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
B.容量瓶用蒸馏水洗净后,没有烘干就用来配制溶液
C.定容摇匀后液面下降再加水到刻度线,不影响所配溶液浓度
D.定容时仰视刻度线会导致所配溶液浓度偏高
E.当容量瓶中的液面距离刻度线2~3cm时改用胶头滴管加水定容
(2)实验室可用软锰矿(主要成分为MnO2)制取KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3 (s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为
(3)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、
 、
、 、
、 。
。①该反应的离子方程式为
②在测定锰离子浓度的实验中,需要配制250 mL 0.10mol/L KIO4的标准溶液,应用托盘天平称取
③下列有关配制溶液的操作或判断正确的是
A.使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
B.容量瓶用蒸馏水洗净后,没有烘干就用来配制溶液
C.定容摇匀后液面下降再加水到刻度线,不影响所配溶液浓度
D.定容时仰视刻度线会导致所配溶液浓度偏高
E.当容量瓶中的液面距离刻度线2~3cm时改用胶头滴管加水定容
更新时间:2020-04-28 14:11:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学方程式中各物质的化学计量数之比等于粒子个数之比,也等于各物质的___________ 之比,对于有气体参与的反应还等于___________ 之比。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)标准状况下,1.7g H2S的体积为___________ L
(2)同温同压下,气体N2和O2的密度之比为___________
(3)同温同压下,等体积的气体SO2和CO的物质的量之比为___________
(4)标准状况下,0.66g某气态氧化物RO2的体积为336mL,则元素R的相对原子质量为___________
(5)将7.8g Na2O2溶于93.8g水中充分反应后,所得溶液的质量分数为___________
(1)标准状况下,1.7g H2S的体积为
(2)同温同压下,气体N2和O2的密度之比为
(3)同温同压下,等体积的气体SO2和CO的物质的量之比为
(4)标准状况下,0.66g某气态氧化物RO2的体积为336mL,则元素R的相对原子质量为
(5)将7.8g Na2O2溶于93.8g水中充分反应后,所得溶液的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】【化学-选修2:化学与技术】镁合金废料回收最常用的是熔炼法,其主要工艺流程为:
废料预处理→熔化→除铁→除气和除渣→铸造。
(1)废料预处理包括粉碎、除油污和油漆。
①粉碎方法有干态机械粉碎法和湿喷机械粉碎法,其中容易造成危险的方法是______ ,理由是______________________________________________________ 。
②把油污和油漆一次性除去最适宜的方法是______
A.用热碱洗涤,过滤
B.用有机溶剂溶解,过滤
C.加热气化除去
(2)镁合金在加热到935K时熔化,并不断向其中通入氩气做保护气。若液态镁与空气接触,不但会发生反应产生杂质,而且降低了镁的回收率。写出与空气的两个主要反应方程式___________________ 、___________________ 。
(3)向熔融镁中加入固体硼砂(B2O3)除铁,生成FeB2沉渣,写出有关的化学反应方程式___________ 。
(4)镁合金除了含有铁之外,还含有少量铝。加入C2Cl6可以除去液态镁中的氢气,还能把铝转化为Al4C3沉渣:
C2Cl6→2C+3Cl2 (1)
3C+4Al→Al4C3 (2)
①除气除渣炉排出的污染性气体有_____________ 。
②如果1t镁合金中,铝占3.6‰,则除去铝最少需要加入C2Cl6__________ g。
废料预处理→熔化→除铁→除气和除渣→铸造。
(1)废料预处理包括粉碎、除油污和油漆。
①粉碎方法有干态机械粉碎法和湿喷机械粉碎法,其中容易造成危险的方法是
②把油污和油漆一次性除去最适宜的方法是
A.用热碱洗涤,过滤
B.用有机溶剂溶解,过滤
C.加热气化除去
(2)镁合金在加热到935K时熔化,并不断向其中通入氩气做保护气。若液态镁与空气接触,不但会发生反应产生杂质,而且降低了镁的回收率。写出与空气的两个主要反应方程式
(3)向熔融镁中加入固体硼砂(B2O3)除铁,生成FeB2沉渣,写出有关的化学反应方程式
(4)镁合金除了含有铁之外,还含有少量铝。加入C2Cl6可以除去液态镁中的氢气,还能把铝转化为Al4C3沉渣:
C2Cl6→2C+3Cl2 (1)
3C+4Al→Al4C3 (2)
①除气除渣炉排出的污染性气体有
②如果1t镁合金中,铝占3.6‰,则除去铝最少需要加入C2Cl6
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)按如图所示操作,充分反应后:
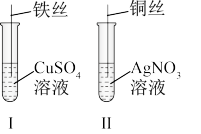
①Ⅰ中发生反应的离子方程式为_______ ;
②Ⅱ中铜丝上观察到的现象是_______ ;
③结合Ⅰ、Ⅱ实验现象可知 、
、 、
、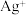 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、 、
、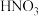 、NO、
、NO、 。该反应物中还原产物是
。该反应物中还原产物是_______ ;若反应方程式中转移了0.3mol电子,则氧化产物的质量是_______ 。
(3)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:_____
_______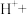 _______
_______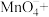 _______
_______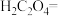 _______
_______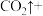 _______
_______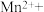 _______
_______
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到的现象是
③结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、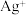 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)某一反应体系中有反应物和生成物共5种物质:S、
 、
、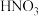 、NO、
、NO、 。该反应物中还原产物是
。该反应物中还原产物是(3)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:
_______
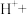 _______
_______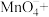 _______
_______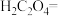 _______
_______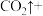 _______
_______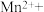 _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据提供的情境书写指定反应的方程式。
一种以 为原料制取
为原料制取 的流程如图所示,450℃,
的流程如图所示,450℃, 在空气中灼烧得到三种锰的氧化物,锰元素所占比例随温度变化的曲线如图所示。
在空气中灼烧得到三种锰的氧化物,锰元素所占比例随温度变化的曲线如图所示。


(1)写出450℃, 在空气中灼烧生成主要产物的化学方程式:
在空气中灼烧生成主要产物的化学方程式:___________ 。
(2)写出“浸取”时 发生反应的离子方程式:
发生反应的离子方程式:___________ 。
一种以
 为原料制取
为原料制取 的流程如图所示,450℃,
的流程如图所示,450℃, 在空气中灼烧得到三种锰的氧化物,锰元素所占比例随温度变化的曲线如图所示。
在空气中灼烧得到三种锰的氧化物,锰元素所占比例随温度变化的曲线如图所示。

(1)写出450℃,
 在空气中灼烧生成主要产物的化学方程式:
在空气中灼烧生成主要产物的化学方程式:(2)写出“浸取”时
 发生反应的离子方程式:
发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)2022年3月13日,永恒的“微火”在万众瞩目中缓缓熄灭,为北京冬奥画上圆满的句号。北京作为双奥之城为世界奉献了一届简约、精彩、卓越的冬奥盛会。
①“微火”不微,照亮世界。奥运火炬“飞扬”的外壳是由聚硅氮烷树脂和碳纤维材料制成,能经受住1200℃的高温。“飞扬”火炬外壳属于____ (填“金属材料”“有机高分子材料”“复合材料”之一)。

②科技“战衣”,助力中国速度。短道速滑“战衣”所用面料能承受碰撞中冰刀的切割,它由聚乙烯(化学式为 )、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为
)、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为_____ (填最简整数比)。
③“氢”车上阵,助力绿色冬奥。氢氧燃料电池就像冬奥大巴车的“心脏”,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,不合理的是____ (填选项序号之一)。

A.H2和O2发生了氧化还原反应
B.该种电池的应用有利于环保
C.该电池的使用过程中,电能转化为化学能
(2)我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。其生产过程中有下列反应:
NaCl+NH3+CO2+H2O=NaHCO3+NH4C1
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
Na2CO3和NaCl的溶解度曲线如图1所示,试回答下列问题:

①将t1℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液分别升温至t2℃,此时所得两溶液的溶质质量分数相比较是____ 。(选填“前者大”“后者大”“相等”之一)。
②t3℃时,将5 g Na2CO3放入试管中,加入10 g水,充分溶解,所得溶液的质量是____ g;然后将试管放入盛有水的烧杯中(如图2所示),再取适量硝酸铵固体放入烧杯内的水中,用玻璃棒搅拌溶解,此时可观察到试管底部固体____ (填“增加”“减少”“无变化”之一)。

③氨盐水比食盐水更容易吸收二氧化碳的原因是_____ 。
④生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,从化学角度说明这句谚语的原理:____ 。
(1)2022年3月13日,永恒的“微火”在万众瞩目中缓缓熄灭,为北京冬奥画上圆满的句号。北京作为双奥之城为世界奉献了一届简约、精彩、卓越的冬奥盛会。
①“微火”不微,照亮世界。奥运火炬“飞扬”的外壳是由聚硅氮烷树脂和碳纤维材料制成,能经受住1200℃的高温。“飞扬”火炬外壳属于

②科技“战衣”,助力中国速度。短道速滑“战衣”所用面料能承受碰撞中冰刀的切割,它由聚乙烯(化学式为
 )、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为
)、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,碳元素和氢元素的质量比为③“氢”车上阵,助力绿色冬奥。氢氧燃料电池就像冬奥大巴车的“心脏”,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,不合理的是

A.H2和O2发生了氧化还原反应
B.该种电池的应用有利于环保
C.该电池的使用过程中,电能转化为化学能
(2)我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。其生产过程中有下列反应:
NaCl+NH3+CO2+H2O=NaHCO3+NH4C1
2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2ONa2CO3和NaCl的溶解度曲线如图1所示,试回答下列问题:

①将t1℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液分别升温至t2℃,此时所得两溶液的溶质质量分数相比较是
②t3℃时,将5 g Na2CO3放入试管中,加入10 g水,充分溶解,所得溶液的质量是

③氨盐水比食盐水更容易吸收二氧化碳的原因是
④生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,从化学角度说明这句谚语的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是硫酸的试剂标签上的部分内容。
某次学生实验需要0.5mol·L-1H2SO4溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
(1)该配制实验中所需98%浓硫酸的体积为___________ mL(保留一位小数)
(2)实验中除量筒、烧杯、玻璃棒外还需要的玻璃仪器:___________ 。
(3)下列操作会引起所配溶液浓度偏大的是___________(填字母)
(4)温度计、量筒、滴定管的一部分如图所示,下述读数(虚线所指刻度)及说法正确的是___________(填字母)。

(5)用所配硫酸与某金属氧化物反应得到200mL某硫酸盐溶液,该溶液中含 1.5NA个,含金属离子NA个,则金属阳离子和硫酸根离子的物质的量浓度比为
1.5NA个,含金属离子NA个,则金属阳离子和硫酸根离子的物质的量浓度比为 ___________
(6)把VmL含有Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成amolNH3(已知 +OH-
+OH- NH3↑+H2O);另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为
NH3↑+H2O);另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为___________ mol/L。
| 硫酸 化学纯(CP级) (500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98 |
(1)该配制实验中所需98%浓硫酸的体积为
(2)实验中除量筒、烧杯、玻璃棒外还需要的玻璃仪器:
(3)下列操作会引起所配溶液浓度偏大的是___________(填字母)
| A.用量筒量取浓硫酸时,仰视量筒的刻度 |
| B.向容量瓶中转移时,有少量液体溅出 |
| C.定容时仰视刻度线 |
| D.定容后倒置摇匀后再正立时,发现液面低于刻度线 |

| A.①是量筒,读数为2.5mL | B.②是量筒,读数为2.5mL |
| C.③是滴定管,读数为2.5mL | D.①是温度计,读数为2.5℃ |
 1.5NA个,含金属离子NA个,则金属阳离子和硫酸根离子的物质的量浓度比为
1.5NA个,含金属离子NA个,则金属阳离子和硫酸根离子的物质的量浓度比为 (6)把VmL含有Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成amolNH3(已知
 +OH-
+OH- NH3↑+H2O);另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为
NH3↑+H2O);另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室欲用质量分数为 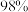 、密度为
、密度为 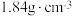 的浓硫酸配制
的浓硫酸配制  的稀硫酸。配制步骤包括:①计算所用浓硫酸的体积;②转移;③定容、摇匀;④量取一定体积的浓硫酸;⑤洗涤;⑥稀释并冷却至室温;⑦轻摇。完成下列问题:
的稀硫酸。配制步骤包括:①计算所用浓硫酸的体积;②转移;③定容、摇匀;④量取一定体积的浓硫酸;⑤洗涤;⑥稀释并冷却至室温;⑦轻摇。完成下列问题:
(1)正确的操作步骤为(填入序号)___________ 。选用的主要仪器有:量筒、烧杯、玻璃棒、___________ 、___________ 。
(2)应量取浓硫酸的体积约为___________ ;量取浓硫酸所用的量筒的规格是___________ (从下列选项中选用)。
A. B.
B.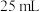 C.
C.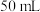 D.
D.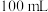
(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是___________ 。
(4)下列情况中,所配制的稀硫酸浓度偏大的是___________ (填序号)。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.洗涤量取浓硫酸使用的量筒,并将洗涤液转移入容量瓶
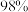 、密度为
、密度为 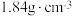 的浓硫酸配制
的浓硫酸配制  的稀硫酸。配制步骤包括:①计算所用浓硫酸的体积;②转移;③定容、摇匀;④量取一定体积的浓硫酸;⑤洗涤;⑥稀释并冷却至室温;⑦轻摇。完成下列问题:
的稀硫酸。配制步骤包括:①计算所用浓硫酸的体积;②转移;③定容、摇匀;④量取一定体积的浓硫酸;⑤洗涤;⑥稀释并冷却至室温;⑦轻摇。完成下列问题:(1)正确的操作步骤为(填入序号)
(2)应量取浓硫酸的体积约为
A.
 B.
B.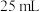 C.
C.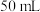 D.
D.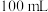
(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
(4)下列情况中,所配制的稀硫酸浓度偏大的是
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
E.洗涤量取浓硫酸使用的量筒,并将洗涤液转移入容量瓶
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学是一门以实验为基础的自然科学。
(1)近年频繁发生的有关化学品泄漏或爆炸事件一次次给我们敲响了安全警钟,操作不当就会存在安全隐患。下列做法正确的是_______________ 。
①将水沿着烧杯内壁缓缓加入浓硫酸中,并用玻璃棒不断搅拌;
②酒精、钠等着火,可以用水扑灭;
③如果发生氯气泄漏,可用沾Na2CO3溶液的湿毛巾捂住口鼻,向上风口或地势高的地方撤离;
④夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风;
⑤不慎将浓硫酸沾到皮肤上,要立即用干布拭去,再用大量水冲洗,然后涂上NaOH溶液;
⑥加热液体的试管口不能对着自己或别人;
⑦实验中当有少量的过氧化钠或金属钠剩余时,用纸包裹好后将其放入垃圾桶中
(2)某同学需要配制0.1mol·L-1的NaHCO3溶液500mL,请根据溶液配制过程中的情况回答下列问题:
①应称取固体NaHCO3的质量为____________________ 。
②实验中除了托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒外还需要的其它仪器有_________________________
③定容观察液面时俯视刻度线,所配溶液浓度_______ (填“偏高”、“偏低”或“无影响”)
④所配的NaHCO3溶液在保存时,常因温度过高而分解,含有少量Na2CO3,若要除去杂质Na2CO3,最简便的方法是_______ ,其反应的离子方程式为_______________________ 。
(1)近年频繁发生的有关化学品泄漏或爆炸事件一次次给我们敲响了安全警钟,操作不当就会存在安全隐患。下列做法正确的是
①将水沿着烧杯内壁缓缓加入浓硫酸中,并用玻璃棒不断搅拌;
②酒精、钠等着火,可以用水扑灭;
③如果发生氯气泄漏,可用沾Na2CO3溶液的湿毛巾捂住口鼻,向上风口或地势高的地方撤离;
④夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风;
⑤不慎将浓硫酸沾到皮肤上,要立即用干布拭去,再用大量水冲洗,然后涂上NaOH溶液;
⑥加热液体的试管口不能对着自己或别人;
⑦实验中当有少量的过氧化钠或金属钠剩余时,用纸包裹好后将其放入垃圾桶中
(2)某同学需要配制0.1mol·L-1的NaHCO3溶液500mL,请根据溶液配制过程中的情况回答下列问题:
①应称取固体NaHCO3的质量为
②实验中除了托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒外还需要的其它仪器有
③定容观察液面时俯视刻度线,所配溶液浓度
④所配的NaHCO3溶液在保存时,常因温度过高而分解,含有少量Na2CO3,若要除去杂质Na2CO3,最简便的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。
(1)X的化学式是___________ 。
(2)用双线桥法标出,上述反应中电子转移的方向和数目___________ 。
(3)上述反应中的还原剂为___________ (填化学式),被还原的元素是___________ (填元素符号)。
(4)向酸性 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是___________ ,反应后溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)0.2mol 参加上述反应,转移电子
参加上述反应,转移电子___________ mol。
 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。(1)X的化学式是
(2)用双线桥法标出,上述反应中电子转移的方向和数目
(3)上述反应中的还原剂为
(4)向酸性
 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是(5)0.2mol
 参加上述反应,转移电子
参加上述反应,转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】认识氧化物的性质,能帮助我们更好地认识自然和保护环境。
(1)摩擦剂是牙膏的主体成分,SiO2是一种常见的摩擦剂。
①Si在元素周期表中的位置是____ 。
②根据用途推测SiO2在水中的溶解性:____ (填“易溶”或“难溶”)。
③比较酸性强弱:H2SO4____ (填“>”或“<”)H2SiO3。
(2)SO2和NO2的任意排放均会污染环境。
①从物质分类角度看,SO2属于酸性氧化物,能与NaOH溶液反应生成亚硫酸盐。写出SO2与过量的NaOH溶液反应的离子方程式:____ 。
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。则反应SO2+Br2+2H2O=H2SO4+2HBr中体现了SO2的____ (填“氧化性”或“还原性”)。
③NO2是一种____ 色的有毒气体,易溶于水,与水反应有无色气体生成,写出NO2与水反应的化学方程式:____ ,反应中每生成标准状况下的气体2.24L,则转移电子的物质的量为____ mol。
(1)摩擦剂是牙膏的主体成分,SiO2是一种常见的摩擦剂。
①Si在元素周期表中的位置是
②根据用途推测SiO2在水中的溶解性:
③比较酸性强弱:H2SO4
(2)SO2和NO2的任意排放均会污染环境。
①从物质分类角度看,SO2属于酸性氧化物,能与NaOH溶液反应生成亚硫酸盐。写出SO2与过量的NaOH溶液反应的离子方程式:
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。则反应SO2+Br2+2H2O=H2SO4+2HBr中体现了SO2的
③NO2是一种
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硝酸是一种重要的化工原料,用来制取一系列硝酸盐类氮肥,如硝酸铵、硝酸钾等;也用来制取硝基的炸药等。有机化工中也用硝酸与丙烯或乙烯、乙二醇作用制取草酸。
(1)某同学对铁与稀硝酸的反应进行探究,若稀HNO3只被还原成NO。
①写出铁与过量稀硝酸反应的离子方程式_______________________________ 。
②写出过量铁与稀硝酸反应的离子方程式_______________________________ 。
③若28克铁与含1.6摩尔硝酸的稀硝酸恰好完全反应,则生成的Fe3+和Fe2+的物质的量之比__________________ 。
④上述反应结束后,向反应后的溶液中加足量氢氧化钠溶液,滤出沉淀洗涤后,在空气中灼烧至质量不变,最终得到的固体质量为_________ g。
(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中的NO3-浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2。
①配平方程式:____ Al+___NO3-+___OH-==___AlO2-+___N2↑+_________。
②上述反应中,还原剂与还原产物的物质的量之比是____ ,反应中转移电子0.3mol,标准状况下生成N2是___________ mL。
(1)某同学对铁与稀硝酸的反应进行探究,若稀HNO3只被还原成NO。
①写出铁与过量稀硝酸反应的离子方程式
②写出过量铁与稀硝酸反应的离子方程式
③若28克铁与含1.6摩尔硝酸的稀硝酸恰好完全反应,则生成的Fe3+和Fe2+的物质的量之比
④上述反应结束后,向反应后的溶液中加足量氢氧化钠溶液,滤出沉淀洗涤后,在空气中灼烧至质量不变,最终得到的固体质量为
(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中的NO3-浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2。
①配平方程式:
②上述反应中,还原剂与还原产物的物质的量之比是
您最近一年使用:0次



