25℃时,Ag2CO3在水中的沉淀溶解平衡曲线如图所示(已知Ksp(AgCl)=1.8×10—10),下列说法正确的是
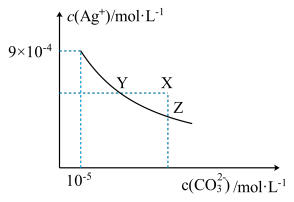

| A.根据图示可计算出Ksp(Ag2CO3)=9×10—9 |
| B.向Ag2CO3饱和溶液中加入K2CO3饱和溶液,可以使Y点移到X点 |
C.反应Ag2CO3(s)+2Cl—(aq) 2AgCl(s)+CO32—(aq)的化学平衡常数K=2.5×108 2AgCl(s)+CO32—(aq)的化学平衡常数K=2.5×108 |
| D.将0.001mol/LAgNO3溶液滴入浓度均为0.001mol/L的KCl和K2CO3的混合溶液,CO32—先沉淀 |
更新时间:2020-04-29 13:41:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.25°C时,等体积的盐酸和醋酸,前者一定比后者的导电能力强 |
| B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl﹣) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,盐酸消耗的NaOH多 |
| D.氯化铜水解的实质是Cu2+与水电离产生的OH﹣结合成弱电解质Cu(OH)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
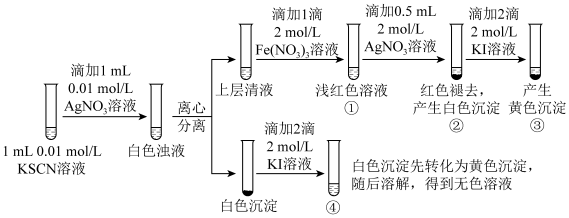
下列说法中,不正确 的是
 (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,
A.①中现象能说明 与 与 生成的白色浊液中存在沉淀溶解平衡 生成的白色浊液中存在沉淀溶解平衡 |
B.②中现象产生的原因是发生了反应: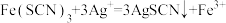 |
| C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 |
D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应 进一步发生了反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象及结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | Fe2(SO4)3溶液蒸发结晶后得到白色固体 | 该固体成分为Fe2O3 |
| B | 向某溶液中加入BaCl2溶液,产生白色沉淀,再加入过量的稀盐酸,沉淀不溶解 | 该溶液中一定含有SO |
| C | Ag2CO3白色悬浊液中滴入几滴Na2S稀溶液,出现黑色沉淀 | Ksp(Ag2S)<Ksp(Ag2CO3) |
| D | 向含有甲基橙的盐酸溶液中滴加氨水直到溶液变为黄色 | 此溶液显碱性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的 、
、 溶液,所得的沉淀溶解平衡图象如下图所示(不考虑
溶液,所得的沉淀溶解平衡图象如下图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是

 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的 、
、 溶液,所得的沉淀溶解平衡图象如下图所示(不考虑
溶液,所得的沉淀溶解平衡图象如下图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
A. 为 为 |
B.n点表示 的不饱和溶液 的不饱和溶液 |
C.在 、 、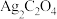 共存的悬浊液中, 共存的悬浊液中, |
D.向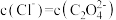 的混合溶液中滴入 的混合溶液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
您最近一年使用:0次

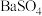 放入水中,对此有关的叙述正确的是
放入水中,对此有关的叙述正确的是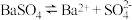
 溶液,Ksp不变,沉淀溶解平衡不移动
溶液,Ksp不变,沉淀溶解平衡不移动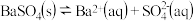
 计测得
计测得 溶液的
溶液的
 是弱酸
是弱酸 溶液中加入
溶液中加入 ,溶液颜色变浅
,溶液颜色变浅 溶液和
溶液和 溶液混合产生白色沉淀和气体
溶液混合产生白色沉淀和气体
 溶液中先滴加
溶液中先滴加 溶液,再滴加
溶液,再滴加 溶液,先生成白色沉淀,后生成黄色沉淀
溶液,先生成白色沉淀,后生成黄色沉淀


