下列说法正确的是( )
| A.25°C时,等体积的盐酸和醋酸,前者一定比后者的导电能力强 |
| B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl﹣) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,盐酸消耗的NaOH多 |
| D.氯化铜水解的实质是Cu2+与水电离产生的OH﹣结合成弱电解质Cu(OH)2 |
更新时间:2020-12-03 18:45:43
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下面是有关弱酸的电离平衡常数。
结合数据,分析下列有关说法,其中错误的是( )
| 弱酸的化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 (25 ℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.反应 + CN - = HCN + + CN - = HCN + 可以发生 可以发生 |
| B.升高温度,HCN溶液中H+浓度增大,平衡正向移动,电离平衡常数增大 |
| C.等浓度的三种酸溶液导电性HCN<H2CO3<CH3COOH |
| D.向CH3COOH溶液中加入少量氢氧化钠固体,平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.一定温度下,将氨水稀释,NH3∙H2O的电离度增大,H2O的电离度也增大 |
| B.水中加酸加碱都会阻碍水的电离,所以c(H+)∙c(OH-)<10-14 |
| C.水中加酸,阻碍水的电离,所以c(H+)=c(OH-)<10-7mol∙L-1 |
| D.醋酸溶液加水稀释,溶液中所有微粒的浓度都会降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学反应原理是研究化学的重要工具,下列相关说法正确的是
A.CH4(g)+Cl2(g)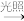 CH3Cl(g)+HCl(g)能自发进行,则该反应 CH3Cl(g)+HCl(g)能自发进行,则该反应 H>0 H>0 |
| B.向碳酸钠溶液中通入少量的氯气:Na2CO3+H2O+2Cl2=2HClO+2NaCl+CO2 |
| C.室温下,稀释0.1 mol/L的HClO溶液,溶液中c(ClO-)减小 |
| D.向硫酸钡悬浊液中加入足量饱和碳酸钠溶液,振荡过滤洗涤,向沉淀中加入盐酸溶液有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温时,0.1mol/L某酸HA溶液的pH=3。关于该溶液叙述正确的是
| A.溶质的电离方程式为HA→H++A- | B.升高温度,溶液的pH增大 |
| C.若加入少量NaA固体,则c(A-)降低 | D.该溶液稀释10倍后,pH < 4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】水是最宝贵的资源之一,下列说法正确的是
A. 的溶液一定呈中性 的溶液一定呈中性 |
B.室温下, 盐酸与等体积水混合后 盐酸与等体积水混合后 |
C.向水中加入固体硫酸铜,水的电离平衡逆向移动, 减小 减小 |
D.25℃时,某溶液中由水电离产生的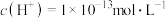 ,该溶液一定显酸性 ,该溶液一定显酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知25℃时,有关弱酸的电离平衡常数:
则下列有关说法不正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A.25℃时,0.1mol·L-1各溶液的pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B.25℃时,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等 |
| C.25℃时,若同浓度的醋酸和氢氧化钠等体积混合,所得溶液pH=8,则c(Na+)-c(CH3COO-)=9.9×10-7mol·L-1 |
| D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确的是
| A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的小 |
| B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明Ksp(AgCl)<Ksp(AgBr) |
| C.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
| D.将0.001 mol·L-1AgNO3溶液分别滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4溶液中先产生Ag2CrO4沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关化学用语表达正确的是
| A.铅蓄电池放电时负极反应式:Pb-2e-=Pb2+ |
B.H2CO3的电离方程式:H2CO3 2H++CO 2H++CO |
C.HS-的水解方程式:HS-+H2O H3O++S2- H3O++S2- |
D.AgCl的溶解平衡表达式:AgCl(s)  Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
您最近一年使用:0次

 所形成的溶液中存在着下列平衡:
所形成的溶液中存在着下列平衡:
 浓度大于
浓度大于 浓度的2倍
浓度的2倍 可得到
可得到 、
、 和
和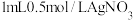 溶液,滴加
溶液,滴加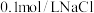 溶液
溶液 ,产生白色沉淀,再滴加2滴
,产生白色沉淀,再滴加2滴 溶液,沉淀由白色变为黄色
溶液,沉淀由白色变为黄色
 溶液,分别滴入2滴
溶液,分别滴入2滴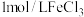 溶液和
溶液和 溶液,加
溶液,加 溶液的试管产生气泡速率更快
溶液的试管产生气泡速率更快 的催化效果强于
的催化效果强于
 计分别测定浓度均为
计分别测定浓度均为 的
的 和
和 的
的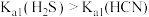
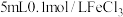 溶液与
溶液与 溶液混合于试管中充分反应后,滴加几滴
溶液混合于试管中充分反应后,滴加几滴 溶液,振荡,溶液变为血红色
溶液,振荡,溶液变为血红色 的反应有一定的限度
的反应有一定的限度

