为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50 mL密度为 1.1 g/cm3的双氧水溶液中, 通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示。请依图回答下列问题:
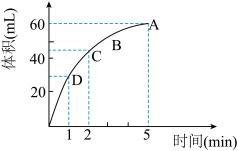
(1)放出一半气体所需要的时间为_____________ ;
(2)A、B、C、D各点反应速率快慢的顺序是______ 。
(3)在5min后,收集到的气体体积不再增加,原因是___________
(4)过氧化氢溶液的初始物质的量浓度为__________

(1)放出一半气体所需要的时间为
(2)A、B、C、D各点反应速率快慢的顺序是
(3)在5min后,收集到的气体体积不再增加,原因是
(4)过氧化氢溶液的初始物质的量浓度为
19-20高一下·山东泰安·期中 查看更多[2]
山东省泰安市新泰市第二中学2019-2020学年高一下学期期中考试化学试题(已下线)专题03 化学反应速率及影响因素、活化能【考题猜想】(9大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
更新时间:2020-05-14 07:55:04
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】Ⅰ.对于 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

(1)定性分析:如图甲可通过观察___________ ,定性比较得出结论。有同学提出将 改为
改为 更为合理,其理由是
更为合理,其理由是___________ 。
(2)定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是___________ 。
Ⅱ.“碘钟”实验中, 的反应速率可以用
的反应速率可以用 与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:
回答下列问题:
(3)表中
___________ 。
(4)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间 的范围为___________(填字母)。
的范围为___________(填字母)。
(5)通过分析比较上表数据,得到的结论是___________ 。
 分解反应,
分解反应, 也有一定的催化作用。为比较
也有一定的催化作用。为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察
 改为
改为 更为合理,其理由是
更为合理,其理由是(2)定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
Ⅱ.“碘钟”实验中,
 的反应速率可以用
的反应速率可以用 与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小反应速率越大。某探究性学习小组在20℃时进行实验,得到的数据如下表:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
 /(mol·L /(mol·L ) ) | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
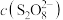 /(mol·L /(mol·L ) ) | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 |  |
(3)表中

(4)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间
 的范围为___________(填字母)。
的范围为___________(填字母)。A.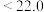 s s | B.22.0~44.0s | C.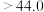 s s | D.数据不足,无法判断 |
(5)通过分析比较上表数据,得到的结论是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(共7分、每空1分)
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有_______ 和_________ 。
(2)元素周期表共有____ 周期,_____ 族;同一周期元素的原子____________ 相同。
(3)在 H、
H、 H、
H、 H、
H、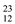 Mg、
Mg、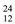 Mg和
Mg和 Cu中共有
Cu中共有______ 种元素,______ 种原子。
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有
(2)元素周期表共有
(3)在
 H、
H、 H、
H、 H、
H、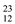 Mg、
Mg、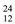 Mg和
Mg和 Cu中共有
Cu中共有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
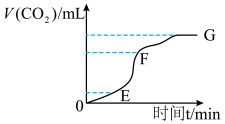
【推荐3】用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如下图所示,分析判断:________ 段化学反应速率最快,_______ 段收集的二氧化碳气体最多。
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)_______________
(1)实验过程如下图所示,分析判断:

(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在容积为1L的密闭容器中,进行如下反应:
A(g)+2B(g) C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
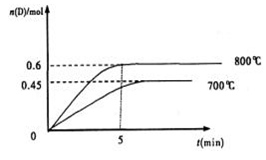
(1)800℃ 时,0—5min内,以B表示的平均反应速率为_________ 。
(2)能判断该反应达到化学平衡状态的依据是___________ 。
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=______________ ,该反应为_______ 反应(填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应_________ 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
A(g)+2B(g)
 C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
(1)800℃ 时,0—5min内,以B表示的平均反应速率为
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(标准状况),实验记录如下(累计值):
(1)在0~1 min、1~2 min、2~3 min、3~4 min、4~5 min时间段中,反应速率最大的时间段是________ ,原因为______________________ ;反应速率最小的时间段是________ ,原因为__________________________ 。
(2)在2~3 min内,用盐酸的浓度变化表示的反应速率为________ 。
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液,其中可行的是________ 。
A.蒸馏水 B.Na2SO4溶液
C.NaNO3溶液 D.Na2CO3溶液
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
(1)在0~1 min、1~2 min、2~3 min、3~4 min、4~5 min时间段中,反应速率最大的时间段是
(2)在2~3 min内,用盐酸的浓度变化表示的反应速率为
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液,其中可行的是
A.蒸馏水 B.Na2SO4溶液
C.NaNO3溶液 D.Na2CO3溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:
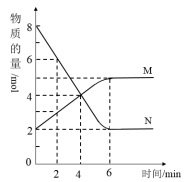
(1)反应的化学方程式为___ 。
(2)反应达到最大限度的时间是___ min,该时间内的平均反应速率v(N)=__ ,v(M)=__ 。
(3)反应达到平衡状态时,放出6QkJ的热量,当容器中充入1molN,反应放出的热量为__ 。
①等于QkJ ②小于QkJ ③大于QkJ ④等于2QkJ
(4)判断该反应达到平衡状态的依据是__ 。
①该条件下,正逆反应速率都为零
②该条件下,混合气体的密度不再发生变化
③该条件下,混合气体的压强不再发生变化
④该条件下,单位时间内消耗2molN的同时,生成1molM
(5)能加快反应速率的措施是___ 。
①升高温度②容器体积不变,充入惰性气体Ar③容器压强不变,充入惰性气体Ar④使用催化剂

(1)反应的化学方程式为
(2)反应达到最大限度的时间是
(3)反应达到平衡状态时,放出6QkJ的热量,当容器中充入1molN,反应放出的热量为
①等于QkJ ②小于QkJ ③大于QkJ ④等于2QkJ
(4)判断该反应达到平衡状态的依据是
①该条件下,正逆反应速率都为零
②该条件下,混合气体的密度不再发生变化
③该条件下,混合气体的压强不再发生变化
④该条件下,单位时间内消耗2molN的同时,生成1molM
(5)能加快反应速率的措施是
①升高温度②容器体积不变,充入惰性气体Ar③容器压强不变,充入惰性气体Ar④使用催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】通过实验测定反应速率的方法有多种,如:
①比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的_____ 来实现;
②在KMnO4与H2C2O4反应中,KMnO4与H2C2O4反应的离子方程式:_____ 。可通过测定_ 来测定该反应的速率;
③在Na2S2O3和H2SO4反应中,反应方程式为:_____ 该反应的速率可通过_____ 来测定。
①比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的
②在KMnO4与H2C2O4反应中,KMnO4与H2C2O4反应的离子方程式:
③在Na2S2O3和H2SO4反应中,反应方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学反应速率可通过实验测定。要测定不同反应时刻反应物或生成物的浓度,可通过观察和测量体系中的某一物质的相关性质,再进行适当的转换和计算。如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的________ 来实现;在KMnO4与H2C2O4反应中,可通过观察单位时间内________________ 变化来测定该反应的速率;在Na2S2O3+H2SO4→Na2SO4+S↓+SO2↑+H2O反应中,该反应的速率可通过______ 来测定。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2触摸试管情况 观察结果 反应完成所需的时间
粉末状 很烫 剧烈反应,带火星的木条复燃 3.5min
块状 微热 反应较慢,火星红亮但木条未复燃 30min
(1)写出上述实验中发生反应的化学方程式:_____ ;
(2)实验结果表明,催化剂的催化效果与_____ 有关;
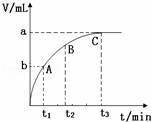
(3)某同学在10mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是_____ 。
MnO2触摸试管情况 观察结果 反应完成所需的时间
粉末状 很烫 剧烈反应,带火星的木条复燃 3.5min
块状 微热 反应较慢,火星红亮但木条未复燃 30min
(1)写出上述实验中发生反应的化学方程式:
(2)实验结果表明,催化剂的催化效果与
(3)某同学在10mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空或计算,(1)(2)小题为判断题。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。___________ (填“×”或“√”)
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。___________ (填“×”或“√”)
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性。
(4)Na与水反应,增大水的用量:反应速率___________ (选填“加快”、“减慢”、“不变”)。
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=___________ mol·L-1·min-1。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(4)Na与水反应,增大水的用量:反应速率
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在一定条件下,aA+bB cC的可逆反应达到平衡:
cC的可逆反应达到平衡:
(1)若A、B、C都是气体,缩小容器体积,则反应速率______________ (填“增大”或“减小”或“不变”)。
(2)若A、B、C都是气体,减小压强,平衡向逆反应方向移动,则a+b__________ c(填“>”或“=”或“<”)。
(3)若A为固体、B为无色气体、C为有色气体,再加入适量的A物质,则平衡__________ 移动(填“向左”或“向右”或“不”),气体的颜色_________ (填“加深”或“变浅”或“不变”)。
(4)若加热后C的质量分数减少,则正反应是__________ 反应(填“放热”或“吸热”)。
 cC的可逆反应达到平衡:
cC的可逆反应达到平衡:(1)若A、B、C都是气体,缩小容器体积,则反应速率
(2)若A、B、C都是气体,减小压强,平衡向逆反应方向移动,则a+b
(3)若A为固体、B为无色气体、C为有色气体,再加入适量的A物质,则平衡
(4)若加热后C的质量分数减少,则正反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】一定温度下,反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
(1)增加Fe的物质的量,其正反应速率__________ ,逆反应速率__________ 。
(2)将容器的体积缩小一半,其正反应速率________ ,逆反应速率_________ 。
(3)若保持体积不变,充入Ar,其逆反应速率________ ,逆反应速率_________ 。
(4)保持压强不变,充入Ar,其正反应速率__________ ,逆反应速率_________ 。
(5)使用催化剂,其正反应速率__________ ,逆反应速率_________ 。
 Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。(1)增加Fe的物质的量,其正反应速率
(2)将容器的体积缩小一半,其正反应速率
(3)若保持体积不变,充入Ar,其逆反应速率
(4)保持压强不变,充入Ar,其正反应速率
(5)使用催化剂,其正反应速率
您最近一年使用:0次



