一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:
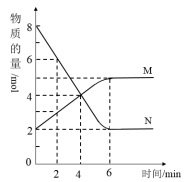
(1)反应的化学方程式为___ 。
(2)反应达到最大限度的时间是___ min,该时间内的平均反应速率v(N)=__ ,v(M)=__ 。
(3)反应达到平衡状态时,放出6QkJ的热量,当容器中充入1molN,反应放出的热量为__ 。
①等于QkJ ②小于QkJ ③大于QkJ ④等于2QkJ
(4)判断该反应达到平衡状态的依据是__ 。
①该条件下,正逆反应速率都为零
②该条件下,混合气体的密度不再发生变化
③该条件下,混合气体的压强不再发生变化
④该条件下,单位时间内消耗2molN的同时,生成1molM
(5)能加快反应速率的措施是___ 。
①升高温度②容器体积不变,充入惰性气体Ar③容器压强不变,充入惰性气体Ar④使用催化剂

(1)反应的化学方程式为
(2)反应达到最大限度的时间是
(3)反应达到平衡状态时,放出6QkJ的热量,当容器中充入1molN,反应放出的热量为
①等于QkJ ②小于QkJ ③大于QkJ ④等于2QkJ
(4)判断该反应达到平衡状态的依据是
①该条件下,正逆反应速率都为零
②该条件下,混合气体的密度不再发生变化
③该条件下,混合气体的压强不再发生变化
④该条件下,单位时间内消耗2molN的同时,生成1molM
(5)能加快反应速率的措施是
①升高温度②容器体积不变,充入惰性气体Ar③容器压强不变,充入惰性气体Ar④使用催化剂
20-21高二上·甘肃武威·阶段练习 查看更多[4]
甘肃省武威市民勤县第一中学2020-2021学年高二上学期12月月考化学试题(理科)(已下线)第08讲 化学平衡状态(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)作业(七) 化学平衡状态 化学平衡常数第二章 第二节 化学平衡 第1课时 可逆反应 化学平衡状态
更新时间:2020-12-28 10:20:30
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某温度时,在4L的容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
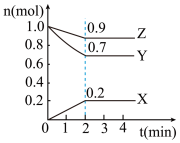
(1)由图中数据分析,该反应的化学方程式为:_______ ;
(2)反应从开始至2min内X的平均反应速率是:_______ 。

(1)由图中数据分析,该反应的化学方程式为:
(2)反应从开始至2min内X的平均反应速率是:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】研究碳、氮、硫及卤素等单质及其化合物在生产生活和环境保护中有着重要意义。
I.反应I2+2S2O =2I-+S4O
=2I-+S4O 常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1 mL淀粉溶液作指示剂,若不经计算,可直接通过褪色时间的长短来判断浓度与反应速率的关系,下列试剂中:①1 mL 0.001 mol·L-1的碘水;②1 mL 0.01 mol·L-1的碘水③3 mL 0.001 mol·L-1的Na2S2O3溶液;④3 mL 0.01 mol·L-1的Na2S2O3溶液。
常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1 mL淀粉溶液作指示剂,若不经计算,可直接通过褪色时间的长短来判断浓度与反应速率的关系,下列试剂中:①1 mL 0.001 mol·L-1的碘水;②1 mL 0.01 mol·L-1的碘水③3 mL 0.001 mol·L-1的Na2S2O3溶液;④3 mL 0.01 mol·L-1的Na2S2O3溶液。
(1)应选择___________ (填代号)。
(2)若某同学选取②④进行实验,测得褪色时间为4s,忽略混合后溶液体积的变化,试计算v(S2O )=
)=___________ 。
II.一定条件下,在水溶液中1 mol Cl-、ClO (x=1,2,3,4)的能量(kJ)相对大小如图所示。
(x=1,2,3,4)的能量(kJ)相对大小如图所示。
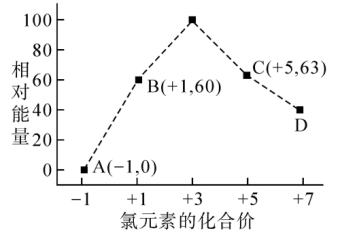
(3)D是___________ (填离子符号);
(4)B→A+C反应的离子方程式为:___________ ;当生成1 mol C时,___________ kJ的热量(填吸收或放出以及具体数值)。
III.工业上可以利用CO2和H2一定条件下合成甲醇,
(5)恒温恒容密闭容器中充入3 molH2和1 molCO2进行反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
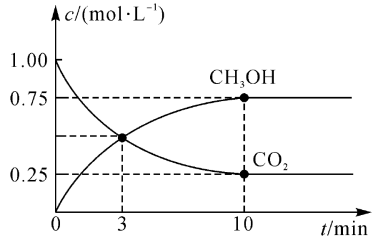
①从0min到3min,以H2的浓度变化表示的化学反应速率v(H2)=___________ 。
②下列表述不正确的是___________ (填字母)。
a.第3分钟时v正(CH3OH)小于第10分钟时v逆(CH3OH)
b.混合气体的平均相对分子质量不随时间的变化而变化,反应达到平衡状态
c.达到平衡时H2的转化率为75%
d.平衡混合气体中CO2(g)和H2(g)的质量之比是22:1
e.反应前的压强与平衡时的压强之比为8:5
(6)用CO2和H2合成甲醇时存在副反应,向某恒容容器中充入1mol CO2和3mol H2,发生如下反应:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g);②CO2(g)+H2(g)
CH3OH(g)+H2O(g);②CO2(g)+H2(g)  CO(g)+H2O(g);③CO(g)+2H2(g)
CO(g)+H2O(g);③CO(g)+2H2(g)  CH3OH(g)。平衡时测得n(CH3OH)=a mol,n(CO)=b mol,则n(H2)=
CH3OH(g)。平衡时测得n(CH3OH)=a mol,n(CO)=b mol,则n(H2)=___________ mol。
I.反应I2+2S2O
 =2I-+S4O
=2I-+S4O 常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1 mL淀粉溶液作指示剂,若不经计算,可直接通过褪色时间的长短来判断浓度与反应速率的关系,下列试剂中:①1 mL 0.001 mol·L-1的碘水;②1 mL 0.01 mol·L-1的碘水③3 mL 0.001 mol·L-1的Na2S2O3溶液;④3 mL 0.01 mol·L-1的Na2S2O3溶液。
常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1 mL淀粉溶液作指示剂,若不经计算,可直接通过褪色时间的长短来判断浓度与反应速率的关系,下列试剂中:①1 mL 0.001 mol·L-1的碘水;②1 mL 0.01 mol·L-1的碘水③3 mL 0.001 mol·L-1的Na2S2O3溶液;④3 mL 0.01 mol·L-1的Na2S2O3溶液。(1)应选择
(2)若某同学选取②④进行实验,测得褪色时间为4s,忽略混合后溶液体积的变化,试计算v(S2O
 )=
)=II.一定条件下,在水溶液中1 mol Cl-、ClO
 (x=1,2,3,4)的能量(kJ)相对大小如图所示。
(x=1,2,3,4)的能量(kJ)相对大小如图所示。
(3)D是
(4)B→A+C反应的离子方程式为:
III.工业上可以利用CO2和H2一定条件下合成甲醇,
(5)恒温恒容密闭容器中充入3 molH2和1 molCO2进行反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
①从0min到3min,以H2的浓度变化表示的化学反应速率v(H2)=
②下列表述不正确的是
a.第3分钟时v正(CH3OH)小于第10分钟时v逆(CH3OH)
b.混合气体的平均相对分子质量不随时间的变化而变化,反应达到平衡状态
c.达到平衡时H2的转化率为75%
d.平衡混合气体中CO2(g)和H2(g)的质量之比是22:1
e.反应前的压强与平衡时的压强之比为8:5
(6)用CO2和H2合成甲醇时存在副反应,向某恒容容器中充入1mol CO2和3mol H2,发生如下反应:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g);②CO2(g)+H2(g)
CH3OH(g)+H2O(g);②CO2(g)+H2(g)  CO(g)+H2O(g);③CO(g)+2H2(g)
CO(g)+H2O(g);③CO(g)+2H2(g)  CH3OH(g)。平衡时测得n(CH3OH)=a mol,n(CO)=b mol,则n(H2)=
CH3OH(g)。平衡时测得n(CH3OH)=a mol,n(CO)=b mol,则n(H2)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】完成有关化学反应速率的相关内容
(1)含义:描述___________ 的物理量。
(2)表示方法:
①对于反应体系体积不变的化学反应,可以用单位时间内___________ 的改变量(取绝对值)来表示该物质的化学反应速率。
②表达式:___________ 。
(3)常用单位:___________ 。
【情境问题思考】
(4)在密闭容器中,合成氨的反应,刚开始时氮气为8mol/L与氢气的浓度为20mol/L,5min后,测得容器内剩余的氮气的浓度为6mol/L。计算用N2、H2、NH3的浓度变化表示的反应速率分别为多少___________ ?
【思考】以上三者数值是否相等?是否矛盾?有何规律?
【结论】在同一个反应中,各物质的反应速率之比等于方程式中的化学计量数(系数)之比,即:v(N2):v(H2):v(NH3)=1:3:2
(1)含义:描述
(2)表示方法:
①对于反应体系体积不变的化学反应,可以用单位时间内
②表达式:
(3)常用单位:
【情境问题思考】
(4)在密闭容器中,合成氨的反应,刚开始时氮气为8mol/L与氢气的浓度为20mol/L,5min后,测得容器内剩余的氮气的浓度为6mol/L。计算用N2、H2、NH3的浓度变化表示的反应速率分别为多少
【思考】以上三者数值是否相等?是否矛盾?有何规律?
【结论】在同一个反应中,各物质的反应速率之比等于方程式中的化学计量数(系数)之比,即:v(N2):v(H2):v(NH3)=1:3:2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】吸入氧气、排出二氧化碳,这看似再简单不过的新陈代谢,在遥远的太空中却并不容易,因为在航天服、航天器、空间站等密闭系统中,CO2浓度会高得多,而超过一定浓度会导致呼吸急促、头晕头痛、昏迷甚至死亡,因此必须通过一定方法将CO2清除。
(1)非再生式氢氧化锂(LiOH)除碳技术
我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附CO2生成碳酸锂,该技术设备操作简单,功能可靠,适用于短期出舱任务。吸附发生的化学方程式为_______ 。
(2)再生式快速循环胺技术
以固态胺作为吸附剂,吸附CO2与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出CO2,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是_______ 变化(填“物理”或“化学”)
(3)萨巴蒂尔(Sabatier)除碳生氧技术
利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如图所示。
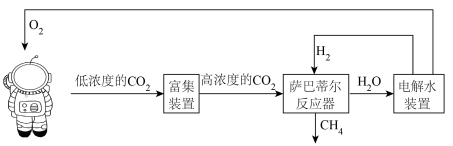
①下列说法错误的是_______ 。
A.CO2的最终产物为CH4和O2
B.电解水装置中,反应物的能量高于生成物的能量
C.萨巴蒂尔反应器中反应的氧化剂与还原剂物质的量之比为1∶4
D.物质转化中O、H原子的利用率均为100%
②CO2富集的原电池模拟装置如图:
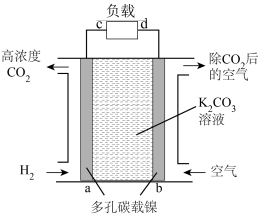
i.b极为_______ 极(填“正”或“负”),a电极上发生的电极反应_______ 。
ii.上述电极材料采用多孔碳载镍,“多孔”的优点是_______ 。
iii.该装置若消耗2 mol H2,则理论上在b极除去CO2的体积为_______ L(标况下)。
(1)非再生式氢氧化锂(LiOH)除碳技术
我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附CO2生成碳酸锂,该技术设备操作简单,功能可靠,适用于短期出舱任务。吸附发生的化学方程式为
(2)再生式快速循环胺技术
以固态胺作为吸附剂,吸附CO2与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,破坏碳酸氢盐的化学键,释放出CO2,从而完成吸附剂的再生。该技术大大提升了舱外航天服的续航时间。固态胺的吸附是
(3)萨巴蒂尔(Sabatier)除碳生氧技术
利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如图所示。

①下列说法错误的是
A.CO2的最终产物为CH4和O2
B.电解水装置中,反应物的能量高于生成物的能量
C.萨巴蒂尔反应器中反应的氧化剂与还原剂物质的量之比为1∶4
D.物质转化中O、H原子的利用率均为100%
②CO2富集的原电池模拟装置如图:

i.b极为
ii.上述电极材料采用多孔碳载镍,“多孔”的优点是
iii.该装置若消耗2 mol H2,则理论上在b极除去CO2的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1mol CO2、3mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
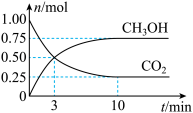
(1)在3min末,H2的浓度为_______ ,这时,反应速率 υ(正)_______ υ(逆)(选填>、<或 =)。
(2)从反应开始到平衡,平均反应速率υ(CO2)=_______ 。达到平衡时,H2的转化率为_______ 。
(3)下列措施不能提高反应速率的是_______。
(4)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:υ(H2)=0.3 mol∙L−1∙s−1;乙:υ(CO2)=0.12 mol∙L−1∙s−1;丙:υ(CH3OH)=4.8 mol∙L−1∙min−1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
(5)在一体积固定的密闭容器中投入一定量的CO2和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO2,同时生成1mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)在3min末,H2的浓度为
(2)从反应开始到平衡,平均反应速率υ(CO2)=
(3)下列措施不能提高反应速率的是_______。
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)在一体积固定的密闭容器中投入一定量的CO2和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO2,同时生成1mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
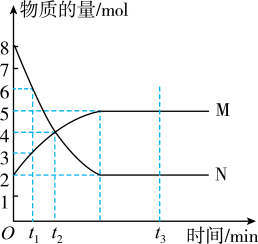
(1)此反应的化学方程式中a/b=___________ ;
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为_________________ ;
(3) N的平衡转化率为_______________ ;
(4)下列叙述中能说明上述反应达到平衡状态的是___________ (填字母)。
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:
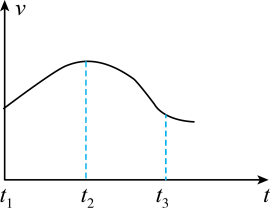
实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是_______ ,t2~t3速率变化的主要原因是______ 。
(2)实验②放出氢气的量减少的原因是___________________ (用离子方程式表示)。
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a或b作答。a.若不正确,请说明原因_____________________________________ 。b.若正确,则写出实验③中原电池的正极电极反应式_______________________ 。
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中a/b=
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3) N的平衡转化率为
(4)下列叙述中能说明上述反应达到平衡状态的是
a.反应中M与N的物质的量之比为1︰1
b.混合气体的总质量不随时间的变化而变化
c.混合气体的总物质的量不随时间的变化而变化
d.单位时间内每消耗a mol N,同时生成b mol M
e.混合气体的压强不随时间的变化而变化
f.N的质量分数在混合气体中保持不变
Ⅱ.研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:

实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是
(2)实验②放出氢气的量减少的原因是
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?请选择下列相应的a或b作答。a.若不正确,请说明原因
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:

(1)反应的化学方程式为___________ 。
(2)反应达到最大限度的时间是___________ min,该时间内的平均反应速率v(N)=___________ 。
(3)判断该反应达到平衡状态的依据是___________ (填序号)
①该条件下,正、逆反应速率都为零
②2V正(N)=V逆(M)
③该条件下,N的物质的量保持不变
(4)能加快反应速率的措施任写两条___________

(1)反应的化学方程式为
(2)反应达到最大限度的时间是
(3)判断该反应达到平衡状态的依据是
①该条件下,正、逆反应速率都为零
②2V正(N)=V逆(M)
③该条件下,N的物质的量保持不变
(4)能加快反应速率的措施任写两条
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】向恒压密闭容器中充入2 mol NO与1 mol O2,容器中的分子总数为2NA___
您最近一年使用:0次
【推荐3】I.将 、
、 和
和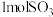 在恒温恒容的密闭容器中发生:
在恒温恒容的密闭容器中发生: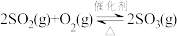 反应。
反应。
(1)下列说明反应达到平衡状态的是_______ (填序号)。
①气体密度不变;
②混合气体的总物质的量不变;
③混合气体的平均相对分子质量不变;
④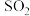 和
和 的物质的量之比不变;
的物质的量之比不变;
⑤消耗的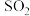 与消耗
与消耗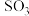 的速率相等;
的速率相等;
⑥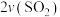 消耗=
消耗=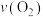 生成;
生成;
(2)达到平衡时,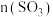 的取值范围
的取值范围_______ 。
II.碘及其化合物在生产生活中有重要作用。将0.4mol氢气和0.2mol碘蒸气放入2L密闭容器中进行反应: ,反应经过5min测得碘化氢的浓度为
,反应经过5min测得碘化氢的浓度为 ,碘蒸气的浓度为
,碘蒸气的浓度为
(3)前5min平均反应速率
_______ 。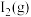 的转化率为
的转化率为_______ 。
(4)生成的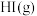 的体积分数为
的体积分数为_______ (保留三位有效数字)。
 、
、 和
和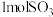 在恒温恒容的密闭容器中发生:
在恒温恒容的密闭容器中发生: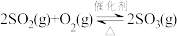 反应。
反应。(1)下列说明反应达到平衡状态的是
①气体密度不变;
②混合气体的总物质的量不变;
③混合气体的平均相对分子质量不变;
④
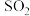 和
和 的物质的量之比不变;
的物质的量之比不变;⑤消耗的
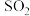 与消耗
与消耗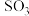 的速率相等;
的速率相等;⑥
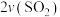 消耗=
消耗=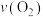 生成;
生成;(2)达到平衡时,
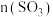 的取值范围
的取值范围II.碘及其化合物在生产生活中有重要作用。将0.4mol氢气和0.2mol碘蒸气放入2L密闭容器中进行反应:
 ,反应经过5min测得碘化氢的浓度为
,反应经过5min测得碘化氢的浓度为 ,碘蒸气的浓度为
,碘蒸气的浓度为
(3)前5min平均反应速率

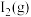 的转化率为
的转化率为(4)生成的
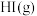 的体积分数为
的体积分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】向一个容积为2 L的密闭容器中充入2mol NH3和3 mol O2,在恒温和催化剂作用下发生反应:4NH3(g)+5O2(g)⇌4NO(g) + 6H2O(l),经过5 min后达到平衡状态。此时,c(NH3):c(O2)=4:7。则:
(1)反应开始至平衡时,以NO的浓度变化表示该反应的平均速率v(NO)=__________ 。
(2)起始状态与平衡状态容器内的压强之比为______ 。
(3)该条件下反应一段时间,下列能说明反应达到平衡状态的是___________ 。
a.c(H2O)保持不变的状态
b.气体的压强保持不变的状态
c.4v正(NH3)=5v逆(O2)
d.NH3与O2浓度之比保持不变的状态
(1)反应开始至平衡时,以NO的浓度变化表示该反应的平均速率v(NO)=
(2)起始状态与平衡状态容器内的压强之比为
(3)该条件下反应一段时间,下列能说明反应达到平衡状态的是
a.c(H2O)保持不变的状态
b.气体的压强保持不变的状态
c.4v正(NH3)=5v逆(O2)
d.NH3与O2浓度之比保持不变的状态
您最近一年使用:0次
【推荐2】乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)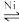 C2H6(g),容器内气体的压强与反应时间的关系如下图:
C2H6(g),容器内气体的压强与反应时间的关系如下图:
(1)有机物C2H6的名称是___________ 。该有机物属于___________ (填序号)。
A.烯烃 B.芳香烃 C.环状饱和烃 D.链状饱和烃(烷烃)
(2)该反应的类型属于___________(填序号)。
(3)达到化学平衡状态时,下列数值与开始时相同的是___________(填序号)
(4)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=___________ 。
在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)
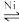 C2H6(g),容器内气体的压强与反应时间的关系如下图:
C2H6(g),容器内气体的压强与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 乙烯的物质的量(mol) | 1.00 | 0.80 | 0.70 | 0.64 | 0.60 | 0.60 |
A.烯烃 B.芳香烃 C.环状饱和烃 D.链状饱和烃(烷烃)
(2)该反应的类型属于___________(填序号)。
| A.取代反应 | B.加成反应 | C.加成聚合反应 | D.聚合反应 |
| A.容器内气体的压强 | B.容器内n(H2) | C.容器内c(CH2=CH2) | D.容器内气体的总质量 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)某温度下在容积为2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
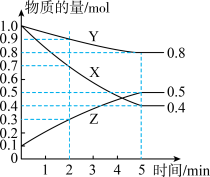
①该反应的化学方程式是_______ 。
②4min时,υ正_______ υ逆(填“>”“<”或“=")。
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经相同时间后,测得三个容器中的反应速率分别为甲:υ(X)=0.3mol·L-1·s-1,乙:υ(Y)=0.12mol·L-1·s-1,丙:υ(Z)=9.6mol·L-1·min-1.则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
④下列措施能增大该反应速率的是_______ (选填字母)
A.升高温度 B.恒容条件下充入Ar气
C.减小Z的浓度 D.将反应容器体积缩小
(2)反应2NO(g)+O2(g)⇌2NO2(g),在一定温度下 密闭容器内,能说明该反应已经达到化学平衡状态的是
密闭容器内,能说明该反应已经达到化学平衡状态的是_______ 。
a.2υ逆(NO)=υ正(O2)
b.容器内压强保持不变
c.υ(NO2)=2υ(O2)
d.容器内的密度保持不变
e.容器内混合气体平均相对分子质量不变
f.c(NO):c(O2):c(NO2)=2:1:2
g.容器内气体颜色不变
(3)常见的烟道气中除去SO2的方法之一:2CO(g)+SO2(g)⇌2CO2(g)+S(l) (ΔH<0),该反应的平衡常数表达式为_______ 。若在2L的密闭容器中进行上述反应,经测定在5min内气体的质量减少了1.6g,则0~5min的平均反应速率υ(SO2)=_______ 。
(1)某温度下在容积为2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②4min时,υ正
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经相同时间后,测得三个容器中的反应速率分别为甲:υ(X)=0.3mol·L-1·s-1,乙:υ(Y)=0.12mol·L-1·s-1,丙:υ(Z)=9.6mol·L-1·min-1.则甲、乙、丙三个容器中反应速率由快到慢的顺序为
④下列措施能增大该反应速率的是
A.升高温度 B.恒容条件下充入Ar气
C.减小Z的浓度 D.将反应容器体积缩小
(2)反应2NO(g)+O2(g)⇌2NO2(g),在一定温度下
 密闭容器内,能说明该反应已经达到化学平衡状态的是
密闭容器内,能说明该反应已经达到化学平衡状态的是a.2υ逆(NO)=υ正(O2)
b.容器内压强保持不变
c.υ(NO2)=2υ(O2)
d.容器内的密度保持不变
e.容器内混合气体平均相对分子质量不变
f.c(NO):c(O2):c(NO2)=2:1:2
g.容器内气体颜色不变
(3)常见的烟道气中除去SO2的方法之一:2CO(g)+SO2(g)⇌2CO2(g)+S(l) (ΔH<0),该反应的平衡常数表达式为
您最近一年使用:0次



