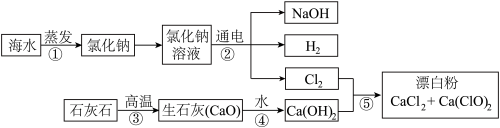
工业制取皮革加工中的鞣化剂硝酸铝,是用铝灰与烧碱、硝酸反应制得的。铝灰是铝、氧化铝和氧化铁的混合物。产品硝酸铝晶体为Al(NO3)3·nH2O。
已知偏铝酸盐能与一般的酸反应,如:NaAlO2+HNO3+H2O→NaNO3+Al(OH)3↓
生产流程如图:
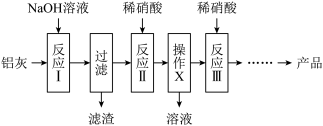
完成下列填空:
(1)用氢氧化钠固体配制30%的氢氧化钠溶液,除烧杯、玻璃棒外还需(选填编号)___ 。
A. B.
B.  C.
C. 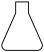 D.
D. 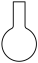
说出流程中产生的滤渣的一种用途是___ 。制作一个过滤器需要___ 。流程中操作x的名称是____ 。
(2)反应Ⅱ加入的硝酸必须适量,原因是___ 。反应Ⅲ加入的硝酸要稍过量,原因是___ 。
(3)从反应Ⅲ所得的溶液制成产品的步骤依次为减压蒸发,___ ,过滤,___ ,低温烘干。
(4)为测定所得的产品的纯度,质检人员称取产品Wg,溶于水配成500mL溶液,从中取出25.00mL,加入过量已知浓度的氨水充分反应后,剩余的氨水用已知浓度的盐酸溶液进行测定。通过计算便可得出产品的纯度。
①上述过程属于定量实验。其中除配制一定物质的量浓度的溶液外,还有一个是___ ,该实验过程中要进行多次读数,读数的方法是读出与___ 的刻度值。
②任意写出一个该测定过程中所涉及的化学反应的离子方程式:___ 。
已知偏铝酸盐能与一般的酸反应,如:NaAlO2+HNO3+H2O→NaNO3+Al(OH)3↓
生产流程如图:

完成下列填空:
(1)用氢氧化钠固体配制30%的氢氧化钠溶液,除烧杯、玻璃棒外还需(选填编号)
A.
 B.
B.  C.
C.  D.
D. 
说出流程中产生的滤渣的一种用途是
(2)反应Ⅱ加入的硝酸必须适量,原因是
(3)从反应Ⅲ所得的溶液制成产品的步骤依次为减压蒸发,
(4)为测定所得的产品的纯度,质检人员称取产品Wg,溶于水配成500mL溶液,从中取出25.00mL,加入过量已知浓度的氨水充分反应后,剩余的氨水用已知浓度的盐酸溶液进行测定。通过计算便可得出产品的纯度。
①上述过程属于定量实验。其中除配制一定物质的量浓度的溶液外,还有一个是
②任意写出一个该测定过程中所涉及的化学反应的离子方程式:
更新时间:2020/05/17 13:54:17
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】Pd/Al2O3是常见的催化剂。一种废Pd/Al2O3纳米催化剂的主要成分及含量为:Al2O3(92.8%),SiO2(5.0%),Pd(0.3%),Pt和炭(共约1.0%)。采用如图工艺从废催化剂中提取金属Pd并制备明矾。
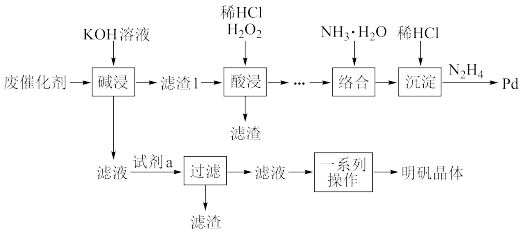
回答下列问题:
(1)为提高“碱浸”效率,可采取的措施有____ (任写两条)。
(2)试剂a的化学式为____ 。
(3)“一系列操作”是指____ 、过滤、洗涤。
(4)“酸浸”时,Pt和Pd分别转化为PtCl 和PdCl
和PdCl ,写出Pd转化为PtCl
,写出Pd转化为PtCl 的离子方程式:
的离子方程式:____ 。
(5)“酸浸”时,若用O3替代H2O2,则氧化效率(单位质量的物质得到的电子数)将____ (填“提高”“降低”或“不变”)。
(6)“络合”过程后得到Pd(NH3) 和Pt(NH3)
和Pt(NH3) ,“沉淀”时,搅拌滴加盐酸调节pH将[Pd(NH3)4]Cl2转化为[Pd(NH3)2]Cl2沉淀,结合平衡移动原理解释实现转化的原因是
,“沉淀”时,搅拌滴加盐酸调节pH将[Pd(NH3)4]Cl2转化为[Pd(NH3)2]Cl2沉淀,结合平衡移动原理解释实现转化的原因是____ 。
(7)采用工艺:“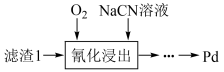 ”也能得到金属Pd,试从绿色化学角度分析该工艺的不足
”也能得到金属Pd,试从绿色化学角度分析该工艺的不足____ 。

回答下列问题:
(1)为提高“碱浸”效率,可采取的措施有
(2)试剂a的化学式为
(3)“一系列操作”是指
(4)“酸浸”时,Pt和Pd分别转化为PtCl
 和PdCl
和PdCl ,写出Pd转化为PtCl
,写出Pd转化为PtCl 的离子方程式:
的离子方程式:(5)“酸浸”时,若用O3替代H2O2,则氧化效率(单位质量的物质得到的电子数)将
(6)“络合”过程后得到Pd(NH3)
 和Pt(NH3)
和Pt(NH3) ,“沉淀”时,搅拌滴加盐酸调节pH将[Pd(NH3)4]Cl2转化为[Pd(NH3)2]Cl2沉淀,结合平衡移动原理解释实现转化的原因是
,“沉淀”时,搅拌滴加盐酸调节pH将[Pd(NH3)4]Cl2转化为[Pd(NH3)2]Cl2沉淀,结合平衡移动原理解释实现转化的原因是(7)采用工艺:“
 ”也能得到金属Pd,试从绿色化学角度分析该工艺的不足
”也能得到金属Pd,试从绿色化学角度分析该工艺的不足
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】磷酸铝(AlPO4)是一种用途广泛的材料,在建筑、耐火材料、化工等方面具有广泛的应用前景。以磷硅渣(主要成分为Ca3(PO4)2、Al2O3、SiO2和V2O5等)为原料制备磷酸铝的工艺流程如图所示:
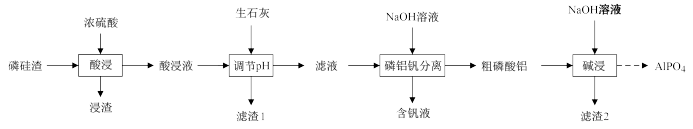
回答下列问题:
(1)酸浸液中含磷元素的主要粒子是_____ (填化学式,下同),浸渣中的主要化学成分是_____ 。
(2)生石灰除了调节pH外,另一作用是_____ 。
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为_____ 。
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是_____ (填化学式)。
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量的影响如图所示:
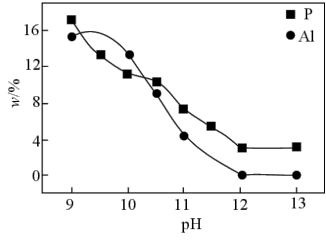
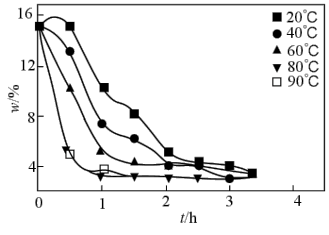
则最优反应条件是_____ 。
(6)固相反应制备磷酸铝的方法之一是在900℃的焙烧炉内加热磷酸二氢铵与氧化铝混合物,写出该反应的化学方程式:_____ 。

回答下列问题:
(1)酸浸液中含磷元素的主要粒子是
(2)生石灰除了调节pH外,另一作用是
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量的影响如图所示:


则最优反应条件是
(6)固相反应制备磷酸铝的方法之一是在900℃的焙烧炉内加热磷酸二氢铵与氧化铝混合物,写出该反应的化学方程式:
您最近一年使用:0次
【推荐3】用方铅矿精矿( 主要为PbS)和软锰矿(主要为MnO2,还有少量Fe2O3,Al2O3等杂质) 制备PbSO4和Mn3O4的工艺流程如下:
②25℃ 时,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.8×10-8
③PbCl2 (s)+2Cl-(aq)
 (aq) △H>0
(aq) △H>0
(1)80℃用盐酸处理两种矿石,为加快酸浸速率,还可采用的方法是_______________ (任写一种)。
(2)向酸浸液中加入饱和食盐水的目的是_______________ ;加入物质X可用于调节酸浸液的pH值,物质X可以是_______________ (填字母)。
A.MnCO3 B.NaOH C.ZnO D.PbO
(3)滤渣中含有两种金属杂质形成的化合物,其成分为_____________ (写化学式);
请设计分离两种金属化合物的路线图(用化学式表示物质,用箭头表示转化关系,箭头上注明试剂和分离方法)。______________________________________
(4)向滤液2中通入NH3和O2发生反应,写出总反应的离子方程式。___________________________________
(5)用Mn3O4为原料可以获得金属锰,选择合适的冶炼方法为___________ (填字母)。
(6)求25℃氯化铅沉淀转化为硫酸铅沉淀反应的平衡常数K=___________ (保留到整数位)。

②25℃ 时,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.8×10-8
③PbCl2 (s)+2Cl-(aq)

 (aq) △H>0
(aq) △H>0(1)80℃用盐酸处理两种矿石,为加快酸浸速率,还可采用的方法是
(2)向酸浸液中加入饱和食盐水的目的是
A.MnCO3 B.NaOH C.ZnO D.PbO
(3)滤渣中含有两种金属杂质形成的化合物,其成分为
请设计分离两种金属化合物的路线图(用化学式表示物质,用箭头表示转化关系,箭头上注明试剂和分离方法)。
(4)向滤液2中通入NH3和O2发生反应,写出总反应的离子方程式。
(5)用Mn3O4为原料可以获得金属锰,选择合适的冶炼方法为___________ (填字母)。
| A.热还原法 | B.电解法 | C.热分解法 |
(6)求25℃氯化铅沉淀转化为硫酸铅沉淀反应的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】欲提纯混有硫酸钠、碳酸氢铵的氯化钠固体,某学生设计了如下方案:
(已知碳酸氢铵受热分解后无固体剩余)
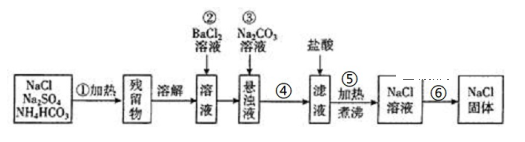
请根据操作流程回答下列问题:
(1)操作①在加热时应选择用_____________ 来盛装混合物(填仪器名称)。
(2)操作②发生的化学反应方程式为:___________________________________________ ;
判断SO42-已沉淀完全的方法是______________________________________________ 。
(3)操作③的目的是___________________________________ 。
(4)操作④和操作⑥的分离提纯方法的名称分别是____________ 、_____________ 。
(已知碳酸氢铵受热分解后无固体剩余)

请根据操作流程回答下列问题:
(1)操作①在加热时应选择用
(2)操作②发生的化学反应方程式为:
判断SO42-已沉淀完全的方法是
(3)操作③的目的是
(4)操作④和操作⑥的分离提纯方法的名称分别是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碳酸锰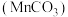 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量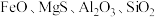 等)制备高纯
等)制备高纯 的流程如下:
的流程如下: 如下表:
如下表:
②室温下, 。回答下列问题:
。回答下列问题:
(1)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是___________ (任写一种),“尾气”中含有由“煅烧”生成的有害气体的化学式为___________ 。
(2)加入 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(3)加入氨水调节溶液 为5.0,则溶液中
为5.0,则溶液中
___________ (填“>”“<”或“=”)c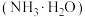 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为___________ (填离子符号,金属离子浓度 时,视为沉淀完全)。
时,视为沉淀完全)。
(4)室温下“沉镁”时,离子反应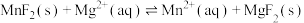 的化学平衡常数
的化学平衡常数
___________ 。
(5)加入 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为___________ 。
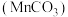 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量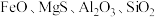 等)制备高纯
等)制备高纯 的流程如下:
的流程如下:
 如下表:
如下表:| 物质 |  |  |  |  |  |
 | 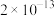 | 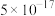 | 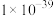 | 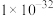 | 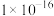 |
 。回答下列问题:
。回答下列问题:(1)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是
(2)加入
 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)加入氨水调节溶液
 为5.0,则溶液中
为5.0,则溶液中
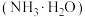 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为 时,视为沉淀完全)。
时,视为沉淀完全)。(4)室温下“沉镁”时,离子反应
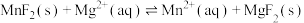 的化学平衡常数
的化学平衡常数
(5)加入
 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为
您最近一年使用:0次