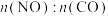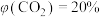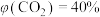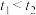以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制比的过程如图所示。下列叙述正确的是( )
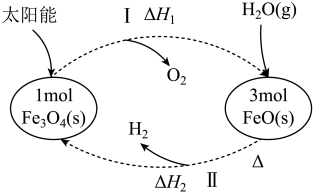

| A.H2的标准燃烧热△H<-(△H1+△H2) |
| B.过程I适当降低反应体系温度,反应更有利 |
| C.过程II中3molFeO(s)的总能量高于lmolFe3O4(s) |
| D.增加铁氧化合物的质量可以显著提高循环制H2的速率 |
更新时间:2020-05-23 12:23:02
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知CaSO4·2H2O脱水过程的热化学方程式如下:
CaSO4·2H2O(s)=CaSO4.1/2H2O (s)+3/2H2O (g) =83.2kJ/mol
=83.2kJ/mol
CaSO4.1/2H2O (s)=CaSO4(s)+1/2H2O (g)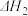
又知:CaSO4·2H2O(s)=CaSO4(s)+2H2O (l)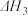 =26kJ/mol
=26kJ/mol
H2O (g)=H2O (l) =-44kJ/mol
=-44kJ/mol
则: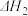 为
为
CaSO4·2H2O(s)=CaSO4.1/2H2O (s)+3/2H2O (g)
 =83.2kJ/mol
=83.2kJ/molCaSO4.1/2H2O (s)=CaSO4(s)+1/2H2O (g)
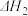
又知:CaSO4·2H2O(s)=CaSO4(s)+2H2O (l)
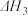 =26kJ/mol
=26kJ/molH2O (g)=H2O (l)
 =-44kJ/mol
=-44kJ/mol则:
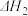 为
为| A.30.8kJ/mol | B.-30.8kJ/mol | C.61.6kJ/mol | D.-61.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】近日,陕西师范大学联合韩国梨花女子大学成功捕获并表征到水氧化催化过程中的锰端基氧和锰过氧化物中间体,明确了水氧化过程中水亲核进攻锰端基氧的氧氧成键机理,如图所示。下列说法正确的是
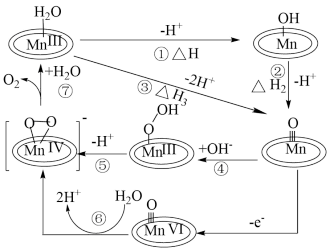

A. |
B.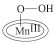 中O的化合价为-2 中O的化合价为-2 |
| C.催化过程中有极性键断裂和非极性键形成 |
D.过程⑦可表示为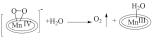 |
您最近一年使用:0次
【推荐1】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 有白色沉淀生成,溶液红色变浅 | 证明纯碱溶液呈碱性是由 水解引起的 水解引起的 |
| B | 室温下,用pH试纸测定浓度均为0.1mol/L的NaClO溶液、CH3COONa溶液pH | NaClO溶液的pH较大 | 酸性:HClO<CH3COOH |
| C | 向1mL 0.1mol/LNaOH溶液中滴入2滴0.1mol/L MgCl2溶液,再滴入2滴0.1mol/L CuSO4溶液 | 沉淀颜色变化:白色—蓝色 | Ksp:Cu(OH)2<Mg(OH)2 |
| D | 分别向两支试管中加入同浓度、同体积的草酸溶液,再分别加入同体积、不同浓度的酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色时间不同 | 浓度不同反应速率不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外兴趣小组利用硫代硫酸钠(Na2S2O3)与稀硫酸反应探究影响化学反应速率的因素[反应方程式为Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O],设计了如表系列实验。下列说法不正确的是
| 实验序号 | 反应温度(℃) | Na2S2O3浓度 | 稀硫酸 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| 1 | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| 2 | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| 3 | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
| A.设计该实验的基本原理为控制变量法 |
| B.实验1和2可探究温度对反应速率的影响 |
| C.若用实验1和3探究稀硫酸浓度对该反应速率的影响,则需V4=10,V5=0 |
| D.将水更换为Na2SO4溶液,对实验结果无影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学与生活息息相关,下列有关说法正确的是
| A.夏天冰箱保鲜食品的原理是降低温度,减小化学反应速率 |
| B.用钠粒可以区别醋酸和酒精,产生气泡的是醋酸 |
| C.氢氧燃料电池、锂电池、硅太阳能电池、铅蓄电池中都利用了原电池原理 |
| D.采用雾化技术燃煤的目的是提高煤燃烧效率和减少SO2排放 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】完成下列实验目的对应的实验操作不正确的是
| 实验目的 | 实验操作 | |
| A | 验证化学反应中的能量变化 | 将NO2球浸泡在冰水、热水中观察颜色变化 |
| B | 探究相同条件下,溶液温度对反应速率的影响 | 在两支试管中各加入5mL0.1mol/L的Na2S2O3和5mL0.1mol/L的H2SO4溶液,再分别放入冷水、热水中,记录出现浑浊所需时间 |
| C | 探究相同条件下,溶液浓度对反应速率的影响 | 在两支试管中各加入4mL0.01mol/L的KMnO4酸性溶液,再分别加入0.1mol/LH2C2O4溶液2mL、0.2mol/LH2C2O4溶液2mL,分别记录溶液褪色所需时间 |
| D | 探究相同条件下,溶液浓度对化学平衡移动的影响 | 在两支试管中各加入5mL0.1mol/L的K2Cr2O7溶液,再分别加入3~10滴浓硫酸和10~20滴6mol/L的NaOH溶液(忽略溶液体积的变化),观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

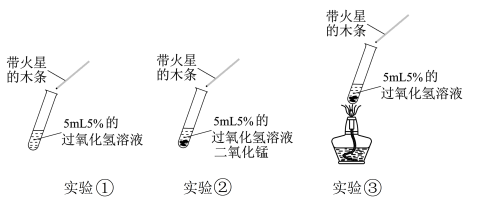

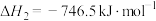 。在不同温度和压强下,分别在两密闭容器中发生上述反应,已知
。在不同温度和压强下,分别在两密闭容器中发生上述反应,已知 。下列说法错误的是
。下列说法错误的是