在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表
2NO2(g)体系中,n(NO)随时间的变化如表
(1)下图表示NO2的变化的曲线是________ 。用O2表示从0~2 s内该反应的平均速率v=________ 。
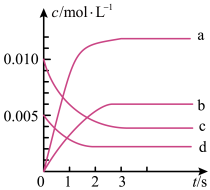
(2)能说明该反应已达到平衡状态的是________ (填字母,下同)。
a. v(NO2)、v(O2)、v(NO)相等
b. 容器内各物质浓度保持不变
c. 该反应v逆=v正
d. 容器内总质量保持不变
(3)为使该反应的反应速率增大,下列措施正确的是________ 。
a 及时分离出NO2气体 b 适当升高温度
c 增大O2的浓度 d 选择高效催化剂
 2NO2(g)体系中,n(NO)随时间的变化如表
2NO2(g)体系中,n(NO)随时间的变化如表| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下图表示NO2的变化的曲线是

(2)能说明该反应已达到平衡状态的是
a. v(NO2)、v(O2)、v(NO)相等
b. 容器内各物质浓度保持不变
c. 该反应v逆=v正
d. 容器内总质量保持不变
(3)为使该反应的反应速率增大,下列措施正确的是
a 及时分离出NO2气体 b 适当升高温度
c 增大O2的浓度 d 选择高效催化剂
19-20高一下·青海海东·期中 查看更多[2]
更新时间:2020-06-06 08:44:21
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】某温度时,在2 L恒容密闭容器中充入0.9 mol A(g)、0.6 mol B(g)、0.3 mol C(g),发生反应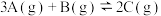 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题:___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(2)0~5 min内,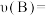
___________ mol∙L−1∙min−1。
(3)反应达到平衡时,
___________ mol∙L−1。
(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率___________ ;
②充入少量不参加反应的稀有气体,化学反应速率___________ ;
③将容器的体积压缩至原来的一半,化学反应速率___________ 。
(5) min时,反应
min时,反应___________ (填“达到”或“没有达到”)化学平衡;5 min时,υ(正)___________ (填“>”、“<”或“=”) υ(逆)。
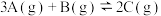 ,各物质物质的量的变化关系如图所示,回答下列问题:
,各物质物质的量的变化关系如图所示,回答下列问题: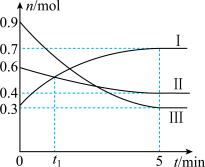
(2)0~5 min内,
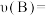
(3)反应达到平衡时,

(4)若仅改变下列一个条件,推测该反应的速率发生的变化 (填“增大”、“减小”或“不变”):
①降低温度,化学反应速率
②充入少量不参加反应的稀有气体,化学反应速率
③将容器的体积压缩至原来的一半,化学反应速率
(5)
 min时,反应
min时,反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某温度时,在2L容器中X、Y、Z三种物质随时间的变化曲线如下图所示,由图中的数据分析,第___ min开始,反应达到最大限度。该反应的化学方程式为____ ,反应开始至2min时为Z的平均反应速率__ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化石燃料燃烧过程中形成 和
和 等污染物,去除污染物的一种方法是在催化剂作用下发生反应:
等污染物,去除污染物的一种方法是在催化剂作用下发生反应: 。某温度下,在容积
。某温度下,在容积 的密闭容器中通入
的密闭容器中通入 和
和 ,测得不同时间
,测得不同时间 的物质的量如下表:
的物质的量如下表:
(1)用 的浓度变化表示
的浓度变化表示 的平均反应速率为
的平均反应速率为_______ 。若要加快反应速率,可以采取的措施有_______ (任写一条)。
(2)下列叙述能说明该反应已经达到平衡状态的是_______。
 和
和 等污染物,去除污染物的一种方法是在催化剂作用下发生反应:
等污染物,去除污染物的一种方法是在催化剂作用下发生反应: 。某温度下,在容积
。某温度下,在容积 的密闭容器中通入
的密闭容器中通入 和
和 ,测得不同时间
,测得不同时间 的物质的量如下表:
的物质的量如下表:时间 | 0 | 1 | 2 | 3 | …… |
 |  |  |  |  | …… |
 的浓度变化表示
的浓度变化表示 的平均反应速率为
的平均反应速率为(2)下列叙述能说明该反应已经达到平衡状态的是_______。
A. 的体积分数不再变化 的体积分数不再变化 | B. 的物质的量不再变化 的物质的量不再变化 |
| C.混合气体的密度不再变化 | D. 和 和 的浓度比保持不变 的浓度比保持不变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为_______ 。
②下列措施能提高NO和NO2去除率的有_______ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
③若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是_______ (填化学式);排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂V2O5作用下的脱硝反应机理如图所示。
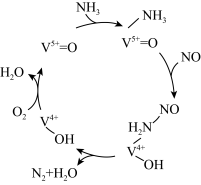
①根据如图机理,等物质的量的NO、NH3在有氧条件下的总化学方程式是_______ 。
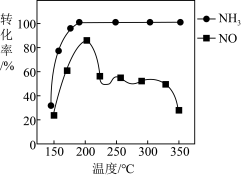
②按上述图中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是_______ 。
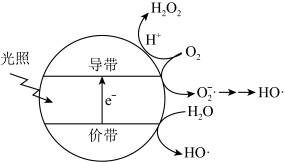
③羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上H2O直接转化为HO·;描述产生HO·的另一种过程:_______ 。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为
②下列措施能提高NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
③若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂V2O5作用下的脱硝反应机理如图所示。

①根据如图机理,等物质的量的NO、NH3在有氧条件下的总化学方程式是
②按上述图中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是

③羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上H2O直接转化为HO·;描述产生HO·的另一种过程:

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】研究CO2、CO的转化、应用等问题,既有利于环境保护,又有利于实现碳达峰、碳中和。中科院大连化学物理研究所设计了一种新型多功能复合催化剂,成功地实现了CO2直接加氢制取高辛烷值汽油:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g)
C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是_____ (写两种)。

 C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g)
C5H12(l)+10H2O(l) △H<0,该研究成果被评价为“CO2催化转化领域的突破性进展”。向某密闭容器中按一定投料比充入CO2、H2,控制条件使其发生反应:5CO2(g)+16H2(g) C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
C5H12(l)+10H2O(l) △H<0。测得H2的平衡转化率与温度、压强之间的关系如图所示。欲提高H2的平衡转化率并提高单位时间内C5H12(l)的产量,可采取的措施是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】一定温度下,在体积为2L的密闭容器中,充入1mol 和3mol
和3mol 发生如下反应:
发生如下反应: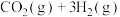
 。经测得
。经测得 和
和 (g)的物质的量随时间变化如图所示。
(g)的物质的量随时间变化如图所示。
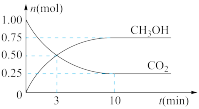
①从反应开始到平衡, 的平均反应速率
的平均反应速率
__ 。
②达到平衡时, 的转化率为
的转化率为__ 。(用百分数表示)
③下列措施不能提高反应速率的是____ 。
A.升高温度 B.加入适当催化剂
C.缩小体积,增大压强 D.恒温、恒压下通入氦气
④下列叙述中不能说明上述反应达到平衡状态的是___ 。
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C. 在混合气体中的质量分数保持不变
在混合气体中的质量分数保持不变
D.反应中 与
与 的物质的量之比为1∶1
的物质的量之比为1∶1
E.单位时间内每消耗1mol 同时生成1mol
同时生成1mol
 和3mol
和3mol 发生如下反应:
发生如下反应: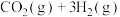
 。经测得
。经测得 和
和 (g)的物质的量随时间变化如图所示。
(g)的物质的量随时间变化如图所示。
①从反应开始到平衡,
 的平均反应速率
的平均反应速率
②达到平衡时,
 的转化率为
的转化率为③下列措施不能提高反应速率的是
A.升高温度 B.加入适当催化剂
C.缩小体积,增大压强 D.恒温、恒压下通入氦气
④下列叙述中不能说明上述反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C.
 在混合气体中的质量分数保持不变
在混合气体中的质量分数保持不变D.反应中
 与
与 的物质的量之比为1∶1
的物质的量之比为1∶1E.单位时间内每消耗1mol
 同时生成1mol
同时生成1mol
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g) COS(g)+H2(g)+Q。
COS(g)+H2(g)+Q。
完成下列填空:
(1)写出H2S的结构式___ ,它的电离方程式为____ 。
(2)若反应容器的体积为2L,反应前将10mol的CO与一定量的H2S混合加热,20秒后,达到平衡,CO变为8mol,以H2S表示速率,则v(H2S)=___ mol/(L•s)。
(3)写出一个能表示该反应达到平衡的标志:___ 。
(4)写出一个既能增大H2S转化率,又能加快反应速率的措施:___ 。
(5)该反应在一定条件下的反应速率(v)与时间(t)的关系如图所示,若反应达到平衡时(t1时),升高温度,v正、v逆如何变化,分别用v′正、v′逆表示画在如图___ 。
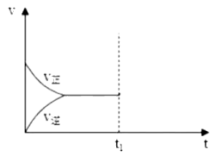
 COS(g)+H2(g)+Q。
COS(g)+H2(g)+Q。完成下列填空:
(1)写出H2S的结构式
(2)若反应容器的体积为2L,反应前将10mol的CO与一定量的H2S混合加热,20秒后,达到平衡,CO变为8mol,以H2S表示速率,则v(H2S)=
(3)写出一个能表示该反应达到平衡的标志:
(4)写出一个既能增大H2S转化率,又能加快反应速率的措施:
(5)该反应在一定条件下的反应速率(v)与时间(t)的关系如图所示,若反应达到平衡时(t1时),升高温度,v正、v逆如何变化,分别用v′正、v′逆表示画在如图

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)。污染跟冬季燃煤密切相关,SO2.CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式_________________ 。
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g) CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
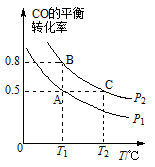
①下列说法不能判断该反应达到化学平衡状态的是____ (填字母)。
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA____ PB(填“>”“<”或“=”)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=________ L。
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图: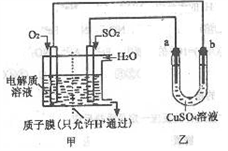
①该电池的负极反应:___________________ ;
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重____ g。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g)
 CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①下列说法不能判断该反应达到化学平衡状态的是
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据要求,回答下列问题:
I.一定温度下,在容积为2L的恒容密闭容器中进行反应:aM(g)⇌bN(g),M、N的物质的量随时间的变化曲线如下图所示:

(1)此反应的化学方程式中,已知化学计量数之比为最简整数比,则b=________ 。
(2)若t2—t1=10min,则从t1到t2时刻,平均反应速率v(N)=________ 。
(3)t1、t2、t3三个时刻中,______ 时刻达到反应的最大限度。
II.一种新型催化剂用于NO和CO的反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
(1)表中,a=______ ,b=______ 。
(2)能验证温度对化学反应速率的影响规律的实验是________ (填实验序号)。
(3)实验I和实验II中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的曲线是___________ (填“甲”或“乙”)。

(4)若在容积固定的绝热容器中发生反应2NO+2CO⇌2CO2+N2,则不能说明该反应已达到平衡状态的是_________ (填标号)。
A.容器内混合气体温度不再变化B.容器内的气体压强保持不变C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
I.一定温度下,在容积为2L的恒容密闭容器中进行反应:aM(g)⇌bN(g),M、N的物质的量随时间的变化曲线如下图所示:

(1)此反应的化学方程式中,已知化学计量数之比为最简整数比,则b=
(2)若t2—t1=10min,则从t1到t2时刻,平均反应速率v(N)=
(3)t1、t2、t3三个时刻中,
II.一种新型催化剂用于NO和CO的反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
| 实验序号 | t(℃) | NO初始浓度(mol•L-1) | CO初始浓度 (mol•L-1) | 催化剂的比表面积 (m2•g-1) |
I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
II | 280 | 1.20×10-3 | b | 124 |
III | 350 | a | 5.80×10-3 | 82 |
(1)表中,a=
(2)能验证温度对化学反应速率的影响规律的实验是
(3)实验I和实验II中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的曲线是

(4)若在容积固定的绝热容器中发生反应2NO+2CO⇌2CO2+N2,则不能说明该反应已达到平衡状态的是
A.容器内混合气体温度不再变化B.容器内的气体压强保持不变C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在1L密闭容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2(g)+H2(g) CO(g)+H2O(g),回答下列问题:
CO(g)+H2O(g),回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。求该条件下的化学平衡常数K1=_______ 。(写出该反应的化学平衡常数的表达式并计算出结果)
(2)在(1)的基础上,把体系温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知该反应的正反应为_______ 反应(填“吸热”或“放热”)。
(3)在(1)的基础上,压缩容器体积为0.5L。该条件下的平衡常数为K3。则K3_______ K1(填“<”或”>”或“=”)。
(4)830℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应_______ (填“向正反应方向进行”或“向逆反应方向进行”或“处于平衡状态”)。
(5)某温度时,在2L密闭容器中发生:C(s)+H2O(g) CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为_______ ,此时容器内总压强与起始时的压强之比为_______ 。
 CO(g)+H2O(g),回答下列问题:
CO(g)+H2O(g),回答下列问题:(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。求该条件下的化学平衡常数K1=
(2)在(1)的基础上,把体系温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知该反应的正反应为
(3)在(1)的基础上,压缩容器体积为0.5L。该条件下的平衡常数为K3。则K3
(4)830℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应
(5)某温度时,在2L密闭容器中发生:C(s)+H2O(g)
 CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
您最近一年使用:0次
【推荐3】CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
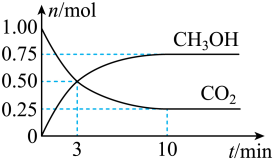
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的转化率为___________ 。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的转化率为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
您最近一年使用:0次

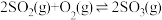 ,当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态
,当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态

