化学与生活密切相关。
I.K2Cr2O7曾用于检测司机是否酒后驾驶: (橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH(未配平)
(橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH(未配平)
(1)基态Cr原子的价电子轨道表达式为__ 。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为__ ,碳原子的轨道杂化类型为__ ,所含σ键与π键的数目之比为__ 。
(3)已知Cr3+等过渡元素水合离子的颜色如表所示:
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因为__ 。
II.ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。
(4)Fe[Zn(OH)Cl2]2溶液中不存在的微粒间作用力有__ (填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
溶液中[Zn(OH)Cl2]-的结构式为__ 。
III.锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。
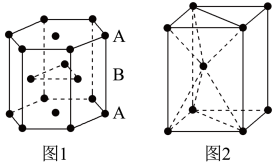
(5)锌的堆积方式为__ ,配位数为__ 。
(6)若锌原子的半径为apm,阿伏加 德罗常数的值为NA,则锌晶体的密度为___ g/cm3(用含a的代数式表示)。
I.K2Cr2O7曾用于检测司机是否酒后驾驶:
 (橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH(未配平)
(橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH(未配平)(1)基态Cr原子的价电子轨道表达式为
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为
(3)已知Cr3+等过渡元素水合离子的颜色如表所示:
| 离子 | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
| 水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因为
II.ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。
(4)Fe[Zn(OH)Cl2]2溶液中不存在的微粒间作用力有
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
溶液中[Zn(OH)Cl2]-的结构式为
III.锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。

(5)锌的堆积方式为
(6)若锌原子的半径为apm,阿伏加 德罗常数的值为NA,则锌晶体的密度为
更新时间:2020-06-09 10:01:06
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】12月 17日凌晨,嫦娥五号完成“ 挖土” 之旅返回地球。查阅资料,月球玄武岩是构成月球的岩石之一,主要由辉石(主要成分硅酸盐)和钛铁矿(主要成分 FeTiO3)等组成。回答下列问题:
(1)基态铁原子的价电子排布式为:______ 。
(2)与 Fe同周期,且最外层电子数相同的主族元素是______ (填元素符号)。
(3)基态 Ti原子核外电子占据的最高能层符号为______ ;其最外层电子的电子云轮廓图为______ 。
(4)1molFe3[Fe(CN)6]2中含有 σ键数为______ ,[Fe(CN)6]3-中配体为______ ,其中 C原子的杂化轨道类型为______ ,H、C、N、Si四种元素的电负性由大到小的顺序为______ 。
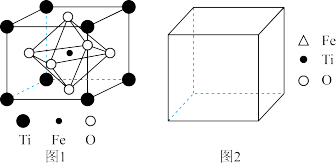
(5)FeTiO3的结构如图 1所示,其中由 O围成的______ (填“ 四面体空隙” 或“ 八面体空隙” )被 Fe占据。在图 2中画出 FeTiO3结构的另一种表示______ (要求:Fe处于晶胞的顶点),Ti的配位数为______ 。
(6)已知该晶胞的密度为 ρg/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数 a=______ pm。(列出计算表达式)
(1)基态铁原子的价电子排布式为:
(2)与 Fe同周期,且最外层电子数相同的主族元素是
(3)基态 Ti原子核外电子占据的最高能层符号为
(4)1molFe3[Fe(CN)6]2中含有 σ键数为
(5)FeTiO3的结构如图 1所示,其中由 O围成的
(6)已知该晶胞的密度为 ρg/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数 a=

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________ 。
(2)B、C、D三种元素的电负性由大到小的顺序是____________ (填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________ ,阴离子的中心原子轨道采用______________ 杂化。
(3)E(CA3) 离子的颜色是
离子的颜色是___________ ;含有化学键类型是_____________ ;离子中C原子杂化轨道类型是__________________ 。
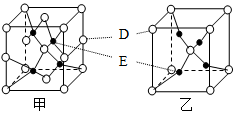
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________ ;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________ 。
(5)若甲的密度为ρ g/cm3,NA表示阿伏伽德罗常数,则甲晶胞的边长可表示为_________ cm。
(1)基态E原子核外电子的排布式为
(2)B、C、D三种元素的电负性由大到小的顺序是
(3)E(CA3)
 离子的颜色是
离子的颜色是(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为

(5)若甲的密度为ρ g/cm3,NA表示阿伏伽德罗常数,则甲晶胞的边长可表示为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态Ni原子价电子中成对电子数与未成对电子数之比为_________ 。
(2)MgO与CaO这两个物质,其中熔点较高的是______ ,原因是___________________________________________ 。
(3)第二周期中,第一电离能介于B元素和N元素之间的元素有_________ 种。
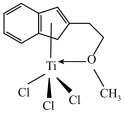
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合, 其结构如图所示。
①组成M的元素中,电负性最大的是__________ (填名称)。
②M中碳原子的杂化方式为__________ 。
③M中不含__________ (填代号)。
a、π键 b、σ键 c、离子键 d、配位键
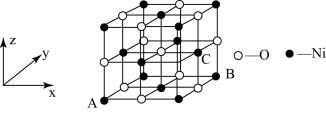
(5)NiO的晶体结构如图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为________________ 。
(1)基态Ni原子价电子中成对电子数与未成对电子数之比为
(2)MgO与CaO这两个物质,其中熔点较高的是
(3)第二周期中,第一电离能介于B元素和N元素之间的元素有
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合, 其结构如图所示。

①组成M的元素中,电负性最大的是
②M中碳原子的杂化方式为
③M中不含
a、π键 b、σ键 c、离子键 d、配位键
(5)NiO的晶体结构如图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】[化学——选修3:物质结构与性质]
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同。D原子最外层电子数为次外层电子数的3倍。E与D位于同一主族。A、B、D三种元素组成的一种化合物X是新装修居室中常含有的一种有害气体。由A、C、D、E、F五种元素按照原子个数比为14∶4∶5∶1∶1形成的化合物Y为深蓝色晶体。
回答下列问题:
(1) 基态E原子的价电子排布图为_____________________ 。
(2) 形成化合物Y的五种元素中第一电离能最大的是__________ ;电负性最大的是________ (填元素符号)。
(3) 化合物X中心原子的杂化方式为________ ,X分子中的两种键角的大小关系是_________________ (用∠XYZ表示,X、Y、Z代表元素符号)。
(4) C2D分子的立体结构为________________ ;A分别与B、C形成的简单化合物熔、沸点由高到低顺序为________ (用化学式表示),简单说明原因_________________ 。
(5) 晶体Y中存在的化学键类型有_____________________ 。(填代号)
A、离子键 B、非极性共价键 C、配位键 D、氢键 E、σ键 F、金属键
(6) 下图是D、F两种元素形成的化合物的晶胞结构示意图,F的配位数是_______________ ;已知晶胞中最近的两个D原子间距离为a nm,阿伏伽德罗常数用NA表示,则该晶体的密度为__________ g/cm3(用含a、NA的表达式表示)。

已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同。D原子最外层电子数为次外层电子数的3倍。E与D位于同一主族。A、B、D三种元素组成的一种化合物X是新装修居室中常含有的一种有害气体。由A、C、D、E、F五种元素按照原子个数比为14∶4∶5∶1∶1形成的化合物Y为深蓝色晶体。
回答下列问题:
(1) 基态E原子的价电子排布图为
(2) 形成化合物Y的五种元素中第一电离能最大的是
(3) 化合物X中心原子的杂化方式为
(4) C2D分子的立体结构为
(5) 晶体Y中存在的化学键类型有
A、离子键 B、非极性共价键 C、配位键 D、氢键 E、σ键 F、金属键
(6) 下图是D、F两种元素形成的化合物的晶胞结构示意图,F的配位数是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】选取下表中的合适物质的字母代号(A~H)填入相应标题(①-⑧)后的横线中(单选),并按要求填空。
①________ 不是平面分子,其衍生物用作高能燃料。
②________ 存在两种异构体,其中一种异构体的结构为:_______ 。
③________ 具有线型结构,Lewis结构式中每个键的键级为2.0。
④________ 是无色的,平面分子,它的一种等电子体是_______ 。
⑤________ 既有酸性,又有碱性,可作制冷剂。
⑥________ 既有酸性,又有碱性;既是氧化剂,又是还原剂,主要做_______ 剂。
⑦________ 是顺磁性分子。
⑧________ 水溶液会分解生成N2O,反应式为_______ 。
| A | B | C | D | E | F | G | H |
 | NO | N2O3 | N2H4 | NH3 | N2O4 | H2N2O2 | NH2OH |
①
②
③
④
⑤
⑥
⑦
⑧
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】中国是最早发现并使用青铜器的国家。司母戊鼎是迄今为止出土的世界上最大、最重的青铜礼器,享有“镇国之宝”的美誉(如图1)。
(1)Cu原子的外围电子排布式为_____ 。
(2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是____ ,I3远大于I2的原因是______ 。
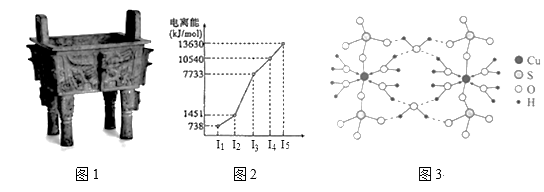
(3)图3是某含铜配合物的晶体结构示意图。
①晶体中H2O和SO42-的中心原子的杂化类型为_____ ,试判断H2O和SO42-的键角大小关系并说明原因_____ 。
②图3中的氢键有(H2O)O—H···O(H2O)和_______ 。
③写出该配合物的化学式_______ 。
(4)一种铜的氯化物晶胞结构如图所示。
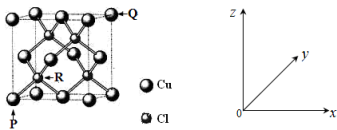
该化合物的化学式为______ ,已知P、Q、R的原子坐标分别(0,0,0)、(1,1,1)、( ,
, ,
, ),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为
),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为______ 。
(1)Cu原子的外围电子排布式为
(2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是

(3)图3是某含铜配合物的晶体结构示意图。
①晶体中H2O和SO42-的中心原子的杂化类型为
②图3中的氢键有(H2O)O—H···O(H2O)和
③写出该配合物的化学式
(4)一种铜的氯化物晶胞结构如图所示。

该化合物的化学式为
 ,
, ,
, ),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为
),若Cu原子与最近的Cl原子的核间距为apm,则该晶体的密度计算表达式为
您最近一年使用:0次
【推荐1】以铁矿石(Fe2O3)为起始物,经过一系列反应可以得到Fe3[Fe(CN)6]2和Fe(SCN)3,请回答下列问题:
(1)写出Fe的原子结构示意图_______ ,O原子核外电子轨道表示式为______ 。
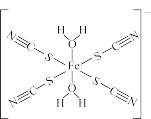
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为__________ 。如图是SCN−与Fe3+形成的一种配离子,画出该配离子中的配位键(以箭头表示)_______ 。
(3)K3[Fe(CN)6]晶体中Fe3+与CN−之间的键型为_______ ,该化学键能够形成的原因是_____ 。
(4)K3[Fe(CN)5NO]的组成元素中,属于第二周期的元素的第一电离能由小到大的顺序是_____ ,配合物中原子序数最小的元素与氢元素形成的相对分子质量为92的芳香化合物中,中心原子的杂化轨道类型是_________ 。
(5)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写出该变化的化学方程式______ 。
(6)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为____ ,若该晶胞边长为acm,则该晶体密度为___ g/cm3(阿伏伽德罗常数的值为NA)。
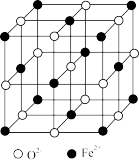
(1)写出Fe的原子结构示意图
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为

(3)K3[Fe(CN)6]晶体中Fe3+与CN−之间的键型为
(4)K3[Fe(CN)5NO]的组成元素中,属于第二周期的元素的第一电离能由小到大的顺序是
(5)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写出该变化的化学方程式
(6)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】金属镍及其化合物在合成材料以及催化剂等方面应用广泛。请回答下列问题:
(1)基态Ni原子的核外电子排布图为___________
(2)NiO、FeO晶体类型及晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为___________ ;又知Ni2+、Fe2+的离子半径分别为69pm、78pm,则NiO熔点___________ FeO(填“>”“<”或“=”)。
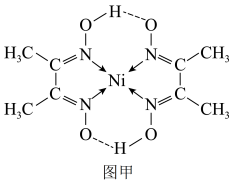
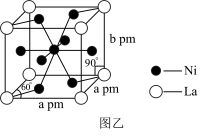
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中C原子的杂化类型为___________ ;元素H、C、N、O、Ni电负性由大到小的顺序为___________ 。___________ ;晶体密度为___________ g·cm-3(列出含a、b、NA的计算表达式,NA表示阿伏加德罗常数的值)。
(1)基态Ni原子的核外电子排布图为
(2)NiO、FeO晶体类型及晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中C原子的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】W、X、Y、Z、R为原子序数依次增大的短周期主族元素,W的核外电子只有一种自旋方向;Y、Z、R在元素周期表中相邻,X的核外电子数与Y的价层电子数相等,R2是氧化性最强的单质,回答下列问题:
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是___________ (填标号)。
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3___________ XR3(填“>”或“<”或“=”);YR3与YW3结构相似,YW3易与过渡金属阳离子形成配离子而YR3不能,原因是___________ 。
(3)同周期元素中,第一电离能比Z大的元素有_________ 种;Z与Y形成的固态Y2Z5由YZ 和YZ
和YZ 两种离子组成,固态Y2Z5中Y原子的杂化方式为
两种离子组成,固态Y2Z5中Y原子的杂化方式为_________ ,YZ 的电子式为
的电子式为_________ 。
(4)X与Z可形成多种结构形式的阴离子,已知阴离子X3Z 结构中只有一个正六元环,则n=
结构中只有一个正六元环,则n=___________ ,该阴离子的结构式为___________ 。
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3
(3)同周期元素中,第一电离能比Z大的元素有
 和YZ
和YZ 两种离子组成,固态Y2Z5中Y原子的杂化方式为
两种离子组成,固态Y2Z5中Y原子的杂化方式为 的电子式为
的电子式为(4)X与Z可形成多种结构形式的阴离子,已知阴离子X3Z
 结构中只有一个正六元环,则n=
结构中只有一个正六元环,则n=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子核外电子的空间运动状态有______ 种,若其电子排布式表示为 违背了
违背了______ 。
(2)高纯硅制备过程中会有 等中间产物生成。沸点:
等中间产物生成。沸点:
______  (填“>”或“<”)。
(填“>”或“<”)。
(3)复兴号高铁车体材质用到 等元素。
等元素。
① 的一种配合物化学式为
的一种配合物化学式为 ,下列说法正确的是
,下列说法正确的是______ (填字母标号)。
A. 与
与 原子配位时,提供孤电子对的是
原子配位时,提供孤电子对的是 原子
原子
B.Mn原子的配位数为6
C. 中
中 键与
键与 键数目之比为
键数目之比为
D. 中C原子的杂化类型为
中C原子的杂化类型为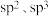
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测 比
比 的分解温度
的分解温度______ (填“高”或“低”),解释原因____________
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有 型结构(如图),晶胞参数(晶胞边长)为
型结构(如图),晶胞参数(晶胞边长)为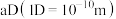 ,其中阴离子
,其中阴离子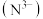 采用面心立方最密堆积方式,则
采用面心立方最密堆积方式,则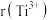 为
为______ D,该氮化钛的密度______  (列出计算式即可)。
(列出计算式即可)。

(1)5G芯片主要材质是高纯硅。基态Si原子核外电子的空间运动状态有
 违背了
违背了(2)高纯硅制备过程中会有
 等中间产物生成。沸点:
等中间产物生成。沸点:
 (填“>”或“<”)。
(填“>”或“<”)。(3)复兴号高铁车体材质用到
 等元素。
等元素。①
 的一种配合物化学式为
的一种配合物化学式为 ,下列说法正确的是
,下列说法正确的是A.
 与
与 原子配位时,提供孤电子对的是
原子配位时,提供孤电子对的是 原子
原子B.Mn原子的配位数为6
C.
 中
中 键与
键与 键数目之比为
键数目之比为
D.
 中C原子的杂化类型为
中C原子的杂化类型为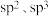
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测
 比
比 的分解温度
的分解温度(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有
 型结构(如图),晶胞参数(晶胞边长)为
型结构(如图),晶胞参数(晶胞边长)为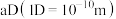 ,其中阴离子
,其中阴离子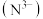 采用面心立方最密堆积方式,则
采用面心立方最密堆积方式,则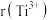 为
为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】氨的催化氧化反应是硝酸工业中的重要反应,某条件下 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.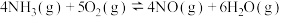
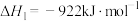
Ⅱ.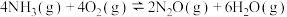
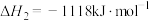
Ⅲ.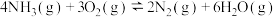

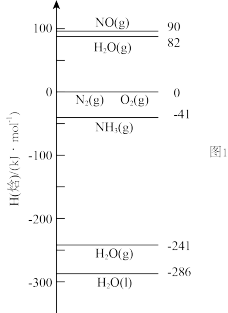
已知:298K时,相关物质的焓的数据如图1。
(1)根据相关物质的焓计算
_______ 
(2)将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图2所示。
的选择性与温度的关系如图2所示。
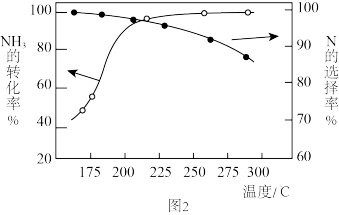
①除去工业尾气中的 适宜的温度为
适宜的温度为_______ 。
②随着温度的升高, 的选择性下降的原因可能为
的选择性下降的原因可能为_______ 。
(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
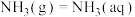

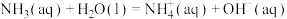

其中p为 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度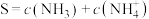 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为_______ 。
(4)为了探究大气中 对
对 和
和 反应的影响,图3和图4展示了无
反应的影响,图3和图4展示了无 与有
与有 存在时反应过程的相关优化构型,表1列出了相关构型的相对能量。
存在时反应过程的相关优化构型,表1列出了相关构型的相对能量。
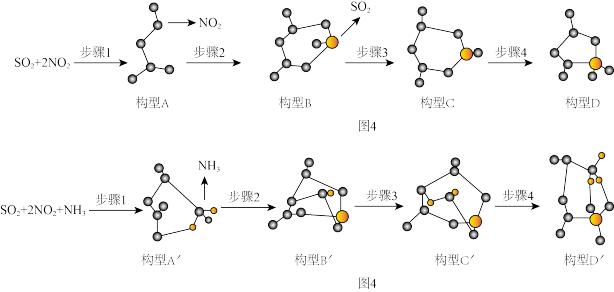
①无 存在时的决速步骤为
存在时的决速步骤为_______ 。
②对比图3与图4, 的功能为
的功能为_______ 。
(5)已知Mg、A1、O三种元素组成的晶体结构如图所示,其晶胞由4个A型小晶格和4个B型小晶格构成,其中 和
和 都在小晶格内部,
都在小晶格内部, 部分在小晶格内部,部分在小晶格顶点。
部分在小晶格内部,部分在小晶格顶点。
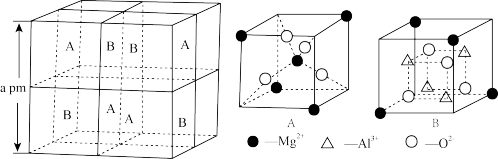
该物质的化学式为_______ , 的配位数为
的配位数为_______ ,两个 之间最近的距离是
之间最近的距离是_______ pm。
 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.
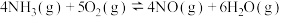
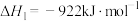
Ⅱ.
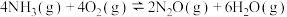
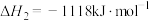
Ⅲ.
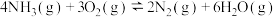

已知:298K时,相关物质的焓的数据如图1。
(1)根据相关物质的焓计算


(2)将一定比例的
 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图2所示。
的选择性与温度的关系如图2所示。
①除去工业尾气中的
 适宜的温度为
适宜的温度为②随着温度的升高,
 的选择性下降的原因可能为
的选择性下降的原因可能为(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
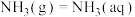

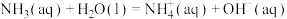

其中p为
 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度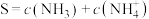 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为(4)为了探究大气中
 对
对 和
和 反应的影响,图3和图4展示了无
反应的影响,图3和图4展示了无 与有
与有 存在时反应过程的相关优化构型,表1列出了相关构型的相对能量。
存在时反应过程的相关优化构型,表1列出了相关构型的相对能量。
| 构型 | 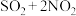 | 构型A | 构型B | 构型C | 构型D |
相对能量/ | 0 | -7.33 | -11.78 | 33.70 | -23.27 |
| 构型 | 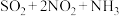 | 构型A′ | 构型B′ | 构型C′ | 构型D′ |
相对能量/ | 0 | -10.18 | -15.12 | 25.48 | -35.22 |
 存在时的决速步骤为
存在时的决速步骤为②对比图3与图4,
 的功能为
的功能为(5)已知Mg、A1、O三种元素组成的晶体结构如图所示,其晶胞由4个A型小晶格和4个B型小晶格构成,其中
 和
和 都在小晶格内部,
都在小晶格内部, 部分在小晶格内部,部分在小晶格顶点。
部分在小晶格内部,部分在小晶格顶点。
该物质的化学式为
 的配位数为
的配位数为 之间最近的距离是
之间最近的距离是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】钛被称为“二十一世纪的金属”,绿矾是重要的化工原料,用钛铁矿[主要成分是钛酸亚铁( ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下: (无色)、
(无色)、 (紫色)形式存在。
(紫色)形式存在。
请回答下列问题:
(1)硫酸与 反应生成
反应生成 的化学方程式是
的化学方程式是______ 。向滤液1中加入适量铁粉,至刚好出现紫色为止,此时溶液仍呈强酸性。已知:氧化性: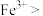
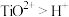 ,则加入适量铁粉的原因是
,则加入适量铁粉的原因是______ 。
(2)系列操作具体为______ ,经系列操作后,再对所得到的绿矾晶体用75%的乙醇溶液洗涤,用乙醇溶液洗涤绿矾的优点为______ 。
(3)滤液2中加入适量的试剂A,A可选用______ (填标号)。
a.稀硫酸 b.碳酸镁 c.二氧化碳 d.鼓入空气
(4)用石墨作阳极、钛网作阴极、熔融 -CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:
-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:______ 。 中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
______ kg。
(6)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为______ 。
 ),含少量
),含少量 、MgO、
、MgO、 等杂质]作原料生产金属钛和绿矾(
等杂质]作原料生产金属钛和绿矾( )等产品的一种工艺流程如下:
)等产品的一种工艺流程如下: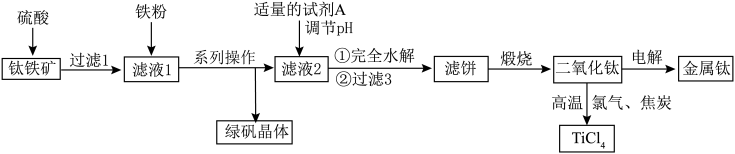
 (无色)、
(无色)、 (紫色)形式存在。
(紫色)形式存在。请回答下列问题:
(1)硫酸与
 反应生成
反应生成 的化学方程式是
的化学方程式是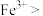
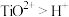 ,则加入适量铁粉的原因是
,则加入适量铁粉的原因是(2)系列操作具体为
(3)滤液2中加入适量的试剂A,A可选用
a.稀硫酸 b.碳酸镁 c.二氧化碳 d.鼓入空气
(4)用石墨作阳极、钛网作阴极、熔融
 -CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:
-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。写出阴极区反应的电极总反应式:
 中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
中的铁元素占矿物中铁元素总量的80%;某次生产中,向滤液1中加入纯铁粉14kg,得到绿矾晶体(M=278g/mol)的质量为278kg,整个过程中铁元素的总利用率为80%,Ti元素的转化率为90%,其他损失忽略不计。按上述流程,可得到
(6)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为

您最近一年使用:0次



