次硫酸氢钠甲醛(NaHSO2·HCHO·2H2O,M=154.0g·mol-1)俗称吊白块,易溶于水,微溶于乙醇,在120℃以上易分解。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
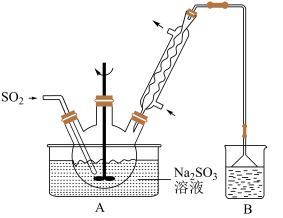
步骤1:在三颈烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。
步骤2:向三颈烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80℃~90℃下,反应约3h,冷却至室温,抽滤。
步骤3:将滤液经结晶、抽滤、洗涤等操作后制得粗产品。
(1)步骤2中加入锌粉反应时会有Zn(OH)2生成,写出发生反应的化学方程式_____________ ;为防止生成的Zn(OH)2覆盖在锌粉表面阻止反应进行,可采取的措施是_____________ 。
(2)下列说法中不正确的是_____________ 。
A.装置B的作用是吸收尾气
B.该实验的加热方式最好选用水浴加热
C.步骤2抽滤的滤渣成分只有Zn(OH)2固体
D.步骤3得到的产品可以在烘箱中高温烘干
(3)如图装置,经过一系列操作完成步骤3中的结晶和洗涤操作。请选择合适的字母,按正确的操作顺序补充完整(洗涤操作只需考虑一次):_____→固液转移至布氏漏斗→开抽气泵→c→f→________→_________→_________→________→d→关抽气泵。_____________
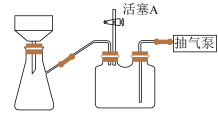
a.将滤液蒸发至大量晶体出现
b.将滤液真空浓缩,冷却结晶
c.关闭活塞A
d.打开活塞A
e.加乙醇洗涤
f.确认抽干
(4)将0.5000g样品充分加热分解,释放出的HCHO用36.00mL0.1000mol·L-1KMnO4溶液吸收(不考虑SO2的影响,5HCHO+4 +12H+=5CO2↑+4Mn2++11H2O),再用0.1000mol·L-1H2C2O4溶液滴定KMnO4溶液,重复实验3次,平均消耗H2C2O4溶液的体积为30.00mL,则样品的纯度为
+12H+=5CO2↑+4Mn2++11H2O),再用0.1000mol·L-1H2C2O4溶液滴定KMnO4溶液,重复实验3次,平均消耗H2C2O4溶液的体积为30.00mL,则样品的纯度为_____________ 。

步骤1:在三颈烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。
步骤2:向三颈烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80℃~90℃下,反应约3h,冷却至室温,抽滤。
步骤3:将滤液经结晶、抽滤、洗涤等操作后制得粗产品。
(1)步骤2中加入锌粉反应时会有Zn(OH)2生成,写出发生反应的化学方程式
(2)下列说法中不正确的是
A.装置B的作用是吸收尾气
B.该实验的加热方式最好选用水浴加热
C.步骤2抽滤的滤渣成分只有Zn(OH)2固体
D.步骤3得到的产品可以在烘箱中高温烘干
(3)如图装置,经过一系列操作完成步骤3中的结晶和洗涤操作。请选择合适的字母,按正确的操作顺序补充完整(洗涤操作只需考虑一次):_____→固液转移至布氏漏斗→开抽气泵→c→f→________→_________→_________→________→d→关抽气泵。

a.将滤液蒸发至大量晶体出现
b.将滤液真空浓缩,冷却结晶
c.关闭活塞A
d.打开活塞A
e.加乙醇洗涤
f.确认抽干
(4)将0.5000g样品充分加热分解,释放出的HCHO用36.00mL0.1000mol·L-1KMnO4溶液吸收(不考虑SO2的影响,5HCHO+4
 +12H+=5CO2↑+4Mn2++11H2O),再用0.1000mol·L-1H2C2O4溶液滴定KMnO4溶液,重复实验3次,平均消耗H2C2O4溶液的体积为30.00mL,则样品的纯度为
+12H+=5CO2↑+4Mn2++11H2O),再用0.1000mol·L-1H2C2O4溶液滴定KMnO4溶液,重复实验3次,平均消耗H2C2O4溶液的体积为30.00mL,则样品的纯度为
更新时间:2020-07-02 10:37:27
|
相似题推荐
【推荐1】回答下列问题:
(1)ClO2是新型自来水消毒剂,具有强氧化性。其一种生产工艺如图甲所示:

①电解反应的化学方程式为_______ 。
②NCl3具有强氧化性,制取ClO2反应的化学方程式为_______ 。
③饮用水中残留的ClO2可用适量FeSO4溶液去除,该反应的离子方程式为_______ 。
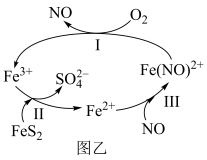
(2)在酸性条件下,黄铁矿(FeS2)催化氧化的流程如图乙,反应Ⅱ的离子方程式为:_______ 。
(1)ClO2是新型自来水消毒剂,具有强氧化性。其一种生产工艺如图甲所示:

①电解反应的化学方程式为
②NCl3具有强氧化性,制取ClO2反应的化学方程式为
③饮用水中残留的ClO2可用适量FeSO4溶液去除,该反应的离子方程式为
(2)在酸性条件下,黄铁矿(FeS2)催化氧化的流程如图乙,反应Ⅱ的离子方程式为:

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
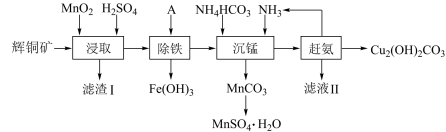
【推荐2】碱式碳酸铜在有机催化、电镀、防腐、烟火、农药、颜料、杀菌剂等方面应用广泛。一种以辉铜矿(主要成分为Cu2S,含有SiO2和少量Fe2O3等杂质)为原料制备碱式碳酸铜的流程如图所示:
已知:
①有关金属离子形成氢氧化物沉淀的pH范围如下:
②[Cu(NH3)4]SO4常温稳定,在热水中会分解生成NH3;
③Ksp[Fe(OH)3] = 4.0 ×10-38;
④S在CS2中的溶解度随温度升高而增大;
⑤CS2的沸点: 46.2°C。
回答下列问题:
(1)为了加快辉铜矿的“浸取”速率,可采取的措施有_______ (任写一种)。
(2)滤渣I经CS2提取后可获得一种淡黄色副产品,则滤渣I中的主要成分有_______ (填化学式)。回收该淡黄色副产品过程中必须控制适宜的温度,不宜过高或过低的原因是_______ , “浸取” 过程中,辉铜矿中的Cu2S与MnO2及稀硫酸反应的离子方程式为_______ 。
(3)常温下,加入的试剂A若为CuO,其“除铁”的原理是_______ (从平衡移动的角度进行解释),调节pH的范围为________ ,加一定量的CuO后,若测得溶液的pH为4,则溶液中Fe3+的浓度为_______ mol·L-1。
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式_______ 。

已知:
①有关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀的pH | 9.0 | 3.7 | 6.7 | 9.8 |
③Ksp[Fe(OH)3] = 4.0 ×10-38;
④S在CS2中的溶解度随温度升高而增大;
⑤CS2的沸点: 46.2°C。
回答下列问题:
(1)为了加快辉铜矿的“浸取”速率,可采取的措施有
(2)滤渣I经CS2提取后可获得一种淡黄色副产品,则滤渣I中的主要成分有
(3)常温下,加入的试剂A若为CuO,其“除铁”的原理是
(4)写出“沉锰”(除Mn2+)过程中反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】高纯硝酸锶[Sr(NO3)2]可用于制造信号灯,光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如图:
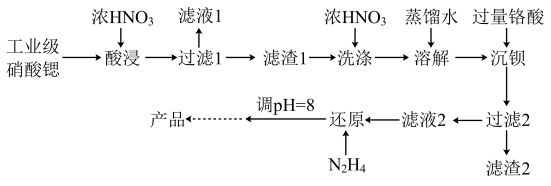
已知:①“滤渣1”的成分为Ba(NO3)2、Sr(NO3)2;②铬酸(H2CrO4)为二元弱酸
(1)用铬酸(H2CrO4)“沉钡”,是工业上常用的方法。H2CrO4中Cr元素的化合价为__ ,其在水中的电离方程式为___ 。
(2)“酸浸”不能采用高温的原因是__ ,“滤液1”的主要溶质是__ (写化学式)。
(3)相对于水洗,用浓HNO3洗涤的优点是__ 。
(4)“滤液2”中过量的H2CrO4被N2H4还原为Cr3+,同时放出无污染的气体,写出发生反应的离子方程式__ 。
(5)已知Cr(OH)3类似氢氧化铝,还原后溶液的pH不能大于8的原因是(用离子方程式说明理由)__ 。

已知:①“滤渣1”的成分为Ba(NO3)2、Sr(NO3)2;②铬酸(H2CrO4)为二元弱酸
(1)用铬酸(H2CrO4)“沉钡”,是工业上常用的方法。H2CrO4中Cr元素的化合价为
(2)“酸浸”不能采用高温的原因是
(3)相对于水洗,用浓HNO3洗涤的优点是
(4)“滤液2”中过量的H2CrO4被N2H4还原为Cr3+,同时放出无污染的气体,写出发生反应的离子方程式
(5)已知Cr(OH)3类似氢氧化铝,还原后溶液的pH不能大于8的原因是(用离子方程式说明理由)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】过氧乙酸(CH3COOOH)不仅被广泛使用在医疗器械清洗、灭菌、消毒,而且在灾区、隔离区、疫区等地的消毒和预防性消毒中被使用,还具有漂白性。常温下过氧乙酸是无色透明,有刺激性酸味液体,易挥发,易溶于水和有机溶剂。可利用冰乙酸和浓度为70%的H2O2反应,制备浓度为40%左右的过氧乙酸。回答下列问题:
(一)制备高浓度
实验装置如图所示。用真空泵抽气减压并维持在真空度10mmHg,将30%H2O2以每2秒1滴的速度滴入蛇形冷凝管中,恒温热水使溶液中的水气化,分离出水后得到较高浓度的H2O2,再以所得H2O2重复上述提纯操作,提纯若干次后H2O2的浓度即可达到70%。

(1)仪器X的名称是_____ ;接真空泵抽气减压的目的是_____ (填标号)。
A.提高液体的沸点 B.降低液体的沸点
C.将H2O蒸气抽进直形冷凝管分离 D.将H2O2蒸气抽进直形冷凝管分离
(2)为探究制备高浓度H2O2的适宜条件,保持真空度和滴速不变,实验结果如表:
由上述数据可知,其它条件不变,制备70%过氧化氢的适宜条件为_____ ;若温度过高,不利于制备高浓度H2O2,原因是_____ 。
(3)与如图装置比较,前述装置的优点是_____ 。

(二)高浓度过氧乙酸的制备及浓度测定
称取40g70%过氧化氢放入250mL的烧杯中,加入50g冰乙酸(CH,COOH).将其放入磁力搅拌器上,边搅拌边滴加2.7g浓硫酸。滴加完毕,密封搅拌1h后避光放置12h。
(4)制备过氧乙酸(CH3COOOH)的化学方程式为_____ 。
(5)过氧乙酸(含有少量H2O2杂质)的浓度测定流程:取样→H2SO4,酸化的KMnO4除H2O2→过量FeSO4溶液还原CH3COOOH→K2Cr2O7溶液滴定剩余FeSO4。
①酸化KMnO4溶液用硫酸而不能用盐酸的原因是_____ 。
②过氧乙酸被Fe2+还原,还原产物为CH3COOH,其离子方程式为_____ 。
③若过氧乙酸样品体积为V0mL,加入c1mol·L-1FeSO4,溶液V1mL,消耗c2mol·L-1K2Cr2O7溶液V2mL,则过氧乙酸浓度为_____ g·L-1。
(6)过氧乙酸的漂白原理与下列哪些物质相同_____ 。(填标号)。
①二氧化硫 ②次氯酸 ③活性炭 ④臭氧
(一)制备高浓度
实验装置如图所示。用真空泵抽气减压并维持在真空度10mmHg,将30%H2O2以每2秒1滴的速度滴入蛇形冷凝管中,恒温热水使溶液中的水气化,分离出水后得到较高浓度的H2O2,再以所得H2O2重复上述提纯操作,提纯若干次后H2O2的浓度即可达到70%。

(1)仪器X的名称是
A.提高液体的沸点 B.降低液体的沸点
C.将H2O蒸气抽进直形冷凝管分离 D.将H2O2蒸气抽进直形冷凝管分离
(2)为探究制备高浓度H2O2的适宜条件,保持真空度和滴速不变,实验结果如表:
| 恒温热水温度/℃ | 初始过氧化氢的浓度/% | 最终过氧化氢的浓度/% | 提纯次数 |
| 65 | 30 | 70 | 5 |
| 75 | 30 | 70 | 3 |
| 85 | 30 | 70 | 2 |
(3)与如图装置比较,前述装置的优点是

(二)高浓度过氧乙酸的制备及浓度测定
称取40g70%过氧化氢放入250mL的烧杯中,加入50g冰乙酸(CH,COOH).将其放入磁力搅拌器上,边搅拌边滴加2.7g浓硫酸。滴加完毕,密封搅拌1h后避光放置12h。
(4)制备过氧乙酸(CH3COOOH)的化学方程式为
(5)过氧乙酸(含有少量H2O2杂质)的浓度测定流程:取样→H2SO4,酸化的KMnO4除H2O2→过量FeSO4溶液还原CH3COOOH→K2Cr2O7溶液滴定剩余FeSO4。
①酸化KMnO4溶液用硫酸而不能用盐酸的原因是
②过氧乙酸被Fe2+还原,还原产物为CH3COOH,其离子方程式为
③若过氧乙酸样品体积为V0mL,加入c1mol·L-1FeSO4,溶液V1mL,消耗c2mol·L-1K2Cr2O7溶液V2mL,则过氧乙酸浓度为
(6)过氧乙酸的漂白原理与下列哪些物质相同
①二氧化硫 ②次氯酸 ③活性炭 ④臭氧
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,在二元弱酸H2C2O4(草酸)溶液中滴加NaOH溶液,所得混合溶液的pH与溶液中离子浓度比的对数值的关系分别如下图所示。

(1)写出H2C2O4的电离方程式:_______ 。
(2) 与pH关系是曲线
与pH关系是曲线_______ (填“M”或“N”)。
(3)写出e点时溶液中发生的主要离子反应方程式_______ 。
(4)NaHC2O4溶液显_______ (填“酸”或“碱”)性,请用数据说明:_______ 。
(5)已知:难溶物Ag2C2O4的Ksp=5.0 ×10-l2,在0.001mol/L 10mL的Na2C2O4溶液中加入等体积、浓度至少为_______ mol/L的AgNO3溶液时才能生成沉淀。
(6)查阅资料,草酸可与酸性高锰酸钾发生如下反应: MnO +H2C2O4+H+→Mn2++CO2↑+ H2O(未配平)。可利用酸性高锰酸钾标准溶液滴定草酸并测取草酸溶液的浓度,滴定达到终点时现象为
+H2C2O4+H+→Mn2++CO2↑+ H2O(未配平)。可利用酸性高锰酸钾标准溶液滴定草酸并测取草酸溶液的浓度,滴定达到终点时现象为_______ 。用0.1000mol/L酸性高锰酸钾标准溶液滴定10.00mL草酸溶液时,消耗标准液的体积如下表。通过计算可知c(H2C2O4)= _______ mol/L。若滴定时所用的酸性高锰酸钾溶液因久置导致浓度变小,则由此测得的c(H2C2O4)会_______ (填“偏大”、“偏小”或“不变”)。

(1)写出H2C2O4的电离方程式:
(2)
 与pH关系是曲线
与pH关系是曲线(3)写出e点时溶液中发生的主要离子反应方程式
(4)NaHC2O4溶液显
(5)已知:难溶物Ag2C2O4的Ksp=5.0 ×10-l2,在0.001mol/L 10mL的Na2C2O4溶液中加入等体积、浓度至少为
(6)查阅资料,草酸可与酸性高锰酸钾发生如下反应: MnO
 +H2C2O4+H+→Mn2++CO2↑+ H2O(未配平)。可利用酸性高锰酸钾标准溶液滴定草酸并测取草酸溶液的浓度,滴定达到终点时现象为
+H2C2O4+H+→Mn2++CO2↑+ H2O(未配平)。可利用酸性高锰酸钾标准溶液滴定草酸并测取草酸溶液的浓度,滴定达到终点时现象为| 初读数V0(mL) | 末读数V1 (mL) | |
| 第一次 | 1.00 | 11.10 |
| 第二次 | 1.50 | 15.30 |
| 第三次 | 2.20 | 12.10 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠。制取装置如图(加热和夹持仪器已略去),部分物质性质如下:

(1)C中盛放Bi(OH)3与NaOH的混合物,与Cl2反应生成NaBiO3,反应的化学方程式为:_______ ,B装置的作用是_______ 。
(2)当观察到_______ (填现象)时,可以初步判断C中反应已经完成。
(3)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭_______ ;打开_______ 。
(4)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有_______ 、过滤、_______ 。
Ⅱ.铋酸钠的应用——检验Mn2+
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。产生紫红色现象的离子方程式为_______ 。
Ⅲ.产品纯度的测定
(6)取上述NaBiO3产品ag,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用bmol·L−1的H2C2O4标准溶液滴定生成的MnO (已知:H2C2O4+MnO
(已知:H2C2O4+MnO —CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗cmL标准溶液。该产品的纯度为
—CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗cmL标准溶液。该产品的纯度为_______ (用含a、b、c的代数式表示)。
Ⅰ.制取铋酸钠。制取装置如图(加热和夹持仪器已略去),部分物质性质如下:

| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水;浅黄色 | 难溶于水;白色 |
(2)当观察到
(3)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭
(4)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有
Ⅱ.铋酸钠的应用——检验Mn2+
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。产生紫红色现象的离子方程式为
Ⅲ.产品纯度的测定
(6)取上述NaBiO3产品ag,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用bmol·L−1的H2C2O4标准溶液滴定生成的MnO
 (已知:H2C2O4+MnO
(已知:H2C2O4+MnO —CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗cmL标准溶液。该产品的纯度为
—CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗cmL标准溶液。该产品的纯度为
您最近一年使用:0次
【推荐1】融雪剂通过降低冰雪融化温度的原理融化道路上的积雪。研究发现,一般融雪剂残留物可腐蚀路面和汽车轮胎等。目前我国北方在冬季仍采用沙土和铲雪车为主,融雪剂为辅的方式清除路面冰雪,保证道路通畅。
请回答下列问题:
(1)氯化钙是常用融雪剂的主要成分之一,以工业碳酸钙(含有少量Na+、Mg2+、Fe3+等杂质)生产氯化钙的主要流程如下:

①流程中试剂W的名称是________________ 。
②流程中滤渣的主要成分是________________ (填化学式)。
③流程中操作Y的目的是_______________ 。
④如果用惰性电极电解用试剂W溶解后的溶液,则电解开始时阴极发生的电极反应式为_________ 。
(2)下列就融雪剂使用的有关原理的解释正确的是_________________ 。
A.“会加快冰雪的融化”是因为提高了冰点
B.“会造成绿化植物死亡”是与盐析有关
C.“会造成土壤板结贫瘠”是与物质的分解吸热有关
D.“会加快路基上铁的腐蚀”是与形成原电池有关
(3)某公司生产的融雪剂由NaCl、NaNO3、AlCl3、CuSO4、K2CO3中的几种物质组成。某同学设计下列过程探究其组成:

请回答下列问题:
①该融雪剂中一定不含的物质是_________________ (填名称)。
②若取融雪剂样品a g,通过上述探究途径得白色沉淀乙bmol,则该融雪剂中含氯元素的质量分数为____________________________ 。
请回答下列问题:
(1)氯化钙是常用融雪剂的主要成分之一,以工业碳酸钙(含有少量Na+、Mg2+、Fe3+等杂质)生产氯化钙的主要流程如下:

①流程中试剂W的名称是
②流程中滤渣的主要成分是
③流程中操作Y的目的是
④如果用惰性电极电解用试剂W溶解后的溶液,则电解开始时阴极发生的电极反应式为
(2)下列就融雪剂使用的有关原理的解释正确的是
A.“会加快冰雪的融化”是因为提高了冰点
B.“会造成绿化植物死亡”是与盐析有关
C.“会造成土壤板结贫瘠”是与物质的分解吸热有关
D.“会加快路基上铁的腐蚀”是与形成原电池有关
(3)某公司生产的融雪剂由NaCl、NaNO3、AlCl3、CuSO4、K2CO3中的几种物质组成。某同学设计下列过程探究其组成:

请回答下列问题:
①该融雪剂中一定不含的物质是
②若取融雪剂样品a g,通过上述探究途径得白色沉淀乙bmol,则该融雪剂中含氯元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】二氧化氯( )是一种高效消毒灭菌剂,可以作为自来水的杀菌消毒试剂。
)是一种高效消毒灭菌剂,可以作为自来水的杀菌消毒试剂。 还原氯酸钠法为一种常见的制备方法,通过
还原氯酸钠法为一种常见的制备方法,通过 与
与 在催化剂、60℃条件下发生反应得到
在催化剂、60℃条件下发生反应得到 ,装置如图所示。
,装置如图所示。

已知:① 与KI反应的离子方程式为
与KI反应的离子方程式为 。
。
②有关物质沸点如表所示:
请回答下列问题:
(1)仪器b的名称是_______ ,其作用是_______ 。
(2)反应中甲醇被氧化为甲酸,写出制备 的化学方程式:
的化学方程式:_______ 。
(3)草酸( )是一种弱酸,利用硫酸酸化的草酸还原
)是一种弱酸,利用硫酸酸化的草酸还原 ,也可较安全地生成
,也可较安全地生成 的离子方程式为
的离子方程式为_______ 。相对于甲醇还原法,草酸还原法较为明显的缺点是_______ 。
(4)该装置中需改进的是_______ 。
(5)自来水厂用碘量法检测水中 的含量,其实验操作如下:取200.00mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的含量,其实验操作如下:取200.00mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定(
标准溶液滴定(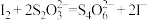 ),达到滴定终点时用去20.00mL
),达到滴定终点时用去20.00mL 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为_______  (保留一位小数)。
(保留一位小数)。
 )是一种高效消毒灭菌剂,可以作为自来水的杀菌消毒试剂。
)是一种高效消毒灭菌剂,可以作为自来水的杀菌消毒试剂。 还原氯酸钠法为一种常见的制备方法,通过
还原氯酸钠法为一种常见的制备方法,通过 与
与 在催化剂、60℃条件下发生反应得到
在催化剂、60℃条件下发生反应得到 ,装置如图所示。
,装置如图所示。
已知:①
 与KI反应的离子方程式为
与KI反应的离子方程式为 。
。②有关物质沸点如表所示:
| 物质 |  |  |  |
| 沸点/℃ | 64.7 | 100.8 | 11 |
(1)仪器b的名称是
(2)反应中甲醇被氧化为甲酸,写出制备
 的化学方程式:
的化学方程式:(3)草酸(
 )是一种弱酸,利用硫酸酸化的草酸还原
)是一种弱酸,利用硫酸酸化的草酸还原 ,也可较安全地生成
,也可较安全地生成 的离子方程式为
的离子方程式为(4)该装置中需改进的是
(5)自来水厂用碘量法检测水中
 的含量,其实验操作如下:取200.00mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的含量,其实验操作如下:取200.00mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定(
标准溶液滴定(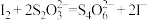 ),达到滴定终点时用去20.00mL
),达到滴定终点时用去20.00mL 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为 (保留一位小数)。
(保留一位小数)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】有一Na2SO3固体因部分被氧化而变质。为测定样品纯度,甲、乙两位同学分别设计了如下实验方案:
【甲同学】称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是___________________________________________ 。在滤液中滴加____________ 溶液,若没有白色沉淀生成,则证明BaCl2溶液不足,还需继续在滤液中加入BaCl2溶液后进行过滤。洗涤残留固体的方法是__________________________________________________ ;在洗出液中滴加_______________ 溶液,可以判断残留固体是否洗涤干净。
(2)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是_________________________________________________________ 。
【乙同学】称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+ (未配平)
(3)配制样品溶液时,不一定 需要的实验仪器是__________ (选填答案编号)。
a.容量瓶 b.玻璃棒 c.滴定管 d.烧杯
(4)滴定终点的判断依据是___________________________________________________ 。
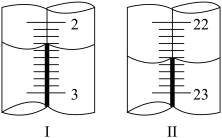
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用__________________________________________ 。滴定管液面变化如图所示,从图Ⅰ图Ⅱ显示消耗的高锰酸钾溶液体积为__________________ 。
【甲同学】称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是
(2)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是
【乙同学】称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+ (未配平)
(3)配制样品溶液时,
a.容量瓶 b.玻璃棒 c.滴定管 d.烧杯
(4)滴定终点的判断依据是
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】TiCl4是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备TiCl4(夹持装置略去)。

已知:TiCl4易挥发,高温时能与O2反应,不与HCl反应,其他相关信息如下表所示:
回答下列问题:
(1)A装置仪器b的名称是___________ ,E装置中的试剂是_________________ 。
(2)装置A中发生反应的离子方程式为________ 。
(3)在通入Cl2前,先打开开关k,从侧管持续通入一段时间的CO2气体的目的是______________________________ 。
(4)装置C中除生成TiCl4外,还生成一种气态不成盐氧化物,该反应的化学方程式为:___ 。
(5)制得的TiCl4中常含有少量CCl4,从混合液中分离出TiCl4操作的名称是______ 。
(6)利用如图装置测定所得TiCl4的纯度:

取wg产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待TiCl4充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴0.1mol·L-1K2CrO4溶液作指示剂,用cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液VmL。已知:常温下Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=1.1×10-12,Ag2CrO4呈砖红色, TiCl4+(2+n)H2O=TiO2·nH2O↓+4HCl
①滴定终点的判断方法是______________________ 。
②产品的纯度为___________ (用含w、c和V的代数式表示)。

已知:TiCl4易挥发,高温时能与O2反应,不与HCl反应,其他相关信息如下表所示:
| 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 水溶性 | |
| TiCl4 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
| CC14 | -23 | 76.8 | 1.6 | 难溶于水 |
(1)A装置仪器b的名称是
(2)装置A中发生反应的离子方程式为
(3)在通入Cl2前,先打开开关k,从侧管持续通入一段时间的CO2气体的目的是
(4)装置C中除生成TiCl4外,还生成一种气态不成盐氧化物,该反应的化学方程式为:
(5)制得的TiCl4中常含有少量CCl4,从混合液中分离出TiCl4操作的名称是
(6)利用如图装置测定所得TiCl4的纯度:

取wg产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待TiCl4充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴0.1mol·L-1K2CrO4溶液作指示剂,用cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液VmL。已知:常温下Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=1.1×10-12,Ag2CrO4呈砖红色, TiCl4+(2+n)H2O=TiO2·nH2O↓+4HCl
①滴定终点的判断方法是
②产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】亚硝酰氯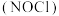 主要用于合成洗涤剂、触媒,也可用作有机合成中间体。沸点为
主要用于合成洗涤剂、触媒,也可用作有机合成中间体。沸点为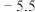 ℃,是黄色气体或红褐色液体,遇水极易反应:
℃,是黄色气体或红褐色液体,遇水极易反应: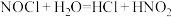 ,伴随着热量的释放。某化学兴趣小组设计如图装置用
,伴随着热量的释放。某化学兴趣小组设计如图装置用 和NO制备亚硝酰氯。
和NO制备亚硝酰氯。
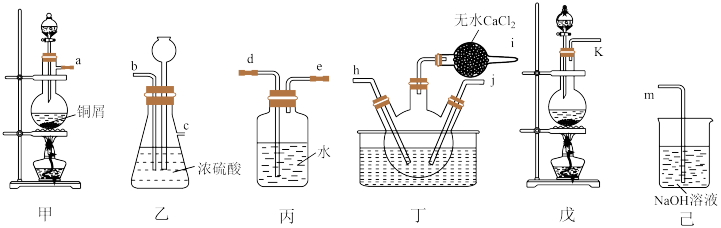
已知:①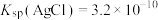 ,
,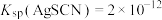 ,
,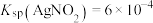 ;
;
②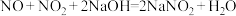 。
。
回答下列问题:
I.制备亚硝酰氯
(1)装置甲中,盛有铜屑的仪器名称为___________ ,用上述装置,按气流方向组装,用字母表示接口的连接顺序为a→___________ →h(i→m)j←___________ ←k(填写接口字母;仪器可重复使用),装置乙的作用是___________ 。
(2)实验开始时,先打开装置甲的分液漏斗活塞滴入适量稀硝酸,当观察到装置丁中___________ 时,再向三颈瓶中通入 制备
制备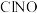 ,当观察到
,当观察到___________ 说明三颈瓶中反应结束。
(3)装置丁中冰盐水的作用是___________ 。
II.产品纯度的测定
实验步骤如下:
①取mg市售亚硝酰氯溶于水,配制成 溶液,取出
溶液,取出 于锥形瓶中;
于锥形瓶中;
②调pH为6,再加入稍过量的 溶液(杂质不参与反应);
溶液(杂质不参与反应);
③充分反应后,加入少量硝基苯,振荡、静置,使沉淀表面被有机物覆盖。
④滴入几滴 溶液,再用
溶液,再用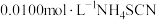 标准溶液滴定,滴定至终点时,共消耗
标准溶液滴定,滴定至终点时,共消耗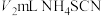 溶液。
溶液。
(4)步骤④中滴定终点的现象是___________ ,市售亚硝酰氯纯度为___________ (用m、 、
、 表示)。
表示)。
(5)下列操作导致测得市售亚硝酰氯纯度偏小的是___________。
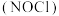 主要用于合成洗涤剂、触媒,也可用作有机合成中间体。沸点为
主要用于合成洗涤剂、触媒,也可用作有机合成中间体。沸点为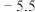 ℃,是黄色气体或红褐色液体,遇水极易反应:
℃,是黄色气体或红褐色液体,遇水极易反应: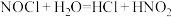 ,伴随着热量的释放。某化学兴趣小组设计如图装置用
,伴随着热量的释放。某化学兴趣小组设计如图装置用 和NO制备亚硝酰氯。
和NO制备亚硝酰氯。
已知:①
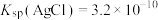 ,
,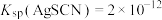 ,
,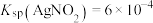 ;
;②
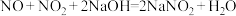 。
。回答下列问题:
I.制备亚硝酰氯
(1)装置甲中,盛有铜屑的仪器名称为
(2)实验开始时,先打开装置甲的分液漏斗活塞滴入适量稀硝酸,当观察到装置丁中
 制备
制备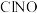 ,当观察到
,当观察到(3)装置丁中冰盐水的作用是
II.产品纯度的测定
实验步骤如下:
①取mg市售亚硝酰氯溶于水,配制成
 溶液,取出
溶液,取出 于锥形瓶中;
于锥形瓶中;②调pH为6,再加入稍过量的
 溶液(杂质不参与反应);
溶液(杂质不参与反应);③充分反应后,加入少量硝基苯,振荡、静置,使沉淀表面被有机物覆盖。
④滴入几滴
 溶液,再用
溶液,再用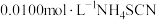 标准溶液滴定,滴定至终点时,共消耗
标准溶液滴定,滴定至终点时,共消耗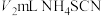 溶液。
溶液。(4)步骤④中滴定终点的现象是
 、
、 表示)。
表示)。(5)下列操作导致测得市售亚硝酰氯纯度偏小的是___________。
A.步骤①中,将 溶解后立即转移至 溶解后立即转移至 容量瓶中 容量瓶中 |
B.步骤②中,有几滴 溶液滴落在锥形瓶外 溶液滴落在锥形瓶外 |
| C.步骤③中,有少量白色沉淀表面没有覆盖有机物 |
| D.步骤④中,滴定终点时,有半滴液体悬挂尖嘴处 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中。KI还可用于分析试剂、感光材料、制药等,其制备原理如下:
反应I:3I2+ 6KOH== KIO3 +5KI+ 3H2O
反应II:3H2S+KIO3=3S↓+KI+ 3H2O
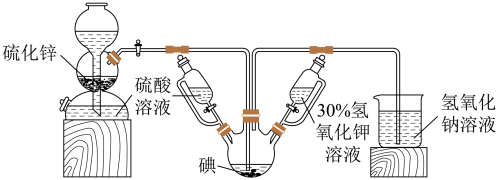
请回答有关问题。
(1)启普发生器中发生反应的化学方程式为________ 。装置中盛装30%氢氧化钾溶液的仪器名称是__________ 。
(2)关闭启普发生器活塞,先滴入30%的KOH溶液.待观察到三颈烧瓶中溶液颜色由棕黄色变为______ (填现象),停止滴入KOH溶液;然后________ (填操作),待三颈烧瓶和烧杯中产生气泡的速率接近相等时停止通气。
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的是_______________ 。
(4)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还含有硫酸钡和____ (填名称)。合并滤液和洗涤液,蒸发至析出结晶,干燥得成品。
(5)实验室模拟工业制备KIO3流程如下:

几种物质的溶解度见下表:
用惰性电极电解KI溶液也能制备KIO3,与电解法相比,上述流程制备KIO3的缺点是_________ 。
(6)某同学测定.上述流程生产的KIO3样品的纯度。
取1.00 g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0 mol·L-1 Na2S2O3溶液,恰好完全反应时共消耗12. 60 mL Na2S2O3溶液。该样品中KIO3的质量分数为___________ (已知反应:I2+2Na2S2O3=2NaI+Na2S4O6)。
反应I:3I2+ 6KOH== KIO3 +5KI+ 3H2O
反应II:3H2S+KIO3=3S↓+KI+ 3H2O

请回答有关问题。
(1)启普发生器中发生反应的化学方程式为
(2)关闭启普发生器活塞,先滴入30%的KOH溶液.待观察到三颈烧瓶中溶液颜色由棕黄色变为
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的是
(4)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还含有硫酸钡和
(5)实验室模拟工业制备KIO3流程如下:

几种物质的溶解度见下表:
| KCl | KH(IO3)2 | KClO3 | |
| 25℃时的溶解度(g) | 20.8 | 0.8 | 7.5 |
| 80℃时的溶解度(g) | 37.1 | 12.4 | 16.2 |
(6)某同学测定.上述流程生产的KIO3样品的纯度。
取1.00 g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0 mol·L-1 Na2S2O3溶液,恰好完全反应时共消耗12. 60 mL Na2S2O3溶液。该样品中KIO3的质量分数为
您最近一年使用:0次



