Pd/A12O3是常见的汽车尾气催化剂。一种从废Pd/A12O3纳米催化剂(主要成分及含量:Pd0.3%,γ-A12O392.8%,其他杂质6.9%)中回收金属Pd的工艺如图:
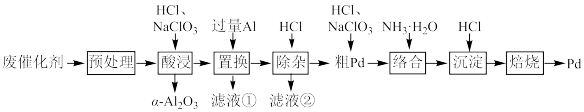
已知:γ-Al2O3能与酸反应,α-A12O3不与酸反应。
回答下列问题:
(1)“预处理”时,γ-A12O3经焙烧转化为α-A12O3,该操作的主要目的是___ 。
(2)“酸浸”时,Pd转化为PdCl ,其离子方程式为
,其离子方程式为___ 。
(3)“滤液①”和“滤液②”中都含有的主要溶质有___ (填化学式)。
(4)“粗Pd”溶解时,可用稀HNO3替代NaClO3,但缺点是___ 。两者相比,___ (填化学式)的氧化效率更高(氧化效率以单位质量得到的电子数表示)。
(5)“沉淀”时,[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,其化学方程式为___ 。
(6)酸性条件下,BrO3-能在负载Pd/A12O3纳米催化剂的电极表面快速转化为Br-。
①发生上述转化反应的电极应接电源的___ 极(填“正”或“负”);
②研究表明,电流密度越大,电催化效率越高;但当电流密度过大时,该电极会发生副反应生成___ (填化学式)。

已知:γ-Al2O3能与酸反应,α-A12O3不与酸反应。
回答下列问题:
(1)“预处理”时,γ-A12O3经焙烧转化为α-A12O3,该操作的主要目的是
(2)“酸浸”时,Pd转化为PdCl
 ,其离子方程式为
,其离子方程式为(3)“滤液①”和“滤液②”中都含有的主要溶质有
(4)“粗Pd”溶解时,可用稀HNO3替代NaClO3,但缺点是
(5)“沉淀”时,[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,其化学方程式为
(6)酸性条件下,BrO3-能在负载Pd/A12O3纳米催化剂的电极表面快速转化为Br-。
①发生上述转化反应的电极应接电源的
②研究表明,电流密度越大,电催化效率越高;但当电流密度过大时,该电极会发生副反应生成
更新时间:2020-07-02 19:47:07
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下其流程图如下:

(1)写出下列B、D所含物质的化学式:固体B____ ; 沉淀D_____ 。
(2)进行操作Ⅰ、Ⅱ、Ⅲ、Ⅳ所用到的玻璃仪器为___________________ ;
(3)写出②、③的反应离子方程式:
②_____________________________________________ 。
③___________________________________________________________________
(4)KAl(SO4)2净水的原因是_____________________________ 。(用离子方程式和必要的文字解释)

(1)写出下列B、D所含物质的化学式:固体B
(2)进行操作Ⅰ、Ⅱ、Ⅲ、Ⅳ所用到的玻璃仪器为
(3)写出②、③的反应离子方程式:
②
③
(4)KAl(SO4)2净水的原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】硝酸铝[Al(NO3)3]是一种常用媒染剂。工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3·9H2O]的流程如下:
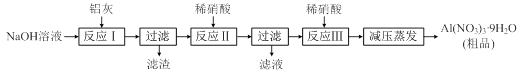
(1)写出反应Ⅰ的离子方程式:_____ (任写一个)。
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是___ ,可采取的措施为_____ 。
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的是_____ 。
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是_____ 。
(5)若用下图所示实验装置制取Al(NO3)3,通入水蒸气的作用是_____ 。


(1)写出反应Ⅰ的离子方程式:
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的是
(4)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是
(5)若用下图所示实验装置制取Al(NO3)3,通入水蒸气的作用是

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】工业上常以铬铁矿(主要成分为亚铬酸亚铁FeCr2O4,还含有Al2O3、SiO2等杂质)为主要原料生产红矾钠(Na2Cr2O7),某实验小组模拟其流程如下图所示:
(1)FeCr2O4中Cr的化合价为____________ ,步骤①焙烧时所用的仪器名称为_________ ;步骤①中生成Na2CrO4的化学方程式为________________________ 。
(2)步骤①煅烧反应极慢,需要升温至纯碱呈熔融状态,反应速率才加快,其主要原因为________ 。
(3)步骤②过滤时所用到的玻璃仪器有________________ ;
(4)涉骤③用硫酸将溶液的pH调至中性,所得滤渣2的主要成分是__________ 、__________ ;
(5)步骤④向滤液2加入硫酸酸化过程中,溶液由黄色变为橙色,反应的离子方程式为___________ 。
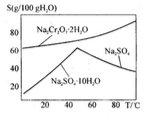
(6)下图是Na2Cr2O7·2H2O和Na2SO4的溶解度曲线,步骤④中获得副产品Na2SO4的实验操作方法为____________________ 。

(1)FeCr2O4中Cr的化合价为
(2)步骤①煅烧反应极慢,需要升温至纯碱呈熔融状态,反应速率才加快,其主要原因为
(3)步骤②过滤时所用到的玻璃仪器有
(4)涉骤③用硫酸将溶液的pH调至中性,所得滤渣2的主要成分是
(5)步骤④向滤液2加入硫酸酸化过程中,溶液由黄色变为橙色,反应的离子方程式为
(6)下图是Na2Cr2O7·2H2O和Na2SO4的溶解度曲线,步骤④中获得副产品Na2SO4的实验操作方法为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】工业用黄铜矿【主要成分CuFeS2(Fe化合价+2),含少量锌、铅的硫化物】冶炼铜的一种方法如图:
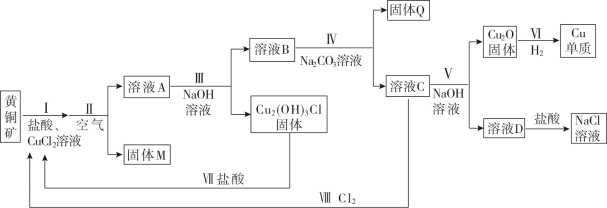
(1)从流程图可以看出,第III步的分离操作是__ 。
(2)完成Ⅰ中发生反应的离子方程式。___ 。
CuFeS2+____Cu2++____ =____CuCl
=____CuCl +Fe2++____S
+Fe2++____S
(3)固体M是S和FeOOH的混合物,写出Ⅱ中通入空气,将FeCl2转化FeOOH沉淀的化学方程式是___ 。
(4)溶液B中含金属元素的离子有:Zn2+、Pb2+和CuCl ,下列说法正确的是
,下列说法正确的是____ 。
(5)反应Ⅵ中用H2将57.6kgCu2O完全还原,若H2的利用率是80%,则需要提供H2的体积是__ m3(标准状况)。
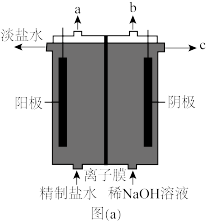
(6)从物质循环利用的角度看,电解NaCl溶液能够很好的服务于该冶炼铜的工艺,分析图(a),结合化学用语说明骤Ⅲ所需原料的生成原理:___ 。

(1)从流程图可以看出,第III步的分离操作是
(2)完成Ⅰ中发生反应的离子方程式。
CuFeS2+____Cu2++____
 =____CuCl
=____CuCl +Fe2++____S
+Fe2++____S(3)固体M是S和FeOOH的混合物,写出Ⅱ中通入空气,将FeCl2转化FeOOH沉淀的化学方程式是
(4)溶液B中含金属元素的离子有:Zn2+、Pb2+和CuCl
 ,下列说法正确的是
,下列说法正确的是| A.Ⅲ中需控制NaOH溶液的用量 |
| B.Ⅳ中加入Na2CO3溶液的目的是除去Zn2+、Pb2+ |
| C.反应Ⅴ发生了氧化还原反应 |
(6)从物质循环利用的角度看,电解NaCl溶液能够很好的服务于该冶炼铜的工艺,分析图(a),结合化学用语说明骤Ⅲ所需原料的生成原理:

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】碳酸镧 为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧
为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧 ,如果溶液碱性太强,易生成受热分解的碱式碳酸镧
,如果溶液碱性太强,易生成受热分解的碱式碳酸镧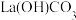 。回答下列问题:
。回答下列问题:
(一)利用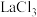 溶液制备水合碳酸澜
溶液制备水合碳酸澜

(1)仪器B的名称为_______ 。
(2)装置接口的连接顺序为f→_______ 。
(3)Z中应先通入_______ (填化学式),后通入过量的另一种气体,该气体需要过量的原因是_______ 。
(4)该反应中生成副产物氯化铵,请写出Z中生成水合碳酸镧的化学方程式:_______ 。
(二) 中x值的测定
中x值的测定
将石英玻璃A管称重,记为 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为 ,将装有试剂的装置C称重,记为
,将装有试剂的装置C称重,记为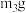 。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
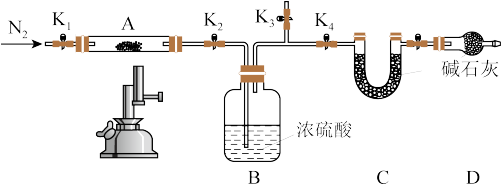
实验步骤如下:
①打开 和
和 ,缓缓通入;
,缓缓通入;
②数分钟后关闭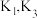 ,打开
,打开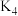 ,点燃酒精喷灯,加热A中样品;
,点燃酒精喷灯,加热A中样品;
③一段时间后,熄灭酒精喷灯,打开 ,通入数分钟后关闭
,通入数分钟后关闭 和
和 ,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为
,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为 (此时装置A中固体为
(此时装置A中固体为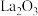 )。称重装置C,记为
)。称重装置C,记为 。
。
(5)实验中第二次通入 的目的为
的目的为_______ 。
(6)根据实验记录,当
_______ ,说明制得的样品中不含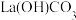 。
。
(7)水合碳酸镧的化学式中x=_________ (用含 的代数式表示,可不化简)。
的代数式表示,可不化简)。
 为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧
为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧 ,如果溶液碱性太强,易生成受热分解的碱式碳酸镧
,如果溶液碱性太强,易生成受热分解的碱式碳酸镧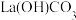 。回答下列问题:
。回答下列问题:(一)利用
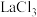 溶液制备水合碳酸澜
溶液制备水合碳酸澜
(1)仪器B的名称为
(2)装置接口的连接顺序为f→
(3)Z中应先通入
(4)该反应中生成副产物氯化铵,请写出Z中生成水合碳酸镧的化学方程式:
(二)
 中x值的测定
中x值的测定将石英玻璃A管称重,记为
 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为 ,将装有试剂的装置C称重,记为
,将装有试剂的装置C称重,记为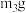 。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
实验步骤如下:
①打开
 和
和 ,缓缓通入;
,缓缓通入;②数分钟后关闭
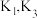 ,打开
,打开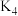 ,点燃酒精喷灯,加热A中样品;
,点燃酒精喷灯,加热A中样品;③一段时间后,熄灭酒精喷灯,打开
 ,通入数分钟后关闭
,通入数分钟后关闭 和
和 ,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为
,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为 (此时装置A中固体为
(此时装置A中固体为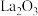 )。称重装置C,记为
)。称重装置C,记为 。
。(5)实验中第二次通入
 的目的为
的目的为(6)根据实验记录,当

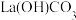 。
。(7)水合碳酸镧的化学式中x=
 的代数式表示,可不化简)。
的代数式表示,可不化简)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】三氯化锑(SbCl3)用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为Sb2S3,还含有As2S3、PbS、CuO和SiO2等)为原料制备SbCl3的工艺流程如图:

已知:① 具有强氧化性,“浸出液”主要含盐酸和:
具有强氧化性,“浸出液”主要含盐酸和: ,还含
,还含 、
、 、
、 和
和 等杂质;
等杂质;
②常温下, ,
,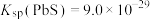 ;
;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
回答下列问题:
(1)Cu位于元素周期表第
(2)“滤渣1”的主要成分有S和
(3)“浸出液”中加入适量Sb的目的是
(4)当
 、
、 共沉淀时,溶液中
共沉淀时,溶液中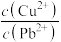 =
=(5)“除砷”时,氧化产物为
 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为(6)已知:“电解”
 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】某化工厂设计用含钴废催化剂(Co、Fe、FeO、Fe2O3以及不溶于酸的杂质)制备氯化钴晶体(CoCl2·6H2O)与新型高效消毒剂高铁酸钾(K2FeO4)的工艺流程如下:
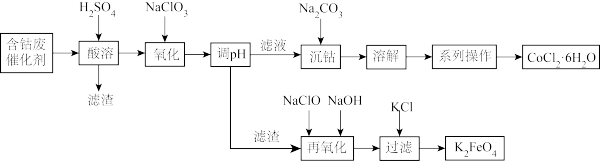
已知:①常温下Fe(OH)3的溶度积为1×10-35,Co(OH)2的溶度积为1.6×10-15
②CoCl2·6H2O呈红色,常温下稳定,易溶于水、乙醇。110-120℃时脱水形成蓝色无水氯化钴。
(1)酸溶时,写出能加快反应速率一种方法:_______ 。
(2)加入氯酸钠氧化的目的是_______ 。
(3)若溶液中Co2+为0.16mol·L-1,则调节pH的范围应为_______ 。
(4)再氧化时,发生反应的化学方程式是_______ 。同条件下溶解度Na2FeO4_______ (填“>”“=”“<”)K2FeO4
(5)得到产品CoCl2·6H2O所进行的一系列操作为_______ 、_______ 、过滤制得CoCl2·6H2O需要减压烘干的原因是_______ 。

已知:①常温下Fe(OH)3的溶度积为1×10-35,Co(OH)2的溶度积为1.6×10-15
②CoCl2·6H2O呈红色,常温下稳定,易溶于水、乙醇。110-120℃时脱水形成蓝色无水氯化钴。
(1)酸溶时,写出能加快反应速率一种方法:
(2)加入氯酸钠氧化的目的是
(3)若溶液中Co2+为0.16mol·L-1,则调节pH的范围应为
(4)再氧化时,发生反应的化学方程式是
(5)得到产品CoCl2·6H2O所进行的一系列操作为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】 可用作电器元件材料,也可作为瓷釉、颜料的制作原料。工业上用酸性含锰废水(主要含
可用作电器元件材料,也可作为瓷釉、颜料的制作原料。工业上用酸性含锰废水(主要含 、
、 、
、 、
、 、
、 )制备
)制备 :
:
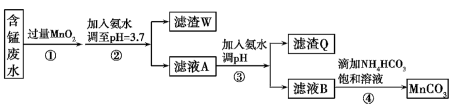
已知:几种金属离子沉淀的pH如下表。
回答下列问题:
(1)①中加入过量 的作用是
的作用是_______ ,滤渣W的成分是_______ 。
(2)过程③中,调pH的目的是_______ 。
(3)过程④中有 生成,则生成
生成,则生成 的离子方程式是
的离子方程式是_______ ,该过程中副产品的化学式是_______ 。
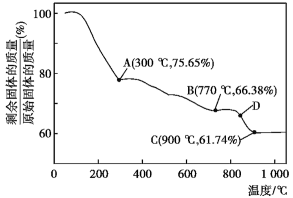
(4) 在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中
在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中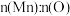 为
为_______ ;图中点D对应固体的成分为_______ (填化学式)。
 可用作电器元件材料,也可作为瓷釉、颜料的制作原料。工业上用酸性含锰废水(主要含
可用作电器元件材料,也可作为瓷釉、颜料的制作原料。工业上用酸性含锰废水(主要含 、
、 、
、 、
、 、
、 )制备
)制备 :
:
已知:几种金属离子沉淀的pH如下表。
金属离子 |
|
|
|
|
开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
完全沉淀的pH | 9.7 | 3.7 | 6.4 | 10.4 |
(1)①中加入过量
 的作用是
的作用是(2)过程③中,调pH的目的是
(3)过程④中有
 生成,则生成
生成,则生成 的离子方程式是
的离子方程式是(4)
 在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中
在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中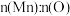 为
为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】过氧化钙(CaO2)微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
I.过氧化钙的制备。流程如下,步骤②的装置示意图为图一:


(1)步骤①将溶液煮沸、过滤。将溶液煮沸的目的是___ 。
(2)图一装置中:①仪器a的名称是___ ;
②反应的化学方程式为___ ;
③该反应需要在冷水浴中进行,原因是___ 。
(3)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是___ 。
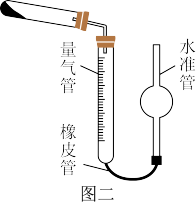
Ⅱ.过氧化钙的测定:已知CaO2在350℃时迅速分解生成CaO和O2。该小组采用如图二所示装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
(1)量气管读数时需注意的项有:①气体冷却到室温;②量气装置两侧液面相平;③___ 。
(2)使用电子天平准确称取0.5000g样品,置于试管中加热使其完全分解,收集到33.60mL(已换算为标准状况)气体,则产品中CaO2的质量分数为___ (保留3位有效数字)。
I.过氧化钙的制备。流程如下,步骤②的装置示意图为图一:



(1)步骤①将溶液煮沸、过滤。将溶液煮沸的目的是
(2)图一装置中:①仪器a的名称是
②反应的化学方程式为
③该反应需要在冷水浴中进行,原因是
(3)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是
Ⅱ.过氧化钙的测定:已知CaO2在350℃时迅速分解生成CaO和O2。该小组采用如图二所示装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
(1)量气管读数时需注意的项有:①气体冷却到室温;②量气装置两侧液面相平;③
(2)使用电子天平准确称取0.5000g样品,置于试管中加热使其完全分解,收集到33.60mL(已换算为标准状况)气体,则产品中CaO2的质量分数为
您最近一年使用:0次




