铁氧体(Fe3O4)法是处理含废铬水的常用方法,其原理是用FeSO4把废水中Cr2O 还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3•FeO)的复合氧化物(
还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3•FeO)的复合氧化物( )。CrxFe2-xO3•FeO处理含1molCr2O
)。CrxFe2-xO3•FeO处理含1molCr2O 废水至少需要加入amolFeSO4•7H2O。下列结论正确的是( )
废水至少需要加入amolFeSO4•7H2O。下列结论正确的是( )
 还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3•FeO)的复合氧化物(
还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3•FeO)的复合氧化物( )。CrxFe2-xO3•FeO处理含1molCr2O
)。CrxFe2-xO3•FeO处理含1molCr2O 废水至少需要加入amolFeSO4•7H2O。下列结论正确的是( )
废水至少需要加入amolFeSO4•7H2O。下列结论正确的是( )| A.x=0.5,a=10 | B.x=1,a=5 | C.x=2,a=l0 | D.x=0.5,a=8 |
更新时间:2020-07-03 12:09:37
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关NaClO和NaCl混合溶液的叙述不正确的是
A.该溶液与 、 、 、 、 可以大量共存 可以大量共存 |
B.该溶液显碱性的原因为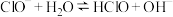 |
C.向该溶液中滴入少量 溶液,反应的离子方程式为: 溶液,反应的离子方程式为: |
D.向该溶液中加入浓盐酸,每产生 ,转移电子约为 ,转移电子约为 个 个 |
您最近一年使用:0次
【推荐2】已知CuO高温灼烧生成Cu2O,Cu2O与稀H2SO4反应的离子方程式为:Cu2O+2H+═Cu+Cu2++H2O。现将经高温灼烧后的CuO样品投入足量稀硫酸中得到混合溶液,有关说法正确的是( )
| A.反应中Cu2O只作氧化剂 |
| B.若有28.8g Cu2O参加反应,则转移电子数为0.2NA |
| C.Cu2O的稳定性比CuO弱 |
| D.如果溶液中出现蓝色,说明CuO已分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用黄铁矿为原料制硫酸产生的硫酸渣(含 、
、 、
、 、MgO等)提取铁红(
、MgO等)提取铁红( )的过程如图所示。下列有关离子反应方程式判断和书写错误的是
)的过程如图所示。下列有关离子反应方程式判断和书写错误的是

 、
、 、
、 、MgO等)提取铁红(
、MgO等)提取铁红( )的过程如图所示。下列有关离子反应方程式判断和书写错误的是
)的过程如图所示。下列有关离子反应方程式判断和书写错误的是
A.酸溶过程中 溶解的离子反应方程式为 溶解的离子反应方程式为 |
B.滤渣A溶解于NaOH溶液的离子方程式为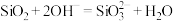 |
C.“还原”过程产物之一为 ,发生的离子反应方程式为 ,发生的离子反应方程式为 |
D.“氧化”过程发生的离子反应方程式为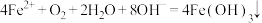 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某化学实验小组在实验室中以含有Zn2+、Al3+、Fe3+、Cu2+、Cl-的废水为原料提取ZnCl2溶液,实验流程如图所示。已知:滤液Ⅰ中存在[Zn(NH3)4]2+、[Cu(NH3)4]2+,滤渣Ⅱ的主要成分为CuS。下列说法错误的是
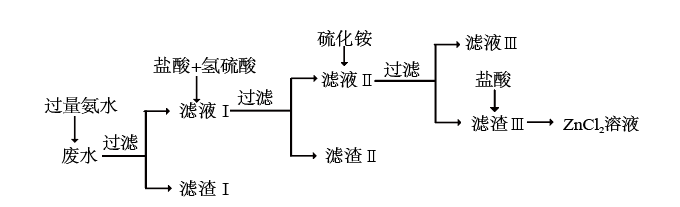

| A.过滤时使用的玻璃仪器有烧杯、漏斗、玻璃棒 |
| B.滤渣Ⅰ的主要成分为氢氧化铁和氢氧化铝 |
| C.滤液Ⅰ、Ⅱ、Ⅲ中均含有氯化铵 |
| D.若直接加热蒸干滤液Ⅱ,可获得纯净的氯化锌 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】垃圾分类,一般是指按一定规定或标准将垃圾分类储存、分类投放和分类搬运,从而转变成公共资源的一系列活动的总称。下列有关垃圾分类说法错误的是
| A.废弃的聚乙烯塑料分类回收之后直接填埋,可以有效减少白色垃圾 |
| B.铝制易拉罐分类回收,可大大节约矿物资源 |
| C.果皮等食品类废物可进行堆肥处理 |
| D.在垃圾分类处理中化学能够发挥重要的作用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学与生活、生产密切相关。下列说法错误的是
| A.用Na2S可除去工业废水中的Cu2+、Hg2+等重金属离子 |
| B.太阳能集水器将空气中水蒸气冷凝成饮用水的过程是放热反应 |
| C.研发新型催化剂,使工业合成氨在温和条件下发生,可降低能耗 |
| D.重视对铅蓄电池、镍镉电池等二次电池的回收,既节省资源又避免污染环境 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】由一种阳离子与两种酸根阴离子组成的盐称为混盐。向混盐 中加入足量稀硫酸,发生反应
中加入足量稀硫酸,发生反应 。下列说法正确的是
。下列说法正确的是
 中加入足量稀硫酸,发生反应
中加入足量稀硫酸,发生反应 。下列说法正确的是
。下列说法正确的是A. 的水溶液与氯化铝溶液混合生成的沉淀是硫化铝 的水溶液与氯化铝溶液混合生成的沉淀是硫化铝 |
B.  中含离子数为 中含离子数为 |
C.上述反应中,每产生 S,转移电子的物质的量为 S,转移电子的物质的量为 |
D. 为混盐,向 为混盐,向 中加入足量稀硫酸会有 中加入足量稀硫酸会有 产生 产生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是
 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是A.反应中作氧化剂的 有 有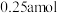 |
B.若反应后溶液中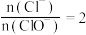 ,则 ,则 |
C. 与 与 的物质的量之和可能为 的物质的量之和可能为 |
D.反应中转移电子的物质的量可能为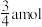 |
您最近一年使用:0次


 和
和

 是一种新型绿色消毒剂,工业上制备高铁酸钠其中一种方法的化学原理为:
是一种新型绿色消毒剂,工业上制备高铁酸钠其中一种方法的化学原理为: ,下列有关说法正确的是
,下列有关说法正确的是 转移3mol电子
转移3mol电子

