含钒石煤(含有铁、硅、铝、钙、镁等元素的氧化物)中的钒大部分是以V(Ⅲ)和V(Ⅳ)形式存在,由含钒石煤提钒的一种工艺流程如下所示:

已知:铜铁试剂能与铜、铁、铝、钛等元素形成不溶于水的配合物。
回答下列问题:
(1)含钒石煤预制时加入复合添加剂对钒浸出率的影响如图所示,其中最佳复合添加剂为______________ 。

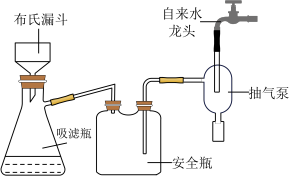
(2)下图为“抽滤”实验原理装置图,“抽滤”时抽气泵的作用是______________ ;
(3)已知酸浸液中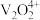 被
被 氧化成
氧化成 ,其离子方程式为
,其离子方程式为___________________ 。“净化除杂”时用铜铁试剂除去所含的 、
、 等杂质离子而不通过调节酸浸液pH的原因是
等杂质离子而不通过调节酸浸液pH的原因是_________________________________________________________ 。
(4)“沉钒”的离子反应方程式为___________________ 。
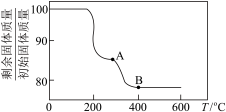
(5)“煅烧”纯净的沉钒产物过程中,固体残留率与温度变化如图所示。已知A点坐标为(260℃,85.47%),则A点对应物质的化学式为________________________ ,B点对应的物质为 ,则B点坐标为
,则B点坐标为________________ 。

已知:铜铁试剂能与铜、铁、铝、钛等元素形成不溶于水的配合物。
回答下列问题:
(1)含钒石煤预制时加入复合添加剂对钒浸出率的影响如图所示,其中最佳复合添加剂为

(2)下图为“抽滤”实验原理装置图,“抽滤”时抽气泵的作用是

(3)已知酸浸液中
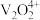 被
被 氧化成
氧化成 ,其离子方程式为
,其离子方程式为 、
、 等杂质离子而不通过调节酸浸液pH的原因是
等杂质离子而不通过调节酸浸液pH的原因是(4)“沉钒”的离子反应方程式为
(5)“煅烧”纯净的沉钒产物过程中,固体残留率与温度变化如图所示。已知A点坐标为(260℃,85.47%),则A点对应物质的化学式为
 ,则B点坐标为
,则B点坐标为
更新时间:2020-07-03 19:21:39
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】羟胺( )在医药、农药等领域应用广泛。回答下列问题:
)在医药、农药等领域应用广泛。回答下列问题:
(1)已知:羟胺在水中主要以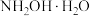 (弱碱)形式存在,电离方式与
(弱碱)形式存在,电离方式与 相似。将羟胺溶液加水稀释,
相似。将羟胺溶液加水稀释, 的值将
的值将___________ (填“增大”、“减小”或“不变”)。
(2)常温下,将0.1 盐酸分别滴入20.00
盐酸分别滴入20.00 0.1
0.1 羟胺溶液和20.00
羟胺溶液和20.00 0.1
0.1
 溶液中,测得溶液
溶液中,测得溶液 [
[ ]随滴入盐酸体积变化如图所示。
]随滴入盐酸体积变化如图所示。
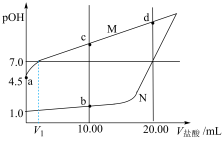
①图中表示盐酸滴定羟胺溶液的曲线是___________ (填“M”或“N”),反应的离子方程式为___________ 。
②常温下,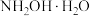 电离平衡常数的值约为
电离平衡常数的值约为___________  ;
;
___________ (保留小数点后2位数)。
③a、b、c、d四点对应的溶液中,水的电离程度由大到小的顺序为___________ 。
④若将b、d点对应的溶液混合,则混合液呈___________ 性,混合液中
___________ 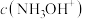 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
 )在医药、农药等领域应用广泛。回答下列问题:
)在医药、农药等领域应用广泛。回答下列问题:(1)已知:羟胺在水中主要以
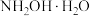 (弱碱)形式存在,电离方式与
(弱碱)形式存在,电离方式与 相似。将羟胺溶液加水稀释,
相似。将羟胺溶液加水稀释, 的值将
的值将(2)常温下,将0.1
 盐酸分别滴入20.00
盐酸分别滴入20.00 0.1
0.1 羟胺溶液和20.00
羟胺溶液和20.00 0.1
0.1
 溶液中,测得溶液
溶液中,测得溶液 [
[ ]随滴入盐酸体积变化如图所示。
]随滴入盐酸体积变化如图所示。
①图中表示盐酸滴定羟胺溶液的曲线是
②常温下,
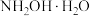 电离平衡常数的值约为
电离平衡常数的值约为 ;
;
③a、b、c、d四点对应的溶液中,水的电离程度由大到小的顺序为
④若将b、d点对应的溶液混合,则混合液呈

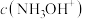 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知镍镉电池的电池总反应为: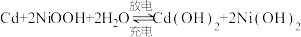 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
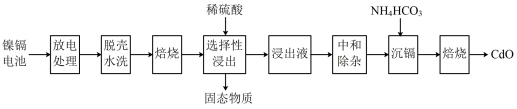
已知:中和除杂后的溶液中主要含有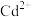 、
、 、
、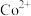 。
。
回答下列问题:
(1)NiOOH中,Ni的化合价为:______ 。
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:______ 。
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:

①“选择性浸出”时,最适宜的pH为______ (填选项字母),写出在此pH下发生的主要离子方程式:______ 。
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:______ 。
表1 浸出液组成
(4)沉铬时生成 的离子反应方程式:
的离子反应方程式:______ 。
(5)镍铬电池充电时, 移向
移向______ (填“明极”或“阳极”),写出阳极的电极反应式:______ 。
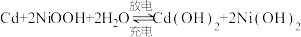 ,利用废旧镍镉电池回收铬的流程如下:
,利用废旧镍镉电池回收铬的流程如下:
已知:中和除杂后的溶液中主要含有
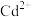 、
、 、
、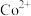 。
。回答下列问题:
(1)NiOOH中,Ni的化合价为:
(2)写出“焙烧”过程中含镍物质变化的化学反应方程式:
(3)在“选择性浸出”一步中,40℃时,不同的金属氧化物在稀
 中2小时后的浸出率随PH的变化如下图1所示,则:
中2小时后的浸出率随PH的变化如下图1所示,则:
①“选择性浸出”时,最适宜的pH为
A.5 B.4 C.3 D.2
②浸出液中各元素含量如表1所示。Co的浓度比镍还小的原因可能是:
| 元素Elements | Cd | Ni | Co | Fe |
浓度(Concentrations/( ) ) | 77.5 | 2.61 | 0.406 | 0.176 |
表1 浸出液组成
(4)沉铬时生成
 的离子反应方程式:
的离子反应方程式:(5)镍铬电池充电时,
 移向
移向
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】 与
与 的氧化性相近。
的氧化性相近。 在自来水消毒和果蔬保鲜等方面应用广泛。某化学兴趣小组通过如图所示装置(夹持装置已略去)对其制备、吸收、释放和应用进行了研究。
在自来水消毒和果蔬保鲜等方面应用广泛。某化学兴趣小组通过如图所示装置(夹持装置已略去)对其制备、吸收、释放和应用进行了研究。

已知:①仪器a中发生的反应为 (未配平);
(未配平);
②仪器b中盛装的粉末的作用是除去生成的 ;
;
③ 被稳定剂完全吸收生成
被稳定剂完全吸收生成 ;
;
④酸性条件下, 可发生反应生成
可发生反应生成 并释放出
并释放出 ;
;
⑤淀粉遇碘会变蓝。
回答下列问题:
(1)仪器a的名称为_______ 。
(2)打开 、关闭
、关闭 ,仪器a中发生反应的离子方程式为
,仪器a中发生反应的离子方程式为_______ 。
(3)一段时间后,关闭 、打开
、打开 ,此时仪器c中释放出的气体为
,此时仪器c中释放出的气体为_______ (填化学名称),仪器d中观察到的现象为_______ 。请写出仪器d中 与
与 发生反应的化学方程式:
发生反应的化学方程式:_______ 。
(4)仪器e中可能发生的反应:
ⅰ.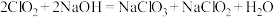 ;
;
ⅱ. 。
。
①反应ⅰ中,氧化产物为_______ (填化学式)。
②若反应ⅰ和ⅱ同时发生,当通入1mol 时,恰好被2L未知浓度的
时,恰好被2L未知浓度的 溶液完全吸收,当此时
溶液完全吸收,当此时 ,则反应后的溶液中
,则反应后的溶液中
_______ (填具体数字) (不考虑气体逸出和溶液体积的变化)。
(不考虑气体逸出和溶液体积的变化)。
 与
与 的氧化性相近。
的氧化性相近。 在自来水消毒和果蔬保鲜等方面应用广泛。某化学兴趣小组通过如图所示装置(夹持装置已略去)对其制备、吸收、释放和应用进行了研究。
在自来水消毒和果蔬保鲜等方面应用广泛。某化学兴趣小组通过如图所示装置(夹持装置已略去)对其制备、吸收、释放和应用进行了研究。
已知:①仪器a中发生的反应为
 (未配平);
(未配平);②仪器b中盛装的粉末的作用是除去生成的
 ;
;③
 被稳定剂完全吸收生成
被稳定剂完全吸收生成 ;
;④酸性条件下,
 可发生反应生成
可发生反应生成 并释放出
并释放出 ;
;⑤淀粉遇碘会变蓝。
回答下列问题:
(1)仪器a的名称为
(2)打开
 、关闭
、关闭 ,仪器a中发生反应的离子方程式为
,仪器a中发生反应的离子方程式为(3)一段时间后,关闭
 、打开
、打开 ,此时仪器c中释放出的气体为
,此时仪器c中释放出的气体为 与
与 发生反应的化学方程式:
发生反应的化学方程式:(4)仪器e中可能发生的反应:
ⅰ.
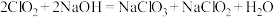 ;
;ⅱ.
 。
。①反应ⅰ中,氧化产物为
②若反应ⅰ和ⅱ同时发生,当通入1mol
 时,恰好被2L未知浓度的
时,恰好被2L未知浓度的 溶液完全吸收,当此时
溶液完全吸收,当此时 ,则反应后的溶液中
,则反应后的溶液中
 (不考虑气体逸出和溶液体积的变化)。
(不考虑气体逸出和溶液体积的变化)。
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某铜合金中 的质量分数为80%~90%,还含有
的质量分数为80%~90%,还含有 等。通常用间接碘量法测定其中
等。通常用间接碘量法测定其中 的含量,步骤如下:
的含量,步骤如下:
1.称取 样品,加入稀
样品,加入稀 和
和 溶液使其溶解,煮沸除去过量的
溶液使其溶解,煮沸除去过量的 ,冷却后过滤,将滤液配制成
,冷却后过滤,将滤液配制成 溶液;
溶液;
Ⅱ.取 滤液于锥形瓶中,加入
滤液于锥形瓶中,加入 溶液,将溶液中的
溶液,将溶液中的 转化为无色稳定的
转化为无色稳定的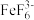 ,充分反应后,加入过量的
,充分反应后,加入过量的 溶液,生成白色沉淀,加入淀粉做指示剂;
溶液,生成白色沉淀,加入淀粉做指示剂;
Ⅲ.向Ⅱ的锥形瓶中加入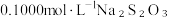 溶液滴定,发生反应:
溶液滴定,发生反应:
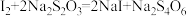 (无色);
(无色);
Ⅳ.平行测定四次,四次滴定实验消耗 标准溶液体积读数如下表所示:
标准溶液体积读数如下表所示:
V.计算铜的质量分数。
已知: 为白色难溶于水的难溶物。
为白色难溶于水的难溶物。
(1)盛装 溶液,应选择下图中的
溶液,应选择下图中的_____________ (填“a”或“b”)。

(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):_______
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.烘干 B.装入滴定液至零刻度以上 C.调整滴定液液面至零刻度或零刻度以下 D.用量筒量取一定体积的溶液倒入锥形瓶中 E.排除气泡 F.用滴定液润洗2至3次G记录起始读数
(3)Ⅱ中 和
和 反应生成
反应生成 白色沉淀和
白色沉淀和 。
。 和
和 反应的离子方程式是
反应的离子方程式是_____________ 。
(4)滴定终点的现象_____________ 。
(5)Ⅳ所消耗的 标准溶液平均体积为
标准溶液平均体积为_____________  ,V计算得到样品中
,V计算得到样品中 的质量分数为
的质量分数为_____________ (结果保留两位小数)。
(6)以下操作造成铜的含量偏高的是_____________ 。
A.滴定管未用标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
F.步骤Ⅱ中未加入 溶液
溶液
 的质量分数为80%~90%,还含有
的质量分数为80%~90%,还含有 等。通常用间接碘量法测定其中
等。通常用间接碘量法测定其中 的含量,步骤如下:
的含量,步骤如下:1.称取
 样品,加入稀
样品,加入稀 和
和 溶液使其溶解,煮沸除去过量的
溶液使其溶解,煮沸除去过量的 ,冷却后过滤,将滤液配制成
,冷却后过滤,将滤液配制成 溶液;
溶液;Ⅱ.取
 滤液于锥形瓶中,加入
滤液于锥形瓶中,加入 溶液,将溶液中的
溶液,将溶液中的 转化为无色稳定的
转化为无色稳定的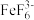 ,充分反应后,加入过量的
,充分反应后,加入过量的 溶液,生成白色沉淀,加入淀粉做指示剂;
溶液,生成白色沉淀,加入淀粉做指示剂;Ⅲ.向Ⅱ的锥形瓶中加入
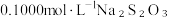 溶液滴定,发生反应:
溶液滴定,发生反应: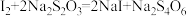 (无色);
(无色);Ⅳ.平行测定四次,四次滴定实验消耗
 标准溶液体积读数如下表所示:
标准溶液体积读数如下表所示:| 滴定次数 | 待测溶液的体积/ |  溶液的体积/ 溶液的体积/ | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 50.00 | 0.00 | 18.02 |
| 第二次 | 50.00 | 0.56 | 18.96 |
| 第三次 | 50.00 | 0.22 | 18.20 |
| 第四次 | 50.00 | 0.35 | 18.35 |
已知:
 为白色难溶于水的难溶物。
为白色难溶于水的难溶物。(1)盛装
 溶液,应选择下图中的
溶液,应选择下图中的
(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→→→→→→开始滴定。
A.烘干 B.装入滴定液至零刻度以上 C.调整滴定液液面至零刻度或零刻度以下 D.用量筒量取一定体积的溶液倒入锥形瓶中 E.排除气泡 F.用滴定液润洗2至3次G记录起始读数
(3)Ⅱ中
 和
和 反应生成
反应生成 白色沉淀和
白色沉淀和 。
。 和
和 反应的离子方程式是
反应的离子方程式是(4)滴定终点的现象
(5)Ⅳ所消耗的
 标准溶液平均体积为
标准溶液平均体积为 ,V计算得到样品中
,V计算得到样品中 的质量分数为
的质量分数为(6)以下操作造成铜的含量偏高的是
A.滴定管未用标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
F.步骤Ⅱ中未加入
 溶液
溶液
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】为了防控疫情,学校要定时进行消毒。
Ⅰ、工业上使用氯气与氢氧化钠反应制取“84消毒液”
(1)其有效成分是___________ (填化学式)。
(2)“84消毒液”使用时应按比例稀释,放置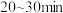 ,放置过程中生成碳酸氢钠,该反应的离子方程式为:
,放置过程中生成碳酸氢钠,该反应的离子方程式为:___________ 。
Ⅱ、“消毒液”中氯元素的存在形态与溶液的关系如表:
(3)请你写出 降低时产生氯气的离子方程式:
降低时产生氯气的离子方程式:___________ 。
Ⅲ、同学猜测“84消毒液”(以下简称“84”)可漂白米醋,进行了如下实验:
(4)实验二的目的是:①___________ ;②___________ 。
(5)结合反应的方程式,解释实验一立即褪色的原因:___________ 。
Ⅳ、 一种常用的自来水消毒剂,某研究小组用如图装置制备少量
一种常用的自来水消毒剂,某研究小组用如图装置制备少量 (夹持装置已略去)。
(夹持装置已略去)。
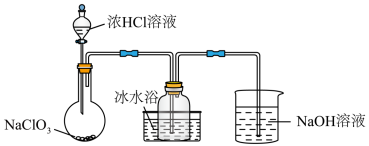
资料: 常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,
常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色, 时液化成红棕色液体。制备
时液化成红棕色液体。制备 的化学反应方程式为
的化学反应方程式为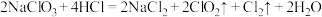
(6)装置中,冰水浴的作用是___________ 。
(7) 中
中 的化合价是
的化合价是___________ 。现有含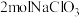 的溶液与足量浓
的溶液与足量浓 反应,可获得
反应,可获得 的质量为
的质量为___________ g。
Ⅰ、工业上使用氯气与氢氧化钠反应制取“84消毒液”
(1)其有效成分是
(2)“84消毒液”使用时应按比例稀释,放置
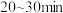 ,放置过程中生成碳酸氢钠,该反应的离子方程式为:
,放置过程中生成碳酸氢钠,该反应的离子方程式为:Ⅱ、“消毒液”中氯元素的存在形态与溶液的关系如表:
溶液 | >9 | 5~6 | 4~5 | 2~3 | <2 |
| 主要成分 |  |  与 与 (少量) (少量) |  与 与 (少量) (少量) |  与 与 |  |
 降低时产生氯气的离子方程式:
降低时产生氯气的离子方程式:Ⅲ、同学猜测“84消毒液”(以下简称“84”)可漂白米醋,进行了如下实验:
| 编号 | 实验操作 | 实验现象 |
| 实验一 | 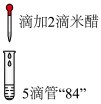 | 滴入米醋后立即褪色,闻到刺激性气味 |
| 实验二 | 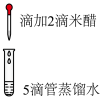 | 溶液为浅棕色,无刺激性气味 |
(5)结合反应的方程式,解释实验一立即褪色的原因:
Ⅳ、
 一种常用的自来水消毒剂,某研究小组用如图装置制备少量
一种常用的自来水消毒剂,某研究小组用如图装置制备少量 (夹持装置已略去)。
(夹持装置已略去)。
资料:
 常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,
常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色, 时液化成红棕色液体。制备
时液化成红棕色液体。制备 的化学反应方程式为
的化学反应方程式为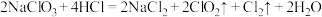
(6)装置中,冰水浴的作用是
(7)
 中
中 的化合价是
的化合价是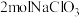 的溶液与足量浓
的溶液与足量浓 反应,可获得
反应,可获得 的质量为
的质量为
您最近半年使用:0次
【推荐3】电化学原理被广泛应用于生产、生活的许多方面,利用电解法脱除煤中的含硫物质(主要是FeS2)的原理如图所示。
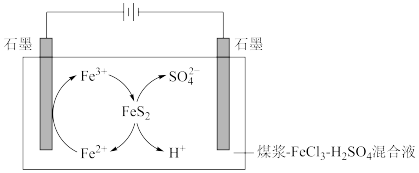
(1)阴极石墨棒上有无色气体产生,该气体是_______ 。
(2)阳极的电极反应式为_______ 。
(3)补全脱硫反应方程式:_______ 。
FeS2+_______+_______=SO +_______+_______
+_______+_______
(4)相同反应时间,FeCl3对脱硫率的影响如图所示。

①电解脱硫过程中,FeCl3的作用是催化剂,结合简单碰撞理论说明使用FeCl3能加快反应速率的原因_______ 。
②FeCl3的质量分数大于1.5%时,脱硫率随FeCl3浓度的增大而下降,解释原因_______ 。
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率η的定义: 。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO
。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO )=0.02mol·L−1,η(SO
)=0.02mol·L−1,η(SO )=
)=_______ (忽略电解前后溶液的体积变化)。
(6)综上,电解法脱硫的优点有_______ (写出两点)。

(1)阴极石墨棒上有无色气体产生,该气体是
(2)阳极的电极反应式为
(3)补全脱硫反应方程式:
FeS2+_______+_______=SO
 +_______+_______
+_______+_______(4)相同反应时间,FeCl3对脱硫率的影响如图所示。

①电解脱硫过程中,FeCl3的作用是催化剂,结合简单碰撞理论说明使用FeCl3能加快反应速率的原因
②FeCl3的质量分数大于1.5%时,脱硫率随FeCl3浓度的增大而下降,解释原因
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率η的定义:
 。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO
。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO )=0.02mol·L−1,η(SO
)=0.02mol·L−1,η(SO )=
)=(6)综上,电解法脱硫的优点有
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】金属锰的用途非常广泛,涉及人类生产生活的方方面面,用含锰废料(主要成分为MnO2,含有少量Al2O3、Fe2O3、MgO、SiO2等)制备锰的流程如下:
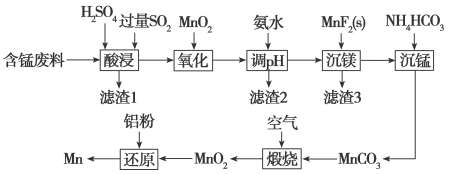
已知:Ⅰ.25 ℃时几种难溶物的溶度积常数见下表:
Ⅱ.当溶液中某离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。
回答下列问题:
(1)基态Mn原子的核外电子排布式为___________ ,Mn2+能形成配离子为八面体的配合物MnCl2·nNH3,在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成1 mol AgCl沉淀,则该配离子化学式为___________ 。比较Fe和Mn的第三电离能,I3(Fe)___________ I3(Mn)(填“大于”或“小于”),原因是___________
(2)“滤渣1”的主要成分为___________ (填化学式)。
(3)写出“酸浸”过程中Fe2O3和SO2反应的化学方程式___________ 。
(4)“氧化”过程中,被MnO2氧化的物质有___________ (写化学式)。
(5)若“调pH”后所得溶液中c(Mn2+)=0.2 mol·L-1,则调pH的范围是4.7≤pH<___________ (保留两位有效数字)。
(6)分别写出“沉镁”和“沉锰”的离子方程式___________ ,___________ 。
(7)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗净的方法是___________ 。

已知:Ⅰ.25 ℃时几种难溶物的溶度积常数见下表:
| 难溶物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 | Mn(OH)2 | MnF2 | MgF2 |
| 溶度积(Ksp) | 2.8×10-39 | 1×10-33 | 5.6×10-12 | 2.0×10-13 | 5.3×10-3 | 5.2×10-11 |
回答下列问题:
(1)基态Mn原子的核外电子排布式为
(2)“滤渣1”的主要成分为
(3)写出“酸浸”过程中Fe2O3和SO2反应的化学方程式
(4)“氧化”过程中,被MnO2氧化的物质有
(5)若“调pH”后所得溶液中c(Mn2+)=0.2 mol·L-1,则调pH的范围是4.7≤pH<
(6)分别写出“沉镁”和“沉锰”的离子方程式
(7)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗净的方法是
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某兴趣小组用废旧干电池(主要含 、炭粉、
、炭粉、 、
、 等)为原料制备硫酸锰铵,同时回收
等)为原料制备硫酸锰铵,同时回收 按如下流程开展了实验:
按如下流程开展了实验:
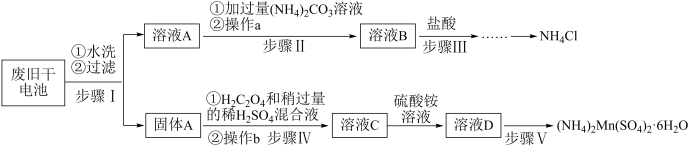
已知:①硫酸锰铵是白色略带粉红色的晶体,易溶于水、不溶于乙醇。
②制备硫酸锰的反应:
③制备硫酸锰铵的反应:
请回答:
(1)下列操作中不正确 的是_______。
(2)步骤III中加盐酸已过量的现象是_______ 。
(3)步骤IV的温度控制在70~80℃的原因是_______ 。推测下列物质可用于代替步骤Ⅳ中草酸的是_______ 。
A.葡萄糖 B.乙酸 C.乙醇 D.亚硫酸钠
(4)步骤Ⅴ为从溶液D中较快得到较纯的硫酸锰铵晶体,请选择下列合理的操作并进行排序→____→____→____→干燥。_______
a.用少量蒸馏水洗涤
b.用少量乙醇溶液洗涤
c.先蒸发浓缩,再改用小火蒸发至出现晶膜
d.直接用小火蒸发至出现晶膜
e.直接用冰水浴冷却
f.先自然冷却至室温,再用冰水浴冷却
g.抽滤
(5)用滴定Mn2+的分析法确定产品中 含量超100%,则
含量超100%,则 产品中可能混有的物质是
产品中可能混有的物质是_______ 。
 、炭粉、
、炭粉、 、
、 等)为原料制备硫酸锰铵,同时回收
等)为原料制备硫酸锰铵,同时回收 按如下流程开展了实验:
按如下流程开展了实验:
已知:①硫酸锰铵是白色略带粉红色的晶体,易溶于水、不溶于乙醇。
②制备硫酸锰的反应:

③制备硫酸锰铵的反应:

请回答:
(1)下列操作中
| A.步骤I用倾析法转移溶液后,洗涤固体A时,注入水并用玻璃棒充分搅拌 |
| B.步骤II中的操作a为萃取分液,步骤Ⅳ中的操作b为趁热过滤 |
C.若步骤IV改为先将固体A在空气中灼烧,然后再将灼烧后产物分批加入到 和 和 的混合液中,则无法制得硫酸锰铵晶体 的混合液中,则无法制得硫酸锰铵晶体 |
D. 反应之所以能进行的原因是相同条件下 反应之所以能进行的原因是相同条件下 的溶解度最小 的溶解度最小 |
(3)步骤IV的温度控制在70~80℃的原因是
A.葡萄糖 B.乙酸 C.乙醇 D.亚硫酸钠
(4)步骤Ⅴ为从溶液D中较快得到较纯的硫酸锰铵晶体,请选择下列合理的操作并进行排序→____→____→____→干燥。
a.用少量蒸馏水洗涤
b.用少量乙醇溶液洗涤
c.先蒸发浓缩,再改用小火蒸发至出现晶膜
d.直接用小火蒸发至出现晶膜
e.直接用冰水浴冷却
f.先自然冷却至室温,再用冰水浴冷却
g.抽滤
(5)用滴定Mn2+的分析法确定产品中
 含量超100%,则
含量超100%,则 产品中可能混有的物质是
产品中可能混有的物质是
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某工厂有废合金(含有铝、铁、铜)粉末,甲同学探索工业废料的利用,用该废合金粉末制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,其实验方案如下:
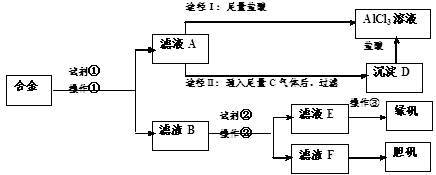
试回答下列问题:
(1)所加试剂①、②分别是____________ 、_____________ 。
(2)操作①的名称为_______ ,所用的仪器除铁架台、铁圈和烧杯,还需要的器材有___________________ 。
(3)由滤液A制AlCl3溶液有途径Ⅰ和途径Ⅱ两种,你认为合理的是__________ ,理由________________ ;
写出A→D反应离子方程式:____________________________ 。
(4)操作③的名称是_________________ 。
(5)丙同学提出可将方案中最初溶解合金的试剂①改为盐酸,重新设计方案,也能得到三种物质,你认为后者的方案比原方案是否更合理:__________ ,理由是___________________________ 。

试回答下列问题:
(1)所加试剂①、②分别是
(2)操作①的名称为
(3)由滤液A制AlCl3溶液有途径Ⅰ和途径Ⅱ两种,你认为合理的是
写出A→D反应离子方程式:
(4)操作③的名称是
(5)丙同学提出可将方案中最初溶解合金的试剂①改为盐酸,重新设计方案,也能得到三种物质,你认为后者的方案比原方案是否更合理:
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是:___________________________ (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为(填代号)___________ 。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
离子方程式为____________ 。
(2)由滤液B制备少量无水AlCl3(AlCl3极易在空气中水解)涉及的操作为:____________ 、冷却结晶、_________ (填操作名称)、洗涤。
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为(填代号)___________ 。
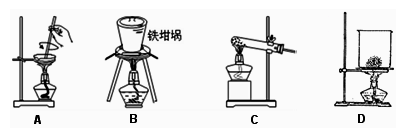
(4)若将铝土矿溶于足量的氢氧化钠溶液,则对应的离子方程式为____________________ 。

(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是:
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为(填代号)
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
离子方程式为
(2)由滤液B制备少量无水AlCl3(AlCl3极易在空气中水解)涉及的操作为:
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为(填代号)

(4)若将铝土矿溶于足量的氢氧化钠溶液,则对应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖,处理废旧的锂离子电池可得到的正极活性粉体中含有Li2O、NiO、 Co2O3、MnO2、Fe、C、Al、 Cu等。采用以下工艺流程可从废旧锂离子电池中分离回收钴、镍、锰,制备正极材料的前驱体(NiCO3·CoCO3· MnCO3)。
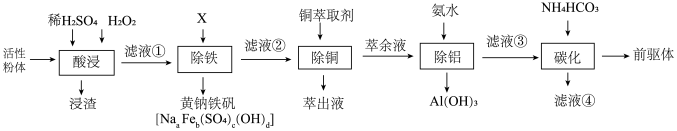
回答下列问题:
(1)“酸浸”温度为85°C,粉体中的钴(以Co2O3表示)还原浸出的离子方程式为___________ ,不能温度过高的原因是___________ 。
(2)“除铁”时需将溶液的pH调至3左右,加入的化合物X的物质名称是___________ 。
(3)“除铜”时获得萃余液的操作名称是___________ 。
(4)“除铝”时反应的离子方程式为___________ 。萃余液中Co2+的浓度为0. 30mol ·L-1,通过计算说明,常温下除铝控制溶液pH为4.0,是否造成Co的损失?___________ 。(列出算式并给出结论)已知: (Ksp[Co (OH)2] =5.9 ×10-15)
(5)碳化时加入NH4HCO3的目的是:___________ 。

回答下列问题:
(1)“酸浸”温度为85°C,粉体中的钴(以Co2O3表示)还原浸出的离子方程式为
(2)“除铁”时需将溶液的pH调至3左右,加入的化合物X的物质名称是
(3)“除铜”时获得萃余液的操作名称是
(4)“除铝”时反应的离子方程式为
(5)碳化时加入NH4HCO3的目的是:
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】Co3O4在磁性材料、电化学领域应用广泛,实验室中可以用CoCO3或CoC2O4煅烧后制得。利用钴渣【含Co(OH)3、Fe(OH)3等】制备钴氧化物的流程如图所示
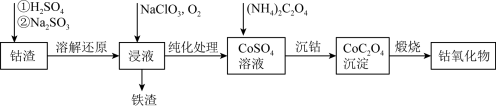
已知: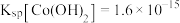 ,
,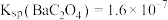 ,
,
 煅烧
煅烧 生成
生成 ,
, 以上生成
以上生成 。
。
(1)“溶解还原”过程中 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“沉钴”时,不能用 溶液代替
溶液代替 溶液,原因是
溶液,原因是___________ 。
(3)检验 固体是否洗净的实验操作是
固体是否洗净的实验操作是___________ 。
(4)为测定草酸钻样品中草酸钴晶体( )的质量分数进行如下实验:
)的质量分数进行如下实验:
①取草酸钴( 摩尔质量为
摩尔质量为 )样品
)样品 ,加入
,加入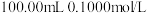 酸性
酸性 溶液,加热(该条件下
溶液,加热(该条件下 不被氧化)。
不被氧化)。
②充分反应后将溶液冷却至室温,加入 容量瓶中,定容。
容量瓶中,定容。
③取 溶液,用
溶液,用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液 。
。
计算样品中草酸钴晶体( )的质量分数:
)的质量分数:___________ 。(写出计算过程)。
(5)以尿素为原料可获得 并制备
并制备 。已知:尿素水溶液在
。已知:尿素水溶液在 以上能缓慢水解产生
以上能缓慢水解产生 ,在
,在 为1~3时水解速率对生成
为1~3时水解速率对生成 沉淀较为适宜。设计以
沉淀较为适宜。设计以 溶液、尿素粉末、盐酸为原料,制备
溶液、尿素粉末、盐酸为原料,制备 的实验方案:取一定体积
的实验方案:取一定体积 溶液,
溶液,___________ 。

已知:
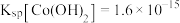 ,
,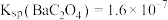 ,
,
 煅烧
煅烧 生成
生成 ,
, 以上生成
以上生成 。
。(1)“溶解还原”过程中
 发生反应的离子方程式为
发生反应的离子方程式为(2)“沉钴”时,不能用
 溶液代替
溶液代替 溶液,原因是
溶液,原因是(3)检验
 固体是否洗净的实验操作是
固体是否洗净的实验操作是(4)为测定草酸钻样品中草酸钴晶体(
 )的质量分数进行如下实验:
)的质量分数进行如下实验:①取草酸钴(
 摩尔质量为
摩尔质量为 )样品
)样品 ,加入
,加入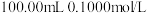 酸性
酸性 溶液,加热(该条件下
溶液,加热(该条件下 不被氧化)。
不被氧化)。②充分反应后将溶液冷却至室温,加入
 容量瓶中,定容。
容量瓶中,定容。③取
 溶液,用
溶液,用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液 。
。计算样品中草酸钴晶体(
 )的质量分数:
)的质量分数:(5)以尿素为原料可获得
 并制备
并制备 。已知:尿素水溶液在
。已知:尿素水溶液在 以上能缓慢水解产生
以上能缓慢水解产生 ,在
,在 为1~3时水解速率对生成
为1~3时水解速率对生成 沉淀较为适宜。设计以
沉淀较为适宜。设计以 溶液、尿素粉末、盐酸为原料,制备
溶液、尿素粉末、盐酸为原料,制备 的实验方案:取一定体积
的实验方案:取一定体积 溶液,
溶液,
您最近半年使用:0次



