题型:解答题-结构与性质
难度:0.65
引用次数:93
题号:10509988
化学上常利用周期表中同族元素的相似性与递变性研究元素的原子结构和性质。回答下列问题:
(1)现代化学中,常利用_____ 特征谱线来鉴定元素。
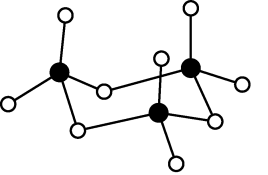
(2)氧族元素中,氧、硫、硒三元素的第一电离能由大到小的顺序为_____ (用元素符号回答),气态SO3为单分子状态,其分子空间构型为_____ 。若SO3的三聚体(SO3)3的环状结构如图所示,则该结构中S原子的杂化轨道类型为_____ 。
(3)卤族元素的氢化物中,H﹣F键的键能>H﹣Cl键的键能>H﹣Br键的键能,原因是_____ 。
(4)铁、钴、镍同处在元素周期表中_____ 族,它们的阳离子易形成各种配合物,已知:磁矩u= ,n为中心原子或离子的单电子数,实验测得配合物[Co(NH3)4Cl2]Cl中u=0,则其中心粒子的化合价为
,n为中心原子或离子的单电子数,实验测得配合物[Co(NH3)4Cl2]Cl中u=0,则其中心粒子的化合价为_____ ,其价电子排布图为_____ 。
(5)已知:铜晶体为面心立方最密堆积,铜原子半径为rpm,阿伏加 德罗常数用NA表示,则铜晶体密度的计算式为_____ 。
(1)现代化学中,常利用
(2)氧族元素中,氧、硫、硒三元素的第一电离能由大到小的顺序为
(3)卤族元素的氢化物中,H﹣F键的键能>H﹣Cl键的键能>H﹣Br键的键能,原因是
(4)铁、钴、镍同处在元素周期表中
 ,n为中心原子或离子的单电子数,实验测得配合物[Co(NH3)4Cl2]Cl中u=0,则其中心粒子的化合价为
,n为中心原子或离子的单电子数,实验测得配合物[Co(NH3)4Cl2]Cl中u=0,则其中心粒子的化合价为(5)已知:铜晶体为面心立方最密堆积,铜原子半径为rpm,阿伏加 德罗常数用NA表示,则铜晶体密度的计算式为

更新时间:2020/06/03 21:37:44
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】碳和硅是自然界中大量存在的元素,硅及其化合物是工业上最重要的材料。设NA代表阿伏加德罗常数的值。粗硅的制备方法有两种:
方法一:
方法二:
(1)基态Si原子中存在_______ 对自旋状态相反的电子,基态Mg原子的最外层电子的电子云轮廓图是_______ 。
(2)上述2个反应中,涉及的所有元素中第一电离能最小的_______ (填元素符号)。
(3)C (金刚石)、晶体硅、CO三种晶体的熔点由高到低的顺序_______ ,其原因是_______ 。
(4)CO在配合物中可作为配体,在 配合物中配位原子是
配合物中配位原子是_______ (填元素符号),1 mol该配合物中含有π键的数目是_______ 。
(5)SiO2晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si键中间插入O原子而形成。
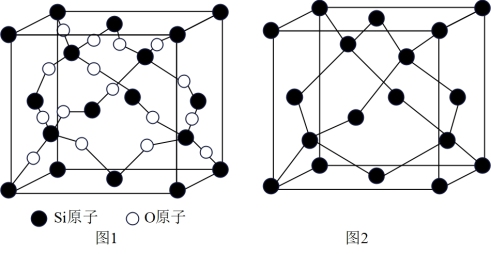
①SiO2晶胞中Si采取_______ 杂化,含有_______ 个O原子。
②SiO2晶胞中假设金刚石晶胞的边长为a pm,试计算该晶胞的密度_______  (写出表达式即可)
(写出表达式即可)
方法一:

方法二:

(1)基态Si原子中存在
(2)上述2个反应中,涉及的所有元素中第一电离能最小的
(3)C (金刚石)、晶体硅、CO三种晶体的熔点由高到低的顺序
(4)CO在配合物中可作为配体,在
 配合物中配位原子是
配合物中配位原子是(5)SiO2晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si键中间插入O原子而形成。

①SiO2晶胞中Si采取
②SiO2晶胞中假设金刚石晶胞的边长为a pm,试计算该晶胞的密度
 (写出表达式即可)
(写出表达式即可)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁及其化合物在化工、医药、材料等领域具有广泛应用,回答下列问题:
(1)Fe元素位于元素周期表的____ 区,与Fe同周期的所有元素的基态原子中,未成对电子数与Fe3+相同的元素有____ 种。
(2)FeCl3蒸汽状态下以双聚分子(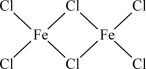 )形式存在,FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是
)形式存在,FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是____ ;FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+,结构如图所示。在该双核阳离子中,H—O—H键角____ (填“大于”、“小于”或“等于”)H2O的H—O—H键角;若对FeCl3水溶液进行加热,该对核阳离子内部首先断开的是____ 键(填“a”或“b”)。____ ,K4[Fe(CN)6]中存在____ (填代号)。
a.离子键 b.氢键 c.配位键 d.金属键
(4)Fe4N的晶胞沿x、y、z轴投影均如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(4-n)CunN,Fe4N转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为____ ;Fe4N晶胞中与N最近的Fe原子数为____ ;Fe与Fe之间的最短距离为____ cm。
(1)Fe元素位于元素周期表的
(2)FeCl3蒸汽状态下以双聚分子(
 )形式存在,FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是
)形式存在,FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是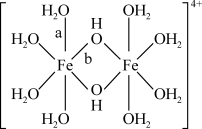
a.离子键 b.氢键 c.配位键 d.金属键
(4)Fe4N的晶胞沿x、y、z轴投影均如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(4-n)CunN,Fe4N转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某油脂厂废弃的油脂加氢镍催化剂的主要成分为Ni,还含有一定量Al、Fe及氧化铁、少量其他不溶性物质,回收废镍催化剂制备硫酸镍晶体( )的工艺流程如下:
)的工艺流程如下:
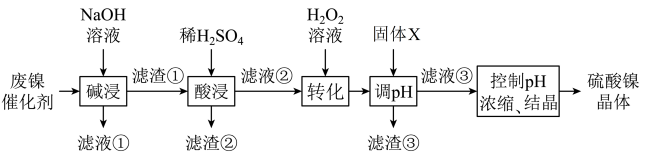
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)下列状态的Ni微粒中,电离最外层一个电子所需能量最大的是_______(填标号)。
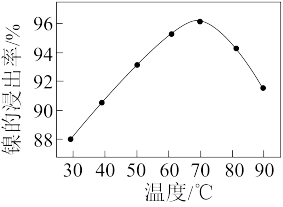
(2)“碱浸”中NaOH溶液的两个作用分别是_______ 。如图是“酸浸”时镍的浸出率与温度的关系,则酸浸时合适的浸出温度是_______ ℃。
(3)为回收金属,向“滤液①”中通入过量二氧化碳气体,反应的离子方程式为_______ 。
(4)“转化”步骤中反应的离子方程式是_____ 。“调pH”时,最适宜的pH范围是______ 。
(5)Ni可以形成多种多样的配合物。 、
、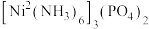 是镍的两种配合物,这两种配合物都存在的作用力是
是镍的两种配合物,这两种配合物都存在的作用力是_______ (填标号)。
a.范德华力 b.配位键 c.极性键 d.离子键 e.氢键 f.非极性键
(6) 中阴离子的空间构型为
中阴离子的空间构型为_______ 。
 )的工艺流程如下:
)的工艺流程如下:
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |
开始沉淀的pH( ) ) | 2.2 | 7.5 | 7.2 |
沉淀完全的pH( ) ) | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)下列状态的Ni微粒中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. | B.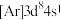 | C.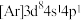 | D. |

(3)为回收金属,向“滤液①”中通入过量二氧化碳气体,反应的离子方程式为
(4)“转化”步骤中反应的离子方程式是
(5)Ni可以形成多种多样的配合物。
 、
、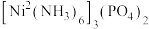 是镍的两种配合物,这两种配合物都存在的作用力是
是镍的两种配合物,这两种配合物都存在的作用力是a.范德华力 b.配位键 c.极性键 d.离子键 e.氢键 f.非极性键
(6)
 中阴离子的空间构型为
中阴离子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钕铁硼磁铁是最常使用的稀土磁铁,被广泛应用于电子产品中。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其他物质。请回答下列问题:
(1)钕(Nd)为60号元素,在元素周期表中位于第____ 周期;基态Fe2+外围电子的轨道表达式为_____________ 。
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。
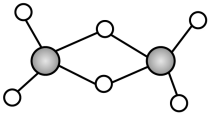
①该分子中Al原子采取______ 杂化。
②Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[Al(OH)4]-中存在的化学键有____ (填标号)。
A.离子键 B.极性共价键 C.金属键 D.非极性共价键 E.氢键
(3)FeO是离子晶体,其晶格能可通过如下的Born﹣Haber循环计算得到。
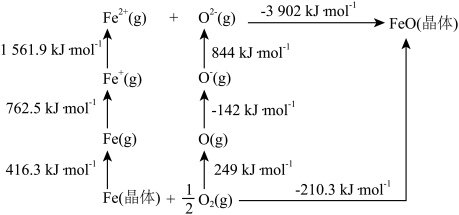
基态Fe原子的第一电离能为___ kJ·mol-1,FeO的晶格能为___ kJ·mol-1。
(4)因材料中含有大量的钕和铁,容易锈蚀是钕铁硼磁铁的一大弱点,可通过电镀镍(Ni)等进行表面涂层处理。已知Ni可以形成化合物四羰基镍[Ni(CO)4],其为无色易挥发剧毒液体,熔点为-25 ℃,沸点为43 ℃,不溶于水,易溶于乙醇、苯、四氯化碳等有机溶剂,四羰基镍的晶体类型是_______ ,写出与配体互为等电子体的分子和离子的化学式为_____ 、_____ (各写一种)。
(5)已知立方BN晶体硬度很大,其原因是________ ;其晶胞结构如图所示,设晶胞中最近的B、N原子之间的距离为a nm,阿伏加 德罗常数的值为NA,则晶体的密度为_____ g·cm-3(列式即可,用含a、NA的代数式表示)。
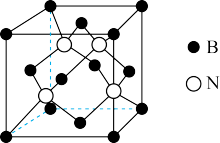
(1)钕(Nd)为60号元素,在元素周期表中位于第
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。

①该分子中Al原子采取
②Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[Al(OH)4]-中存在的化学键有
A.离子键 B.极性共价键 C.金属键 D.非极性共价键 E.氢键
(3)FeO是离子晶体,其晶格能可通过如下的Born﹣Haber循环计算得到。

基态Fe原子的第一电离能为
(4)因材料中含有大量的钕和铁,容易锈蚀是钕铁硼磁铁的一大弱点,可通过电镀镍(Ni)等进行表面涂层处理。已知Ni可以形成化合物四羰基镍[Ni(CO)4],其为无色易挥发剧毒液体,熔点为-25 ℃,沸点为43 ℃,不溶于水,易溶于乙醇、苯、四氯化碳等有机溶剂,四羰基镍的晶体类型是
(5)已知立方BN晶体硬度很大,其原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】镍铜合金是由60%镍、33%铜、7%铁三种金属组成的合金材料。镍铜合金有较好的室温力学性能和高温强度,耐蚀性强,耐磨性好,容易加工,可作为航空发动机的结构材料。根据所学知识,回答下列问题:
(1)Ni原子位于元素周期表中的__________ 区,基态Ni最高能层电子的电子云轮廓图为________ 形。与Ni同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为__________ 。
(2)Cu与Fe的第二电离能分别为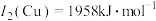 ,
,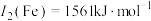 ,
,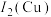 大于
大于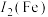 的主要原因是
的主要原因是__________ 。
(3)已知Cu2O的立方晶胞结构如图所示。

①已知a、b的坐标参数依次为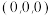 、
、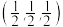 ,则d的坐标参数为
,则d的坐标参数为__________ 。
②晶胞边长为cpm,该晶体的密度为___________ g·cm-3。(列计算式,设 为阿伏加德罗常数的数值)
为阿伏加德罗常数的数值)
(1)Ni原子位于元素周期表中的
(2)Cu与Fe的第二电离能分别为
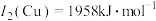 ,
,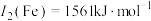 ,
,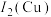 大于
大于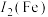 的主要原因是
的主要原因是(3)已知Cu2O的立方晶胞结构如图所示。

①已知a、b的坐标参数依次为
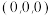 、
、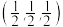 ,则d的坐标参数为
,则d的坐标参数为②晶胞边长为cpm,该晶体的密度为
 为阿伏加德罗常数的数值)
为阿伏加德罗常数的数值)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)SiCl4是生产高纯硅的前驱体,其中Si采取杂化类型为_______ 。SiCl4可发生水解反应,机理如图:
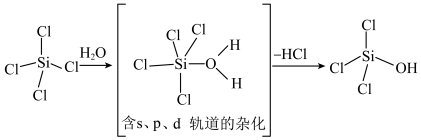
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为_________ (填标号),CO2分子中存在_______ 个σ键和_______ 个π键。
(2)三价铬离子能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(3)[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
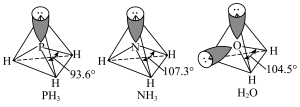
PH3中P的杂化类型是_______ ,H2O的键角小于NH3的,分析原因_______ 。
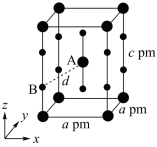
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe-F键长为r pm,则B点原子的分数坐标为
)。已知Xe-F键长为r pm,则B点原子的分数坐标为________ ;晶胞中A、B间距离d=________ pm。
(1)SiCl4是生产高纯硅的前驱体,其中Si采取杂化类型为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)三价铬离子能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中提供电子对形成配位键的原子是
(3)[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。

PH3中P的杂化类型是
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe-F键长为r pm,则B点原子的分数坐标为
)。已知Xe-F键长为r pm,则B点原子的分数坐标为
您最近一年使用:0次



