部分短周期主族元素在周期表中的相对位置如图。
请回答:
(1)上述元素的最高价氧化物的水化物中,碱性最强的化合物的电子式为__ 。
(2)c、d和e 三种简单离子半径由大到小的顺序为________ ( 用离子符号表示)。
(3)单质e与b的简单氢化物反应的化学方程式为________ 。
(4)a和c形成的简单化合物的立体构型为__________ 。
(5)工业上制备单质d的化学方程式为____________ 。
| a | b | c | ||||
| d | e | f |
(1)上述元素的最高价氧化物的水化物中,碱性最强的化合物的电子式为
(2)c、d和e 三种简单离子半径由大到小的顺序为
(3)单质e与b的简单氢化物反应的化学方程式为
(4)a和c形成的简单化合物的立体构型为
(5)工业上制备单质d的化学方程式为
更新时间:2020-07-22 20:31:48
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】(I)A、B、C、D、E为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B 在C中充分燃烧能生成其最高价化合物BC2。D+与C2-具有相同的电子数。A在E中燃烧,产物溶于水得到一种强酸。回答下列问题:(1)B在元素周期表中的位置是_______ ,写出一种工业制备单质E方法的离子方程式_______ 。(2)这五种元素两两之间能形成多种化合物,请写出A2C和DA相互反应的化学方程式_______
(II)化合物甲由四种元素组成,撞击甲容易发生爆炸生成三种物质,产物之一是纯净固体单质乙,另两种产物丙和丁是相对分子质量相同的常见气体,其中丁是空气的主要成分之一,3.0g甲发生爆炸反应,生成2.16g乙和标准状况下0.224L丁,其余为丙.回答下列问题:
(1)丁的结构式_____________
(2)甲发生爆炸反应的化学方程式为____________________
(3)已知化合物甲中,有两种元素的化合价为最高正价,另两种元素的化合价为最低负价,
爆炸反应中氧化产物与还原产物的物质的量之比为_____________ .
(II)化合物甲由四种元素组成,撞击甲容易发生爆炸生成三种物质,产物之一是纯净固体单质乙,另两种产物丙和丁是相对分子质量相同的常见气体,其中丁是空气的主要成分之一,3.0g甲发生爆炸反应,生成2.16g乙和标准状况下0.224L丁,其余为丙.回答下列问题:
(1)丁的结构式
(2)甲发生爆炸反应的化学方程式为
(3)已知化合物甲中,有两种元素的化合价为最高正价,另两种元素的化合价为最低负价,
爆炸反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】X、Y、Z均为短周期元素,X元素的气态氢化物的水溶液滴入无色酚酞变红,Y元素的最外层电子数是次外层电子数的2倍,Z元素是短周期元素中原子半径最大的元素(He、Ne、Ar除外)。
(1)写出X的元素符号___________ ,其原子结构示意图为__________________ 。
(2)元素Y的最简单氢化物的化学式___________________ 。
(3)Z元素的最高价氧化物对应的水化物的电子式为_________________________ 。
(4)X元素最高价氧化物对应的水化物与氧化铝反应的离子方程式为_______________ 。
(5)Y元素的最高价氧化物和Z元素的过氧化物发生氧化还原反应的化学方程式为____________________ 。
(6)在2 L密闭容器中进行下列反应:CO2(g)+C(s) 2CO(g) ΔH>0 (吸热),其他条件不变,只改变下列某一反应条件,分析化学反应速率的变化趋势并进行相关计算。
2CO(g) ΔH>0 (吸热),其他条件不变,只改变下列某一反应条件,分析化学反应速率的变化趋势并进行相关计算。
①增加C,化学反应速率_______________ (填“增大”、“减小”或“不变”)
②减小密闭容器的体积,化学反应速率____________ (填“增大”、“减小”或“不变”)
③若起始时将2 mol CO充入容器发生反应,2S后测得CO2为0.6 mol,则2S内CO的平均反应速率为________________ 。
(1)写出X的元素符号
(2)元素Y的最简单氢化物的化学式
(3)Z元素的最高价氧化物对应的水化物的电子式为
(4)X元素最高价氧化物对应的水化物与氧化铝反应的离子方程式为
(5)Y元素的最高价氧化物和Z元素的过氧化物发生氧化还原反应的化学方程式为
(6)在2 L密闭容器中进行下列反应:CO2(g)+C(s)
 2CO(g) ΔH>0 (吸热),其他条件不变,只改变下列某一反应条件,分析化学反应速率的变化趋势并进行相关计算。
2CO(g) ΔH>0 (吸热),其他条件不变,只改变下列某一反应条件,分析化学反应速率的变化趋势并进行相关计算。①增加C,化学反应速率
②减小密闭容器的体积,化学反应速率
③若起始时将2 mol CO充入容器发生反应,2S后测得CO2为0.6 mol,则2S内CO的平均反应速率为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】A、B、C、D、E、F为短周期元素,非金属元素 最外层电子数与其周期数相同,
最外层电子数与其周期数相同, 的最外层电子数是其所在周期数的2倍。
的最外层电子数是其所在周期数的2倍。 在D中充分燃烧能生成其最高价化合物
在D中充分燃烧能生成其最高价化合物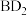 。
。 与
与 具有相同的电子数。
具有相同的电子数。 在
在 中燃烧,产物溶于水得到一种强酸。回答下列问题:
中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)写出一种实验室制备单质 的化学方程式
的化学方程式_______ 。
(2)B、D、E组成的一种盐中, 的质量分数为
的质量分数为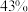 ,其俗名为
,其俗名为_______ ,其水溶液与少量 单质反应的化学方程式为
单质反应的化学方程式为_______ 。
(3)由这些元素组成的物质,其组成和结构信息如下表:
 的化学为
的化学为_______ ; 的化学式为
的化学式为_______  的电子式为
的电子式为_______ 。
(4)由A和B、D元素组成的两种二元化合物(含有两种不同元素)形成一类新能源物质。一种化合物分子通过_______ 构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为_______ 。
 最外层电子数与其周期数相同,
最外层电子数与其周期数相同, 的最外层电子数是其所在周期数的2倍。
的最外层电子数是其所在周期数的2倍。 在D中充分燃烧能生成其最高价化合物
在D中充分燃烧能生成其最高价化合物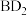 。
。 与
与 具有相同的电子数。
具有相同的电子数。 在
在 中燃烧,产物溶于水得到一种强酸。回答下列问题:
中燃烧,产物溶于水得到一种强酸。回答下列问题:(1)写出一种实验室制备单质
 的化学方程式
的化学方程式(2)B、D、E组成的一种盐中,
 的质量分数为
的质量分数为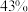 ,其俗名为
,其俗名为 单质反应的化学方程式为
单质反应的化学方程式为(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物 | 组成和结构信息 |
| a | 含有 的由两种元素形成的离子化合物 的由两种元素形成的离子化合物 |
| b | 含有非极性共价键的由两种元素形成的离子化合物,且原子数之比为 |
| c | 化学组成为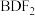 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 的化学为
的化学为 的化学式为
的化学式为 的电子式为
的电子式为(4)由A和B、D元素组成的两种二元化合物(含有两种不同元素)形成一类新能源物质。一种化合物分子通过
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】已知 A、B、C、D、E、F 是六种短周期主族元素,原子序数依次增大。A、C、F 的单质在常温下呈气态,B 的原子最外层电子数是其电子层数的 2 倍,A 与 D 同主族,C 的气态氢化物能与其最高价氧化物的水化物反应,E 是地壳中含量最高的金属元素。清回答下列问题:
(1)F 的元素符号为______ ,B、C、D、E 四种元素原子半径由大到小的顺序是(写元素符号)_____ 。
(2)B 在元素周期表中的位置为_____ ,B 与硫元素形成的二元化合物的电子式为_____ 。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)_____ 。
(4)由 A,C,F 组成的一种常见的盐中结构中包含_____ (选填“离子键”“极性键”和“非极性键”)
(5)单质 B 和元素 C 的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为______ 。
(1)F 的元素符号为
(2)B 在元素周期表中的位置为
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)
(4)由 A,C,F 组成的一种常见的盐中结构中包含
(5)单质 B 和元素 C 的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有7种短周期主族元素,其中元素A、B、C、D原子序数依次减小,该四种元素原子K层电子总数为7,L层电子中总数为22,M层电子总数为12,E与B同主族,F与C同主族,短周期中G的原子半径最大,用化学用语或文字回答下列问题。
(1)A元素在周期表中的位置_____ ,画出B的原子结构示意图_____ 。
(2)A、C、F、G简单离子半径由大到小顺序_____ (用离子符号填写)。
(3)G、C按1∶1形成的化合物含化学键类型_____ ,写出该化合物的电子式_____ 。
(4)下列事实能说明A元素的非金属性比F元素的非金属性强的是____ 。
a.A单质与Na2S溶液反应溶液变混浊
b.F氢化物的酸性比A的氢化物酸性弱
c.A和F两元素的简单氢化物受热分解,前者的分解温度高
(5)在微电子工业中,E的简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为_____ 。
(1)A元素在周期表中的位置
(2)A、C、F、G简单离子半径由大到小顺序
(3)G、C按1∶1形成的化合物含化学键类型
(4)下列事实能说明A元素的非金属性比F元素的非金属性强的是
a.A单质与Na2S溶液反应溶液变混浊
b.F氢化物的酸性比A的氢化物酸性弱
c.A和F两元素的简单氢化物受热分解,前者的分解温度高
(5)在微电子工业中,E的简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】已知:A~H均为短周期元素,它们的最高(或最低)化合价与原子序数的关系如下图。
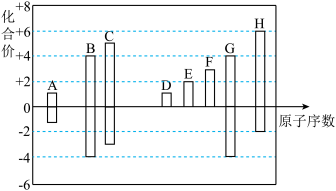
(1)画出F元素的原子结构示意图_______ ,元素H的单质与足量氧气反应的产物为_______ ,元素C、D、H的简单离子的半径由大到小顺序为_______ (用离子符号表示)。
(2)C元素的简单气态氢化物与其最高价氧化物对应的水化物反应生成的化合物与D的最高价氧化物对应的水化物的浓溶液反应的的离子方程式_______ 。G的最高价氧化物与D的最高价氧化物对应的水化物反应的离子方程式_______ 。
(3)C和F组成的化合物FC被大量用于制造电子元件。工业上用F的氧化物、B单质和C单质在高温下制备FC,其中F的氧化物和B单质的物质的量之比为1∶3,则该反应的化学方程式为_______ 。
(4)请写出F的最高价氧化物溶于D的最高价氧化物对应水化物的离子方程式_______ 。
(5)上述三种元素的最高价氧化物的水化物之间两两皆能反应,且三种元素原子的最外层共有9个电子,请指明其中的非金属元素名称为:_______ 。

(1)画出F元素的原子结构示意图
(2)C元素的简单气态氢化物与其最高价氧化物对应的水化物反应生成的化合物与D的最高价氧化物对应的水化物的浓溶液反应的的离子方程式
(3)C和F组成的化合物FC被大量用于制造电子元件。工业上用F的氧化物、B单质和C单质在高温下制备FC,其中F的氧化物和B单质的物质的量之比为1∶3,则该反应的化学方程式为
(4)请写出F的最高价氧化物溶于D的最高价氧化物对应水化物的离子方程式
(5)上述三种元素的最高价氧化物的水化物之间两两皆能反应,且三种元素原子的最外层共有9个电子,请指明其中的非金属元素名称为:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】铁和钴是两种重要的过渡元素。请回答下列问题:
(1)钴在元素周期表中的位置是___________ ,其基态原子的价电子排布图为___________ 。
(2)FeCO3是菱铁矿的主要成分,其中C原子的杂化方式为________ ;分子中的大π键可用符号Π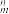 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则CO32-中的大π键应表示为
),则CO32-中的大π键应表示为________ 。
(3)已知Fe2+半径为61pm,Co2+半径为65pm,在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3受热分解温度低于CoCO3,其原因可能是______ 。
(4)Co(NH3)5Cl3是钴的一种配合物,向含0.01mol该配合物的溶液中加入足量AgNO3溶液,生成白色沉淀2.87g。则该配合物的配位数为_____ 。
(5)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构(如图所示),则该晶体中与铁原子距离最近的铁原子数目为___________ ;若该晶胞参数为a pm,则该晶体的密度为___________ g·cm-3(阿伏伽德罗常数的值用NA表示)。

(1)钴在元素周期表中的位置是
(2)FeCO3是菱铁矿的主要成分,其中C原子的杂化方式为
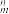 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则CO32-中的大π键应表示为
),则CO32-中的大π键应表示为(3)已知Fe2+半径为61pm,Co2+半径为65pm,在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3受热分解温度低于CoCO3,其原因可能是
(4)Co(NH3)5Cl3是钴的一种配合物,向含0.01mol该配合物的溶液中加入足量AgNO3溶液,生成白色沉淀2.87g。则该配合物的配位数为
(5)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构(如图所示),则该晶体中与铁原子距离最近的铁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】过渡金属( 等)在工业生产中有重要的作用,是化学工作者研究的对象。
等)在工业生产中有重要的作用,是化学工作者研究的对象。
(1) 的结构示意图如图-1所示。
的结构示意图如图-1所示。

①基态 的核外电子排布式为
的核外电子排布式为___________ 。
②图中 与
与 之间形成的化学键称为
之间形成的化学键称为___________ 。
③ 能与
能与 结合成
结合成 ,
, 中的键角
中的键角_______  中的键角(填“>”、“<”或“=”)
中的键角(填“>”、“<”或“=”)
(2)锰元素能形成很多重要的化合物。
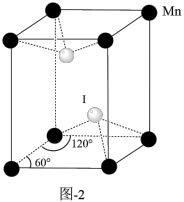
①锰与碘形成的某种化合物的晶胞结构如图-2所示,该化合物的化学式为___________ 。
② 能形成配合物
能形成配合物 ,其配离子的结构如图-3所示(配体位于顶点)。若
,其配离子的结构如图-3所示(配体位于顶点)。若 该配合物与足量
该配合物与足量 反应生成
反应生成 沉淀,则化学式中的n为
沉淀,则化学式中的n为___________ 。

③三醋酸锰由硝酸锰晶体和乙酸酐反应制得。乙酸酐[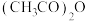 ]可由
]可由 在一定条件下脱水形成,其结构如图-4所示,
在一定条件下脱水形成,其结构如图-4所示, 乙酸酐中所含的
乙酸酐中所含的 键数目为
键数目为___________ 。已知羧酸是一大类含羧基( )的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释
)的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释 的酸性大于
的酸性大于 的原因:
的原因:___________ 。

 等)在工业生产中有重要的作用,是化学工作者研究的对象。
等)在工业生产中有重要的作用,是化学工作者研究的对象。(1)
 的结构示意图如图-1所示。
的结构示意图如图-1所示。
①基态
 的核外电子排布式为
的核外电子排布式为②图中
 与
与 之间形成的化学键称为
之间形成的化学键称为③
 能与
能与 结合成
结合成 ,
, 中的键角
中的键角 中的键角(填“>”、“<”或“=”)
中的键角(填“>”、“<”或“=”)(2)锰元素能形成很多重要的化合物。
①锰与碘形成的某种化合物的晶胞结构如图-2所示,该化合物的化学式为

②
 能形成配合物
能形成配合物 ,其配离子的结构如图-3所示(配体位于顶点)。若
,其配离子的结构如图-3所示(配体位于顶点)。若 该配合物与足量
该配合物与足量 反应生成
反应生成 沉淀,则化学式中的n为
沉淀,则化学式中的n为
③三醋酸锰由硝酸锰晶体和乙酸酐反应制得。乙酸酐[
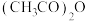 ]可由
]可由 在一定条件下脱水形成,其结构如图-4所示,
在一定条件下脱水形成,其结构如图-4所示, 乙酸酐中所含的
乙酸酐中所含的 键数目为
键数目为 )的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释
)的有机酸,其酸性强弱由羧基中的羟基的极性大小决定。请解释 的酸性大于
的酸性大于 的原因:
的原因:
您最近一年使用:0次
【推荐3】以氮化镓(GaN)为首的第三代半导体材料适合于制作高温、高频、抗辐射及大功率器件,通常也称为高温半导体材料。回答下列问题:
(1)基态Ga原子价层电子的电子排布图为______ ;第二周期中,第一电离能介于N和B之间的元素有______ 种。
(2)HCN分子中σ键与π键的数目之比为______ ,其中σ键的对称方式为______ 。与CN-互为等电子体的一种分子为______ 。
(3)NaN3是汽车安全气囊中的主要化学成分,其中阴离子与CO2互为等电子体,阴离子中心原子的杂化轨道类型为______ 。NF3的空间构型为______ 。
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,分析其变化原因______ 。
(5)GaN晶胞结构如图1所示。已知六棱柱底边边长为a cm,阿伏伽德罗常数的值为NA。
①晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为______ ;
②从GaN晶体中“分割”出的平行六面体如图2。若该平行六面体的体积为 a3cm3,GaN晶体的密度为
a3cm3,GaN晶体的密度为______ g/cm3(用a、NA表示)。
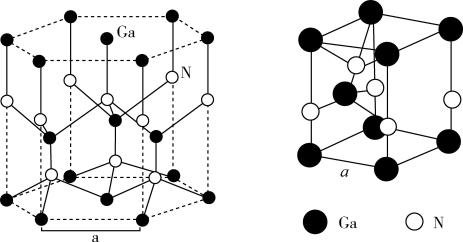
图1 图2
(1)基态Ga原子价层电子的电子排布图为
(2)HCN分子中σ键与π键的数目之比为
(3)NaN3是汽车安全气囊中的主要化学成分,其中阴离子与CO2互为等电子体,阴离子中心原子的杂化轨道类型为
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,分析其变化原因
GaN | GaP | GaAs | |
熔点 | 1700℃ | 1480℃ | 1238℃ |
(5)GaN晶胞结构如图1所示。已知六棱柱底边边长为a cm,阿伏伽德罗常数的值为NA。
①晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为
②从GaN晶体中“分割”出的平行六面体如图2。若该平行六面体的体积为
 a3cm3,GaN晶体的密度为
a3cm3,GaN晶体的密度为
图1 图2
您最近一年使用:0次



