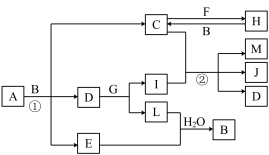
为探究固体化合物X(含四种短周期元素)的组成和性质,设计并完成如下实验 :

已知 :白色固体A是一种优质的耐高温材料;无色溶液D只含一种溶质且为正盐。
请回答:
(1)白色沉淀C的化学式是_________________ 。
(2)白色固体 A →无色溶液 B 的离子方程式是_____________ 。
(3)X 的化学式是______________ 。

已知 :白色固体A是一种优质的耐高温材料;无色溶液D只含一种溶质且为正盐。
请回答:
(1)白色沉淀C的化学式是
(2)白色固体 A →无色溶液 B 的离子方程式是
(3)X 的化学式是
2020高二·浙江·学业考试 查看更多[3]
更新时间:2020-07-24 16:43:10
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
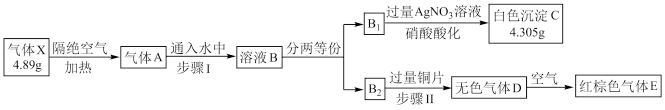
【推荐1】由三种元素组成的化合物X,相对分子质量小于120,按如图流程进行实验。气体A是由红棕色气体E和黄绿色气体F组成的混合物,溶液B是两种强酸的混合物,可被80 mL 1.5 mol·L-1NaOH溶液恰好中和。
请回答:
(1)组成X的三种元素是_______ (填元素符号)。
(2)X的化学式是_______ 。
(3)步骤I发生反应的化学方程式是_______ 。
(4)步骤II发生反应的离子方程式是_______ 。
(5)已知:气体X直接溶于水也可得到溶液B。有文献指出,气体X溶于水得到溶液B的反应分两步进行:第一步生成物之一是具有漂白性的含氧酸,第二步接着反应得到溶液B。写出第一步反应的化学方程式_______ 。

请回答:
(1)组成X的三种元素是
(2)X的化学式是
(3)步骤I发生反应的化学方程式是
(4)步骤II发生反应的离子方程式是
(5)已知:气体X直接溶于水也可得到溶液B。有文献指出,气体X溶于水得到溶液B的反应分两步进行:第一步生成物之一是具有漂白性的含氧酸,第二步接着反应得到溶液B。写出第一步反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略):
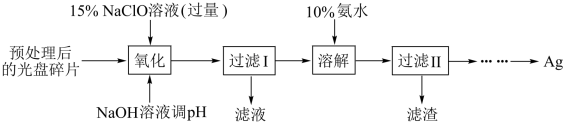
已知:①NaClO溶液与Ag反应的产物为AgCl、NaOH和
②NaClO溶液在受热或酸性条件下易分解: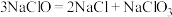
③铜和银是同族相邻元素
请回答下列问题:
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为_____ ;
(2)银元素位于元素周期表的第_____ 周期第_____ 族,属于_____ 区;
(3)“溶解”阶段中发生的反应的离子方程式为_____ ;
(4)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并将洗涤液合并入_____ ;
(5)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为_____ 。

已知:①NaClO溶液与Ag反应的产物为AgCl、NaOH和

②NaClO溶液在受热或酸性条件下易分解:
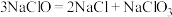
③铜和银是同族相邻元素
请回答下列问题:
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为
(2)银元素位于元素周期表的第
(3)“溶解”阶段中发生的反应的离子方程式为
(4)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并将洗涤液合并入
(5)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与
 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】下列转化关系中,X. Y是生活中用途广泛的两种金属单质,A. B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。

(1)请写出反应①的化学方程式:_________________________________
(2)由D到E的离子方程式:___________________________ 。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:___________________
(4) 0.3 mol Y在高温下与足量的水蒸气充分反应,转移的电子的物质的量为______ mol。
(5)在D和E的混合溶液中,检验其中E的金属阳离子的试剂为______________ 。
(6)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是______________________ 。

(1)请写出反应①的化学方程式:
(2)由D到E的离子方程式:
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:
(4) 0.3 mol Y在高温下与足量的水蒸气充分反应,转移的电子的物质的量为
(5)在D和E的混合溶液中,检验其中E的金属阳离子的试剂为
(6)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol丁分子中不同原子的数目比为1:2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件已略去)。
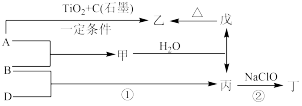
请回答:
(1)写出B单质的电子式___________ 。写出丙的结构式____________ 。
(2)戊与强碱反应的离子方程式:____________________________ 。
(3)丁中所包含的化学键类型有_____________ (填字母序号)。
A.离子键B.极性共价键C.非极性共价键
(4)利用单质B与H2为原料、含H+的固体物质作电解质,在常压下用H2和用He气稀释的单质B分别通入电解池的两极,在570℃时进行反应,反应物转化率高达78%,则生成产物的电极上的电极反应式为_______________________________ ,另一个电极上的电极反应类型是___________ 。
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为:_______________ 。
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为:_________________ 。
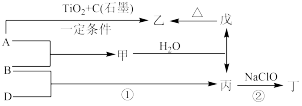
请回答:
(1)写出B单质的电子式
(2)戊与强碱反应的离子方程式:
(3)丁中所包含的化学键类型有
A.离子键B.极性共价键C.非极性共价键
(4)利用单质B与H2为原料、含H+的固体物质作电解质,在常压下用H2和用He气稀释的单质B分别通入电解池的两极,在570℃时进行反应,反应物转化率高达78%,则生成产物的电极上的电极反应式为
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为:
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.某化合物M(仅含三种短周期元素)是一种储氢材料。为探究M的组成和性质,设计并完成如下实验:
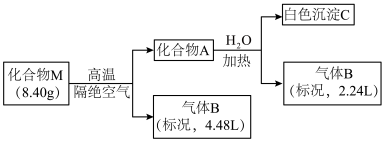
已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是______________ (用元素符号表示)。
(2)化合物A与水反应的化学方程式是______________________ 。
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是______ 。
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为___________________________ 。
(5)X的化学式_____________ 。
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式___________________ 。
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式_____________________ 。
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式________ ,判断该同学设计的验证方法合理性并说明理由_________ 。

已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是
(2)化合物A与水反应的化学方程式是
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为
(5)X的化学式
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】镁菱锌矿(主要成分为ZnCO3、MgCO3等,含有少量FeCO3、CaCO3等杂质)可用于生产媒染剂、防腐剂ZnSO4•7H2O以及耐火材料MgO。制备工艺流程如图:
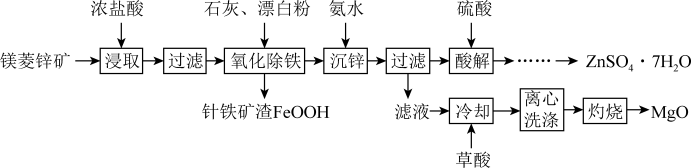
已知:65℃时Ksp[Mg(OH)2]=1.8×10-11;Ksp[Zn(OH)2]=2.0×10-17,Kw=10-13;lg2≈0.3。
回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3:1),目的是_______ ,还可采用_______ (写出一种)等方式达到此目的。
(2)“氧化除铁”在90℃,控制溶液pH在4.0~5.0,得到针铁矿渣的离子方程式为_______ 。
(3)“沉锌”前,滤液(65℃)中含有0.50mol•L-1 Zn2+和1.8mol•L-1 Mg2+,保持该温度,则应加入氨水调节pH在________ 范围(c≤1.0×10-5mol•L-1,沉淀完全)。利用平衡移动原理说明“沉锌”时加入氨水的作用________ 。
(4)“酸解”后获得ZnSO4•7H2O的操作依次经过蒸发浓缩、_______ 、过滤、洗涤、干燥。制得的ZnSO4•7H2O在烘干时需减压烘干的原因是________ 。
(5)“滤液”中加入H2C2O4饱和溶液产生MgC2O4沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:________ 。

已知:65℃时Ksp[Mg(OH)2]=1.8×10-11;Ksp[Zn(OH)2]=2.0×10-17,Kw=10-13;lg2≈0.3。
回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如3:1),目的是
(2)“氧化除铁”在90℃,控制溶液pH在4.0~5.0,得到针铁矿渣的离子方程式为
(3)“沉锌”前,滤液(65℃)中含有0.50mol•L-1 Zn2+和1.8mol•L-1 Mg2+,保持该温度,则应加入氨水调节pH在
(4)“酸解”后获得ZnSO4•7H2O的操作依次经过蒸发浓缩、
(5)“滤液”中加入H2C2O4饱和溶液产生MgC2O4沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】10分)A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空:
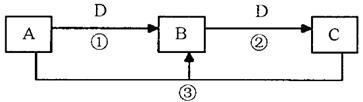
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是_____ ;工业上制取A的离子方程式为_____________ 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为___________________________________________ 。
(3)若D是氯碱工业的主要产品,B有两性,则反应②的离子方程式是__________________ 。
(4)若D是空气质量预报必报的气体,A、B、C的焰色反应都呈黄色,则可以证明B是否变质的一组试剂是________________________________ (请写出试剂名称)。

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
(3)若D是氯碱工业的主要产品,B有两性,则反应②的离子方程式是
(4)若D是空气质量预报必报的气体,A、B、C的焰色反应都呈黄色,则可以证明B是否变质的一组试剂是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】下列表格是元素周期表的一部分。请按要求填空(用化学用语填写)
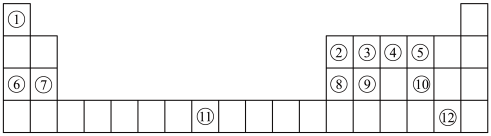
(1)元素①和⑥形成的化合物中存在的化学键类型为_______ 。
(2)用化学方程式表示④的简单氢化物的工业制法_______ 。
(3)写出由③④⑥形成的化合物的电子式_______ 。
(4)列举元素⑨形成的氧化物的一种用途_______ ,元素⑪在周期表中的位置_______ 。
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为_______ 。
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为_______ 。
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为_______ 。

(1)元素①和⑥形成的化合物中存在的化学键类型为
(2)用化学方程式表示④的简单氢化物的工业制法
(3)写出由③④⑥形成的化合物的电子式
(4)列举元素⑨形成的氧化物的一种用途
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol
 ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】I.氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式___________ 。
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为___________ 。
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是___________ ,其中 H2S在该反应中___________ (填序号)。
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是___________ (填“还原性”或“氧化性”)。
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:___________ 。
(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式___________ 。
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是___________ 。
(8)比较④与⑨的简单气态氢化物的稳定性___________ >___________ (填化学式)。
(9)由下列元素形成的化合物中含有离子键的是___________。
(10)写出⑤在空气中燃烧产物的电子式:___________ 。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:

(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是
(8)比较④与⑨的简单气态氢化物的稳定性
(9)由下列元素形成的化合物中含有离子键的是___________。
| A.①③ | B.②③ | C.①④ | D.⑥⑨ |
您最近一年使用:0次