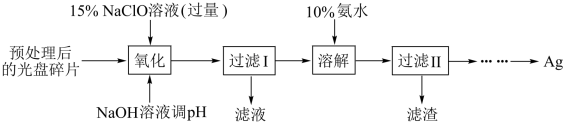
某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略):
已知:①NaClO溶液与Ag反应的产物为AgCl、NaOH和
②NaClO溶液在受热或酸性条件下易分解: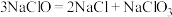
③铜和银是同族相邻元素
请回答下列问题:
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为_____ ;
(2)银元素位于元素周期表的第_____ 周期第_____ 族,属于_____ 区;
(3)“溶解”阶段中发生的反应的离子方程式为_____ ;
(4)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并将洗涤液合并入_____ ;
(5)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为_____ 。

已知:①NaClO溶液与Ag反应的产物为AgCl、NaOH和

②NaClO溶液在受热或酸性条件下易分解:
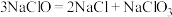
③铜和银是同族相邻元素
请回答下列问题:
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为
(2)银元素位于元素周期表的第
(3)“溶解”阶段中发生的反应的离子方程式为
(4)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并将洗涤液合并入
(5)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与
 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为
更新时间:2023-07-14 07:23:25
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
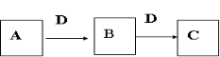
【推荐1】A、B、C、D四种物质或其水溶液有如图转化关系。
试回答下列问题:
(1)若A为金属单质,C为淡黄色固体,写出物质C的一种用途:_________ ;写出物质C与水反应的化学方程式_________ 。若不考虑其他离子的影响,向同时含有下列离子的混合溶液中加入少量固体C后,再继续滴加足量的稀硫酸,最终离子数目不变的是_________ 。
a.Na+ b.Mg2+ c.K+ d.Fe2+ e.Fe3+
(2)若A是一种引起温室效应的气体,D为焰色试验显黄色的强碱,则B→C的离子方程式_________ ,若A为焰色试验显黄色的强碱, D为引起温室效应的气体,B→ C的离子方程式_________ 。
(3)若A、B、C中均含有同一种非金属元素,A单质常用来自来水杀菌消毒,D是目前使用量最大的金属。实验室常用鉴定B中金属阳离子的试剂(填名称)_________ 。向物质C的溶液中滴加氢氧化钠后得到的沉淀会有一系列颜色变化,试写出该转化的化学反应方程式:_________ 。

试回答下列问题:
(1)若A为金属单质,C为淡黄色固体,写出物质C的一种用途:
a.Na+ b.Mg2+ c.K+ d.Fe2+ e.Fe3+
(2)若A是一种引起温室效应的气体,D为焰色试验显黄色的强碱,则B→C的离子方程式
(3)若A、B、C中均含有同一种非金属元素,A单质常用来自来水杀菌消毒,D是目前使用量最大的金属。实验室常用鉴定B中金属阳离子的试剂(填名称)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】 在医药、电子等领域有重要应用。可采用碱浸氧化法把含砷废渣(含有
在医药、电子等领域有重要应用。可采用碱浸氧化法把含砷废渣(含有 等)中的砷转化成
等)中的砷转化成 并将其分离出来,其工艺流程如下:
并将其分离出来,其工艺流程如下:
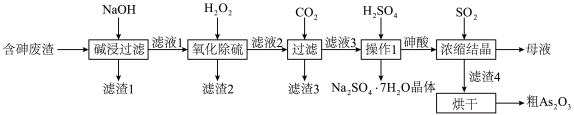
回答下列问题:
(1) 中砷元素的化合价为
中砷元素的化合价为_______ 。
(2)“碱浸”时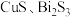 不溶,
不溶, 转化成了可溶于水的
转化成了可溶于水的 和
和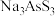 ,该反应的实际速率比理论上缓慢很多,可能的原因为
,该反应的实际速率比理论上缓慢很多,可能的原因为_______ (写出一种原因即可)。
(3)“滤渣2”为硫,反应后砷元素的化合价变成 ,写出除硫反应的离子方程式
,写出除硫反应的离子方程式_______ 。“氧化除硫”中可替代 的物质是
的物质是_______ (写出一种即可)。
(4)“滤渣3”为_______ (填化学式)。“操作1”的过程:先_______ ,再过滤得到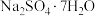 。
。
(5)上述流程中,可以循环使用“母液”的操作步骤为_______ (填工艺流程图方框中的操作步骤)。
(6)利用反应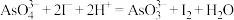 测定“滤液2”中
测定“滤液2”中 的含量。取
的含量。取 “滤液2”于锥形瓶中,加入适量硫酸,再加入过量
“滤液2”于锥形瓶中,加入适量硫酸,再加入过量 溶液,充分反应后,以淀粉为指示剂,用
溶液,充分反应后,以淀粉为指示剂,用 的
的 标准溶液滴定到终点,重复三次实验,记录用去
标准溶液滴定到终点,重复三次实验,记录用去 标准溶液的平均体积为
标准溶液的平均体积为 ,则“滤液2”中
,则“滤液2”中 含量为
含量为_______  。(已知:
。(已知: )
)
 在医药、电子等领域有重要应用。可采用碱浸氧化法把含砷废渣(含有
在医药、电子等领域有重要应用。可采用碱浸氧化法把含砷废渣(含有 等)中的砷转化成
等)中的砷转化成 并将其分离出来,其工艺流程如下:
并将其分离出来,其工艺流程如下:
回答下列问题:
(1)
 中砷元素的化合价为
中砷元素的化合价为(2)“碱浸”时
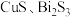 不溶,
不溶, 转化成了可溶于水的
转化成了可溶于水的 和
和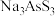 ,该反应的实际速率比理论上缓慢很多,可能的原因为
,该反应的实际速率比理论上缓慢很多,可能的原因为(3)“滤渣2”为硫,反应后砷元素的化合价变成
 ,写出除硫反应的离子方程式
,写出除硫反应的离子方程式 的物质是
的物质是(4)“滤渣3”为
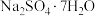 。
。(5)上述流程中,可以循环使用“母液”的操作步骤为
(6)利用反应
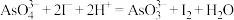 测定“滤液2”中
测定“滤液2”中 的含量。取
的含量。取 “滤液2”于锥形瓶中,加入适量硫酸,再加入过量
“滤液2”于锥形瓶中,加入适量硫酸,再加入过量 溶液,充分反应后,以淀粉为指示剂,用
溶液,充分反应后,以淀粉为指示剂,用 的
的 标准溶液滴定到终点,重复三次实验,记录用去
标准溶液滴定到终点,重复三次实验,记录用去 标准溶液的平均体积为
标准溶液的平均体积为 ,则“滤液2”中
,则“滤液2”中 含量为
含量为 。(已知:
。(已知: )
)
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】Ⅰ.某钠盐溶液中通入足量氨气,无明显现象.再在所得溶液中通入过量CO2,产生大量白色沉淀。
(1)写出氨气的电子式_______________ 。
(2)该钠盐溶液中一定不可能含有下列哪种微粒_______________ (填编号)。
(3)写出一个通入过量CO2时生成白色沉淀的离子方程式________________ 。
Ⅱ.电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放.某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下:
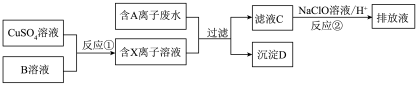
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,反应后的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
(4)沉淀D的化学式是________________ 。
(5)写出沉淀D在氧气中灼烧发生的化学方程式______________________ 。
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理___________________ 。
(7)反应①为制得某种元素的低价X离子,从氧化还原反应的角度分析,___________ 填“能”或“不能”用Na2SO3溶液来代替B溶液,原因是_________________ 。
(8)设计实验证明所用Na2SO3溶液是否变质_____________________ 。
(1)写出氨气的电子式
(2)该钠盐溶液中一定不可能含有下列哪种微粒
| A.Cl﹣ | B.Fe2+ | C.SiO32﹣ | D.AlO2﹣ |
Ⅱ.电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放.某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下:

已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,反应后的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
(4)沉淀D的化学式是
(5)写出沉淀D在氧气中灼烧发生的化学方程式
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理
(7)反应①为制得某种元素的低价X离子,从氧化还原反应的角度分析,
(8)设计实验证明所用Na2SO3溶液是否变质
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】元素①~⑧在元素周期表中的位置如下,回答有关问题:
(1)某元素是①~⑧外的元素,其最外层电子数是次外层电子数的 ,在地壳中含量仅次于氧元素,则该元素在周期表的位置
,在地壳中含量仅次于氧元素,则该元素在周期表的位置_______________ ;
(2)元素①~⑧化学性质最稳定的元素是________ (填数字), 写出该元素含有22个中子的核素的化学符号________
(3)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为_______________ (用化学式表示,下同),②③⑥元素氢化物的稳定性最强的是________ (填化学式)。
(4)比较④_________ ⑧的金属性(填“>”或“<”),能说明这一结论的依据有________
A.单质的熔点大小 B.最高价氧化物水化物的碱性强弱
C.单质的密度大小 D.单质与水反应的剧烈程度
(5)能体现②⑥元素非金属性强弱的化学方程式_______________________________ 。
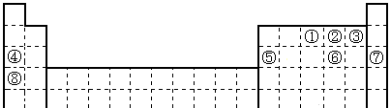
(1)某元素是①~⑧外的元素,其最外层电子数是次外层电子数的
 ,在地壳中含量仅次于氧元素,则该元素在周期表的位置
,在地壳中含量仅次于氧元素,则该元素在周期表的位置(2)元素①~⑧化学性质最稳定的元素是
(3)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为
(4)比较④
A.单质的熔点大小 B.最高价氧化物水化物的碱性强弱
C.单质的密度大小 D.单质与水反应的剧烈程度
(5)能体现②⑥元素非金属性强弱的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】随着新能源汽车销量的猛增,动力电池退役高峰将至,磷酸铁锂 是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片(
是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( 、导电石墨、铝箔)中回收锂的工艺流程如下:
、导电石墨、铝箔)中回收锂的工艺流程如下:
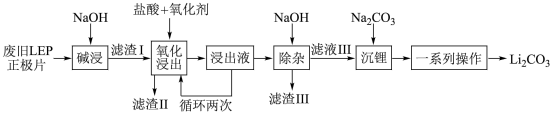
已知:i.废旧磷酸铁锂正极片中的化学物质均不溶于水也不与水反应。
ii. 在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
回答下列问题:
(1) 中密度最小的金属元素在周期表中的位置是
中密度最小的金属元素在周期表中的位置是_______ 。
(2)“氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如下表,实际生产中氧化剂选用 ,不选用
,不选用 的原因是
的原因是_______ 。在“氧化浸出”时,适当的升温可加快反应速率,但一般不采取高温法,其原因是_______ 。 “氧化浸出”时生成了难溶的 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3)“浸出液”循环两次的目的是_______ 。
(4)“滤渣II”经纯化可得 ,流程中生成的
,流程中生成的 、
、 在高温条件下与
在高温条件下与 煅烧可得
煅烧可得 ,实现再生利用,其化学方程式为
,实现再生利用,其化学方程式为_______ 。
(5)“一系列操作”具体包括_______ 、洗涤、干燥。
 是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片(
是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( 、导电石墨、铝箔)中回收锂的工艺流程如下:
、导电石墨、铝箔)中回收锂的工艺流程如下:
已知:i.废旧磷酸铁锂正极片中的化学物质均不溶于水也不与水反应。
ii.
 在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。回答下列问题:
(1)
 中密度最小的金属元素在周期表中的位置是
中密度最小的金属元素在周期表中的位置是(2)“氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如下表,实际生产中氧化剂选用
 ,不选用
,不选用 的原因是
的原因是 ,该反应的化学方程式为
,该反应的化学方程式为| 序号 | 锂含量/% | 氧化剂 |  | 浸出液 浓度 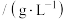 | 浸出渣中 含量/% |
| 1 | 3.7 |  | 3.5 | 9.02 | 0.10 |
| 2 | 3.7 |  | 3.5 | 9.05 | 0.08 |
| 3 | 3.7 |  | 3.5 | 7.05 | 0.93 |
| 4 | 3.7 |  | 3.5 | 8.24 | 0.43 |
(4)“滤渣II”经纯化可得
 ,流程中生成的
,流程中生成的 、
、 在高温条件下与
在高温条件下与 煅烧可得
煅烧可得 ,实现再生利用,其化学方程式为
,实现再生利用,其化学方程式为(5)“一系列操作”具体包括
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】钒基笼目金属在超导电性方面有广阔的应用前最。某钒基笼目金属(M)的晶体结构如图所示。
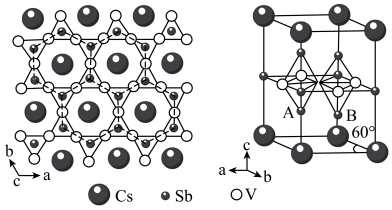
(1)Sb在元素周期表中的位置是___________ 。
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为___________ 。
(3)钒化合物在药物化学及催化化学等领域应用广泛。基态钒原子的价电子排布图为___________ ,钒有+2、+3、+4、+5等多种化合价,其中最稳定的化合价是_________ , 的空间结构为
的空间结构为________ 。
(4)SbH3的键角比NH3的键角小,原因是___________ 。
(5)该钒基笼目金属(M)的化学式为___________ ,与V原子距离最近且等距的V原子________ 个。
(6)已知,该晶胞中距离最近的两个V原子间的距离为2.75 Å,则晶胞体内A、B原子之间的距离为___________ Å ( ≈1.73, 保留两位小数)。
≈1.73, 保留两位小数)。

(1)Sb在元素周期表中的位置是
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为
(3)钒化合物在药物化学及催化化学等领域应用广泛。基态钒原子的价电子排布图为
 的空间结构为
的空间结构为(4)SbH3的键角比NH3的键角小,原因是
(5)该钒基笼目金属(M)的化学式为
(6)已知,该晶胞中距离最近的两个V原子间的距离为2.75 Å,则晶胞体内A、B原子之间的距离为
 ≈1.73, 保留两位小数)。
≈1.73, 保留两位小数)。
您最近一年使用:0次
【推荐1】资料显示, 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。
将等体积的 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。
实验记录如下:
(1)基态 的电子排布式
的电子排布式___________ 。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有 (蓝色)或
(蓝色)或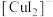 (无色),进行以下实验探究:
(无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入 ,多次萃取、分液。
,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去 的原理是
的原理是___________ 。
ii.查阅资料, (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:___________ ,___________ 。
(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,___________ (填实验现象)。实验Ⅲ中铜被氧化的化学方程式是___________ 。
(4)上述实验结果, 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
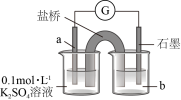
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为___________ ,b试剂为___________ 。
 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。将等体积的
 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。实验记录如下:
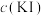 | 实验现象 | |
| 实验Ⅰ | 0.01 | 极少量 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 |
| 实验Ⅱ | 0.1 | 部分 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 |
| 实验Ⅲ | 4 |  完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 |
 的电子排布式
的电子排布式(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有
 (蓝色)或
(蓝色)或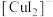 (无色),进行以下实验探究:
(无色),进行以下实验探究:步骤a.取实验Ⅲ的深红棕色溶液,加入
 ,多次萃取、分液。
,多次萃取、分液。步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去
 的原理是
的原理是ii.查阅资料,
 (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是
 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,(4)上述实验结果,
 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某化学实验小组探究 与
与 溶液的反应。
溶液的反应。
实验一:用如图所示实验装置制备 ,并将足量
,并将足量 通入
通入 溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。
溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。
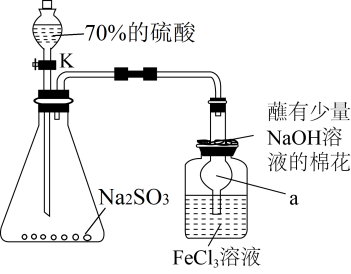
(1)制备 的化学反应方程式为
的化学反应方程式为___________ 。
(2)仪器 的名称为
的名称为___________ 。
(3)某同学取适量酸性 于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有
于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有 ,此结论
,此结论___________ (填“正确”、“不正确”),理由是___________ 。
实验二:探究血红色溶液产生的原因
实验过程如下表:
(4)实验①中, 是
是___________ (填化学式);实验②中现象是___________ 。
(5)为了进一步探究血红色物质产生的主要原因,又进行了以下实验:在
 的
的 溶液中,加入浓度相同的
溶液中,加入浓度相同的 溶液
溶液 ,
, 溶液
溶液 并混合均匀,改变
并混合均匀,改变 、
、 的值并维持
的值并维持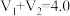 进行多组实验,测得混合溶液的吸光度与
进行多组实验,测得混合溶液的吸光度与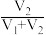 出的关系如图所示。(已知吸光度越大,溶液颜色越深)。
出的关系如图所示。(已知吸光度越大,溶液颜色越深)。
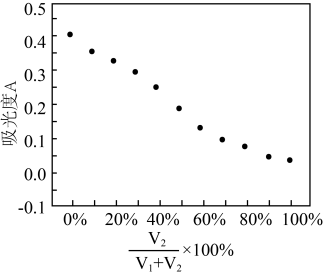
①维持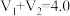 的目的是
的目的是___________ 。
②该实验得出的结论是___________ 。
 与
与 溶液的反应。
溶液的反应。实验一:用如图所示实验装置制备
 ,并将足量
,并将足量 通入
通入 溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。
溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。
(1)制备
 的化学反应方程式为
的化学反应方程式为(2)仪器
 的名称为
的名称为(3)某同学取适量酸性
 于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有
于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有 ,此结论
,此结论实验二:探究血红色溶液产生的原因
实验过程如下表:
| 实验序号 | 假设 | 实验内容 | 结论 |
| ① |  增大 增大 | 取上述血红色溶液,滴入 溶液,溶液又变为黄色 溶液,溶液又变为黄色 | 假设不成立 |
| ② |  和 和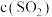 增大 增大 | 在 溶液中,滴入 溶液中,滴入  溶液,溶液呈血红色,再逐渐滴入 溶液,溶液呈血红色,再逐渐滴入 溶液,出现 溶液,出现 | 假设不成立 |
| ③ | 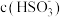 或 或 增大 增大 | 在 溶液中加入 溶液中加入 溶液,立即变为血红色 溶液,立即变为血红色 | 假设成立 |
 是
是(5)为了进一步探究血红色物质产生的主要原因,又进行了以下实验:在

 的
的 溶液中,加入浓度相同的
溶液中,加入浓度相同的 溶液
溶液 ,
, 溶液
溶液 并混合均匀,改变
并混合均匀,改变 、
、 的值并维持
的值并维持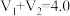 进行多组实验,测得混合溶液的吸光度与
进行多组实验,测得混合溶液的吸光度与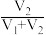 出的关系如图所示。(已知吸光度越大,溶液颜色越深)。
出的关系如图所示。(已知吸光度越大,溶液颜色越深)。
①维持
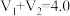 的目的是
的目的是②该实验得出的结论是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】过渡金属元素铬( )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)请写出基态铬( )原子价电子的轨道表示式
)原子价电子的轨道表示式___________ 。
(2)超分子的定义是广义的,包括离子。一种羟甲基酚钠盐形成的含铁超分子的化学式为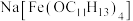 ,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:
,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:___________ 。
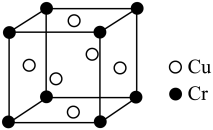
(3)某铜铬合金的立方晶胞结构如图所示。该铜铬合金的化学式为___________ ;离 原子最近的
原子最近的 原子数目为
原子数目为___________ ,离 原子最近的
原子最近的 原子数目为
原子数目为___________ 。若该晶胞参数为apm,则该晶体的密度为___________  。
。___________ 种。其同主族元素Si可形成硅酸盐,下图中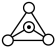 表示硅氧四面体,则该硅酸盐结构的通式为
表示硅氧四面体,则该硅酸盐结构的通式为___________ 。
 )是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:(1)请写出基态铬(
 )原子价电子的轨道表示式
)原子价电子的轨道表示式(2)超分子的定义是广义的,包括离子。一种羟甲基酚钠盐形成的含铁超分子的化学式为
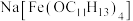 ,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:
,已知羟甲基酚属于杯酚,请写出该含铁超分子的一种特性:(3)某铜铬合金的立方晶胞结构如图所示。该铜铬合金的化学式为
 原子最近的
原子最近的 原子数目为
原子数目为 原子最近的
原子最近的 原子数目为
原子数目为 。
。
 表示硅氧四面体,则该硅酸盐结构的通式为
表示硅氧四面体,则该硅酸盐结构的通式为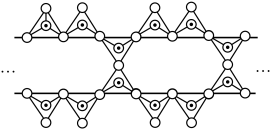
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。某化学兴趣小组设计如图装置以制备Cl2O(支撑及夹持装置已省略)。
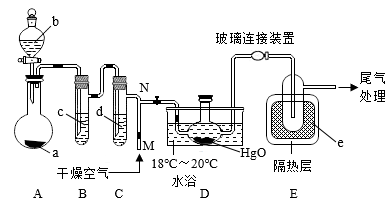
已知:①a中固体试剂是MnO2,b中试剂是浓盐酸。
②Cl2O的部分性质如表:
请回答:
(1)指出该制备装置中存在的一个明显错误_____ (经改进后进行有关实验)。
(2)装置C中盛有的试剂是_____ 。
(3)写出装置A中制备Cl2的化学方程式_____ 。
(4)装置D中采用18℃~20℃水浴的原因之一是:如温度过低,反应速率慢,另一个可能的原因是_____ 。
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是_____ 。
(6)Cl2O是市场上一种比较理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是等质量的Cl2O的_____ 倍(结果保留一位小数)
(7)据文献报道,Cl2O的另一种制备方法是利用Cl2与适量潮湿的Na2CO3反应来制得,同时产生一种无色气体(该气体含两种元素),写出该反应的化学方程式______ 。

已知:①a中固体试剂是MnO2,b中试剂是浓盐酸。
②Cl2O的部分性质如表:
| 熔点 | 沸点 | 制备方法 |
| 120.6℃ | 3.8℃ | 2HgO+2Cl2=Cl2O+HgCl2·HgO(反应放热) |
(1)指出该制备装置中存在的一个明显错误
(2)装置C中盛有的试剂是
(3)写出装置A中制备Cl2的化学方程式
(4)装置D中采用18℃~20℃水浴的原因之一是:如温度过低,反应速率慢,另一个可能的原因是
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是
(6)Cl2O是市场上一种比较理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是等质量的Cl2O的
(7)据文献报道,Cl2O的另一种制备方法是利用Cl2与适量潮湿的Na2CO3反应来制得,同时产生一种无色气体(该气体含两种元素),写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】磷精矿[主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等]湿法制备磷酸的一种工艺流程如下:

已知:溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有____ (任写一条即可)。
(2)写出磷精矿粉酸浸时,其主要成分发生反应的化学方程式__________ ,该反应体现出酸性关系:H2SO4_____ H3PO4(填“>”或“<”)。
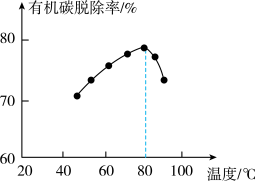
(3)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因是_________ 。
(4)脱硫时,CaCO3稍过量,充分反应后仍有 残留,原因是
残留,原因是____________ 。
(5)取ag所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用bmol/LNaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液cmL,精制磷酸中H3PO4的质量分数是____________ (已知:H3PO4摩尔质量为98g/mol)。

已知:溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有
(2)写出磷精矿粉酸浸时,其主要成分发生反应的化学方程式
(3)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因是

(4)脱硫时,CaCO3稍过量,充分反应后仍有
 残留,原因是
残留,原因是(5)取ag所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用bmol/LNaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液cmL,精制磷酸中H3PO4的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图(如图),回答下列问题。
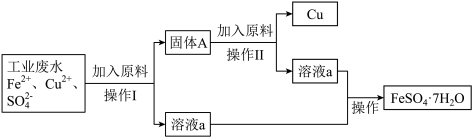
(1)操作Ⅰ中所用的仪器有____ 。
(2)固体A的成分是___ 和____ 。(填名称);操作Ⅲ是____ 。
(3)如何检验溶液a中主要阴离子____ 。
(4)回收的铜可以用于制备胆矾(CuSO4·5H2O)。将铜和0.22mol/LH2SO4溶液混合后,在加热的情况下不断通入氧气就可以制得CuSO4,然后将所得的溶液经过“一系列操作”后得到胆矾。写出生成CuSO4的化学方程式:___ 。
(5)某同学用密度为1.84g/cm3、质量分数为98%的浓硫配制500mL0.22mol/L的稀硫酸溶液,需要用规格为___ mL的量筒量取___ mL的浓硫酸。
(6)配制该溶液的过程中,下列操作使得所配得的溶液浓度偏小的是___ (填字母)。
A.稀释密度为1.84g/cm3、质量分数为98%的浓硫酸时,不小心溅出少量硫酸溶液
B.用蒸馏水洗涤烧杯、量筒及玻璃棒,并将洗涤液注入容量瓶中
C.定容时反复上下倒转容量瓶后,发现凹液面最低处低于刻度线,再补加水到刻度线
D.量取密度为1.84g/cm3、质量分数为98%的浓硫酸时,仰视量筒的刻度线
E.洗涤容量瓶后,立即用来配制溶液
F.稀释浓硫酸结束后立即将溶液转移到容量瓶中

(1)操作Ⅰ中所用的仪器有
(2)固体A的成分是
(3)如何检验溶液a中主要阴离子
(4)回收的铜可以用于制备胆矾(CuSO4·5H2O)。将铜和0.22mol/LH2SO4溶液混合后,在加热的情况下不断通入氧气就可以制得CuSO4,然后将所得的溶液经过“一系列操作”后得到胆矾。写出生成CuSO4的化学方程式:
(5)某同学用密度为1.84g/cm3、质量分数为98%的浓硫配制500mL0.22mol/L的稀硫酸溶液,需要用规格为
(6)配制该溶液的过程中,下列操作使得所配得的溶液浓度偏小的是
A.稀释密度为1.84g/cm3、质量分数为98%的浓硫酸时,不小心溅出少量硫酸溶液
B.用蒸馏水洗涤烧杯、量筒及玻璃棒,并将洗涤液注入容量瓶中
C.定容时反复上下倒转容量瓶后,发现凹液面最低处低于刻度线,再补加水到刻度线
D.量取密度为1.84g/cm3、质量分数为98%的浓硫酸时,仰视量筒的刻度线
E.洗涤容量瓶后,立即用来配制溶液
F.稀释浓硫酸结束后立即将溶液转移到容量瓶中
您最近一年使用:0次



