A+、B+、C-、D、E、F2- 6种微粒(分子或离子),它们分别含10个电子,其中只有B+和F2-为单核微粒,且C-和E的组成元素相同,已知它们有如下转化关系:A++C-→D+E,据此回答下列问题:
(1)写出D的电子式_______ ,E的结构式________ 。
(2)实验室制备D物质的反应方程式__________ 。
(3)上述六种微粒中所含有的元素原子半径从大到小的顺序是__ (用元素符号表示)。
(4)B、F两元素组成的原子数目比为1:1的化合物的电子式______ 、该物质中存在的化学键有______ 。
(1)写出D的电子式
(2)实验室制备D物质的反应方程式
(3)上述六种微粒中所含有的元素原子半径从大到小的顺序是
(4)B、F两元素组成的原子数目比为1:1的化合物的电子式
更新时间:2020-07-24 19:46:33
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是____ (填元素符号,下同),第一电离能最小的是____ 。
(2)C所在的主族元素气态氢化物中,沸点最低的是____ (填化学式)。
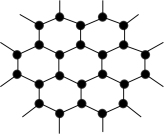
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为____ 。
(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是____ (填选项序号)。

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
D单质 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:____ 。
(1)这四种元素中电负性最大的是
(2)C所在的主族元素气态氢化物中,沸点最低的是
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为

(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是

①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
D单质
 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀请书写第⑤步反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4•H2O。
(1)Cu2+价电子排布式为_______ ;[Cu(NH3)4]SO4•H2O中,1mol[Cu(NH3)4]2+含有σ键的数目为_____ 。
(2)SO42-中S原子轨道杂化类型为_____ ,H2O与H+以配位键形成H3O+,则H3O+的空间构型为____ (用文字描述)。
(3)N、O、S第一电离能由大到小的顺序为___________ 。
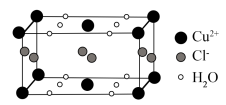
(4)某含有结晶水的铜的氯化物的晶胞结构如图所示,该化合物的化学式是________ 。
(1)Cu2+价电子排布式为
(2)SO42-中S原子轨道杂化类型为
(3)N、O、S第一电离能由大到小的顺序为
(4)某含有结晶水的铜的氯化物的晶胞结构如图所示,该化合物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E、F是前四周期的核电荷数依次增大主族元素,A的最外层电子数是其电子层数的2倍,C、D同一主族,D元素原子M层有两对成对电子,E在前四周期主族元素中原子半径最大,F的基态原子中有4个未成对电子。
(1)基态Fe2+的电子排布式是_____ 。
(2)B、C、D的第一电离能由大到小的顺序是_____ 。(填字母对应的元素符号)
(3)BC 离子的空间构型为
离子的空间构型为_____ 。
(4)某F的配合物化学式是[F(H2O)5Cl]Cl2·H2O,与中心F3+的形成配位键的原子或离子是_____ 。
(5)F(AC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。
每个AC分子与F原子间均有1个配位键。
①1 mol F(AC)5中所含σ键的数目为_____ 。
②F(AC)5分子的结构可能为下图中的_____ (填“甲”或“乙”)
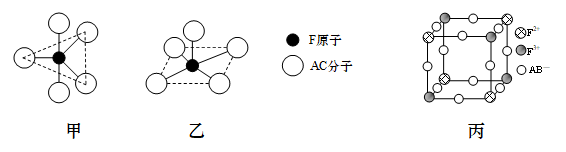
(6)由A、B、E、F元素形成的一种蓝色晶体,其晶体结构示意图如图丙所示(图中E的离子未画出)。该蓝色晶体的化学式为_____ 。
(1)基态Fe2+的电子排布式是
(2)B、C、D的第一电离能由大到小的顺序是
(3)BC
 离子的空间构型为
离子的空间构型为(4)某F的配合物化学式是[F(H2O)5Cl]Cl2·H2O,与中心F3+的形成配位键的原子或离子是
(5)F(AC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。
每个AC分子与F原子间均有1个配位键。
①1 mol F(AC)5中所含σ键的数目为
②F(AC)5分子的结构可能为下图中的

(6)由A、B、E、F元素形成的一种蓝色晶体,其晶体结构示意图如图丙所示(图中E的离子未画出)。该蓝色晶体的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D、E为原子序数依次增大的短周期元素。已知A、B、E三原子最外层共有11个电子,且这三种元素的最高价氧化物对应水化物之间两两皆能反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。回答:
(1)写出元素符号:A___________ 、B___________ 、C___________ 、D___________ 、E___________ 。
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式___________ 。A、E两元素最高价氧化物对应水化物相互反应的化学方程式___________ 。
(3)比较C、D最高价氧化物对应水化物的酸性___________ (用化学式表示)。
(1)写出元素符号:A
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式
(3)比较C、D最高价氧化物对应水化物的酸性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】有原子序数小于20的A、B、C、D、E、F六种元素,它们的原子序数依次增大. 已知B元素是地壳中含量最多的元素; A和C的价电子数相同,B和D的价电子数也相同,且A和C两元素原子核外电子数之和是B、D两元素原子核内质子数之和的二分之一;C、D、E三种元素的基态原子具有相同的电子层数,且E原子的p轨道上电子数比D原子的p轨道上多一个电子;六种元素的基态原子中,F原子的电子层数最多且和A处在同一主族.回答下列问题:
(1)写出基态F原子的核外电子排布式____________
(2)A、B、C共同形成的化合物中化学键的类型____________ 。
(1)写出基态F原子的核外电子排布式
(2)A、B、C共同形成的化合物中化学键的类型
您最近一年使用:0次
【推荐3】A、B、C、D、E、F、G为周期表前四周期元素,原子序数依次增大。A元素的价电子构型为 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价阳离子的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价阳离子的 轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。回答下列问题:
轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。回答下列问题:
(1)第一电离能:A__________ B,电负性:C__________ B(填“>”“=”或“<”)
(2)基态D原子核外电子的运动状态有___________ 种。
(3)元素E在周期表中的位置是______________ 。F属于周期表的__________ 区。
(4)基态G原子的价电子排布式为_____________________ 。
 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价阳离子的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的1/6;E元素正三价阳离子的 轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。回答下列问题:
轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。回答下列问题:(1)第一电离能:A
(2)基态D原子核外电子的运动状态有
(3)元素E在周期表中的位置是
(4)基态G原子的价电子排布式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D 四种元素,原子序数依次增大,A 原子的最外层上有4个电子;B的阴离子和 C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)C离子的结构示意图为_____ 。D在周期表中位置_____ 。
(2)A、D两元素形成的化合物属_____ (填“离子”或“共价”)化合物。
(3)写出D的最高价氧化物的水化物和A单质反应的化学方程式:_____ 。
(4)写出B与氯元素和氢元素形成的氯水中含有的具有漂白性物质的结构式_____________
(1)C离子的结构示意图为
(2)A、D两元素形成的化合物属
(3)写出D的最高价氧化物的水化物和A单质反应的化学方程式:
(4)写出B与氯元素和氢元素形成的氯水中含有的具有漂白性物质的结构式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】 、
、 、
、 、
、 、
、 、
、 六种短周期主族元素,其原子序数依次增大。
六种短周期主族元素,其原子序数依次增大。 是形成化合物种类最多的元素,
是形成化合物种类最多的元素, 、
、 能形成两种液态化合物
能形成两种液态化合物 和
和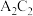 ,
, 、
、 同主族,
同主族, 元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为___________ , 、
、 、
、 三种元素的原子半径由大到小顺序为
三种元素的原子半径由大到小顺序为___________ (用原子符号表示)。
(2)化合物 、
、 性质比较:热稳定性:
性质比较:热稳定性:
___  ;沸点:
;沸点:
____  (填“
(填“ ”或“
”或“ ”)。
”)。
(3)物质 由
由 、
、 两种元素组成,
两种元素组成, 的产量可以用来衡量一个国家的石油化工发展水平,则
的产量可以用来衡量一个国家的石油化工发展水平,则 分子的电子式为:
分子的电子式为:___________ ,将 通入溴的四氧化碳溶液中,发生反应的化学方程式为
通入溴的四氧化碳溶液中,发生反应的化学方程式为___________ 。
(4) 的单质和化合物是一种用途很广的材料。写出
的单质和化合物是一种用途很广的材料。写出 单质与氧化铁高温加热制取铁的化学方程式:
单质与氧化铁高温加热制取铁的化学方程式:___________ 。
(5)向 溶液中通入适量的
溶液中通入适量的 单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:___________ 。
 、
、 、
、 、
、 、
、 、
、 六种短周期主族元素,其原子序数依次增大。
六种短周期主族元素,其原子序数依次增大。 是形成化合物种类最多的元素,
是形成化合物种类最多的元素, 、
、 能形成两种液态化合物
能形成两种液态化合物 和
和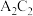 ,
, 、
、 同主族,
同主族, 元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
元素的周期序数与主族序数相等。根据以上信息,回答下列问题:(1)
 元素在周期表中的位置为
元素在周期表中的位置为 、
、 、
、 三种元素的原子半径由大到小顺序为
三种元素的原子半径由大到小顺序为(2)化合物
 、
、 性质比较:热稳定性:
性质比较:热稳定性:
 ;沸点:
;沸点:
 (填“
(填“ ”或“
”或“ ”)。
”)。(3)物质
 由
由 、
、 两种元素组成,
两种元素组成, 的产量可以用来衡量一个国家的石油化工发展水平,则
的产量可以用来衡量一个国家的石油化工发展水平,则 分子的电子式为:
分子的电子式为: 通入溴的四氧化碳溶液中,发生反应的化学方程式为
通入溴的四氧化碳溶液中,发生反应的化学方程式为(4)
 的单质和化合物是一种用途很广的材料。写出
的单质和化合物是一种用途很广的材料。写出 单质与氧化铁高温加热制取铁的化学方程式:
单质与氧化铁高温加热制取铁的化学方程式:(5)向
 溶液中通入适量的
溶液中通入适量的 单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素,元素A的一种原子无中子,B位于第二周期第IVA族,C位于第二周期第VIA族,B、C能形成无色无味的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C形成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ar的电子层结构相同,试回答:
(1)它们的元素符号是:A__ ;B___ ;C__ ;D__ ;E__ 。
(2)A与B形成的化合物以___ 键结合,C和E的化合物以__ 键结合。
(3)BC2的结构式为___ ;C和E形成的化合物E2C其电子式为:___ 。
(1)它们的元素符号是:A
(2)A与B形成的化合物以
(3)BC2的结构式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D是原子序数依次增大的短周期主族元素。A元素的单质是一种清洁燃料,B元素的原子最外层电子数为次外层电子数的3倍,C元素的+1价离子与B元素的简单离子的电子层结构相同,D与B位于同一主族。根据上述内容判断:
(1)A为___________ (填元素符号),D的原子结构示意图为___________ 。
(2)对这四种元素的原子半径从小到大排序___________ (填元素符号)。
(3)B元素在元素周期表中的位置为___________ ,其氢化物属于___________ (填下列字母)。该氢化物比D元素氢化物的沸点___________ (填“高”或“低”)。
A.非电解质 B.强电解质 C.弱电解质 D.离子化合物 E.共价化合物
(4)C的最高价氧化物的水化物所含化学键的类型为___________ ,其与D的最高价氧化物的水化物发生反应的化学方程式为___________ 。
(1)A为
(2)对这四种元素的原子半径从小到大排序
(3)B元素在元素周期表中的位置为
A.非电解质 B.强电解质 C.弱电解质 D.离子化合物 E.共价化合物
(4)C的最高价氧化物的水化物所含化学键的类型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表揭示了元素之间的内在联系,使元素构成了一个较为系统的体系.请回答下列问题:
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的_______ 。按照元素在周期表中的顺序给元素编号,得到原子序数。人们发现原子序数与元素的原子结构之间存在如下关系:原子序数=_______ =核外电子数
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。
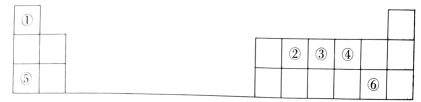
(1)②、③、④三种元素中,原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)①、④、⑤三种元素形成的化合物的电子式为_______ ,该化合物中化学键的类型有_______ 。
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:_______ 。根据元素周期律推测,下列性质中Q不可能具有的是_______ (填选项字母)。
A.最高正化合价为 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。

(1)②、③、④三种元素中,原子半径由大到小的顺序为
(2)①、④、⑤三种元素形成的化合物的电子式为
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:
A.最高正化合价为
 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素,用化学用语回答下列问题:
(1)⑤在元素周期表中的位置是__________ 。
(2)①的最高价氧化物的结构式为___________ 。
(3)②③单质在加热条件下形成的物质中含有的化学键类型是__________ 。
(4)用电子式表示④⑦元素物质的形成过程__________ 。
(5)②、④、⑥离子半径由大到小的顺序为____________ 。
(6)②⑦组成的物质是新的自来水消毒剂,可以用来除去水中超标的锰离子,生成黑色沉淀,当消耗13.50g②⑦组成的物质时,共转移了1mol电子,则反应的离子方程式为____________ 。
① | ② | |||||||
③ | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)①的最高价氧化物的结构式为
(3)②③单质在加热条件下形成的物质中含有的化学键类型是
(4)用电子式表示④⑦元素物质的形成过程
(5)②、④、⑥离子半径由大到小的顺序为
(6)②⑦组成的物质是新的自来水消毒剂,可以用来除去水中超标的锰离子,生成黑色沉淀,当消耗13.50g②⑦组成的物质时,共转移了1mol电子,则反应的离子方程式为
您最近一年使用:0次



