 、
、 、
、 、
、 、
、 、
、 六种短周期主族元素,其原子序数依次增大。
六种短周期主族元素,其原子序数依次增大。 是形成化合物种类最多的元素,
是形成化合物种类最多的元素, 、
、 能形成两种液态化合物
能形成两种液态化合物 和
和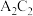 ,
, 、
、 同主族,
同主族, 元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
元素的周期序数与主族序数相等。根据以上信息,回答下列问题:(1)
 元素在周期表中的位置为
元素在周期表中的位置为 、
、 、
、 三种元素的原子半径由大到小顺序为
三种元素的原子半径由大到小顺序为(2)化合物
 、
、 性质比较:热稳定性:
性质比较:热稳定性:
 ;沸点:
;沸点:
 (填“
(填“ ”或“
”或“ ”)。
”)。(3)物质
 由
由 、
、 两种元素组成,
两种元素组成, 的产量可以用来衡量一个国家的石油化工发展水平,则
的产量可以用来衡量一个国家的石油化工发展水平,则 分子的电子式为:
分子的电子式为: 通入溴的四氧化碳溶液中,发生反应的化学方程式为
通入溴的四氧化碳溶液中,发生反应的化学方程式为(4)
 的单质和化合物是一种用途很广的材料。写出
的单质和化合物是一种用途很广的材料。写出 单质与氧化铁高温加热制取铁的化学方程式:
单质与氧化铁高温加热制取铁的化学方程式:(5)向
 溶液中通入适量的
溶液中通入适量的 单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
更新时间:2021-07-07 07:20:14
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是_______ ,最活泼的非金属元素是_______ ,其单质常用作半导体材料的元素是_______ 。
(2)碱性最强的最高价氧化物对应水化物是_______ ,酸性最强的最高价氧化物对应水化物是_______ ,最稳定的气态氢化物是_______ 。
(3)将等质量的④、⑤、⑥分别投入100mL1mol/L硫酸溶液中,充分反应后产生的 在相同状况下的体积分别是
在相同状况下的体积分别是 、
、 、
、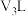 ,则下列关系中可能成立的是
,则下列关系中可能成立的是_______ 。
A.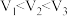 B.
B.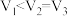 C.
C.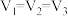 D.
D.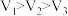 E.
E.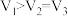
(4)能够比较⑧与⑨的非金属性强弱的依据是_______ 。
a.氢化物酸性⑨强于⑧
b.⑨单质能与⑧氢化物反应得到⑧单质
c.最高价氧化物水化物酸性⑨强于⑧
d.单质与 反应⑨比⑧更容易
反应⑨比⑧更容易
(5)某兴趣小组甲同学尝试用以下装置进行实验,以比较①⑦⑨三种元素的非金属性。
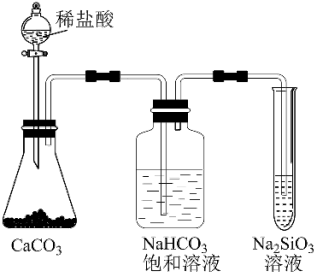
甲同学使用 饱和溶液的作用是
饱和溶液的作用是_______ 。乙同学认为以上设计存在错误,请分析乙同学的理由_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)将等质量的④、⑤、⑥分别投入100mL1mol/L硫酸溶液中,充分反应后产生的
 在相同状况下的体积分别是
在相同状况下的体积分别是 、
、 、
、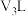 ,则下列关系中可能成立的是
,则下列关系中可能成立的是A.
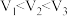 B.
B.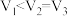 C.
C.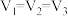 D.
D.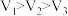 E.
E.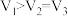
(4)能够比较⑧与⑨的非金属性强弱的依据是
a.氢化物酸性⑨强于⑧
b.⑨单质能与⑧氢化物反应得到⑧单质
c.最高价氧化物水化物酸性⑨强于⑧
d.单质与
 反应⑨比⑧更容易
反应⑨比⑧更容易(5)某兴趣小组甲同学尝试用以下装置进行实验,以比较①⑦⑨三种元素的非金属性。

甲同学使用
 饱和溶液的作用是
饱和溶液的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,表中所列的每个字母分别代表某一元素。
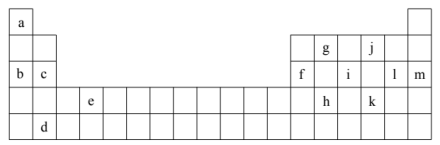
(1)表中所列元素中,属于短周期元素的有_______ ,属于主族元素的有_______ ,e元素在元素周期表中的位置是_______ 周期_______ 族。
(2)下列_______元素的单质可能都是电的良导体。
(3)i元素属于_______ (填“金属”或“非金属”)元素,它的最高化合价是_______ ,最低化合价是_______ 。
(4)按原子半径从小到大的顺序排列元素b、c、f、l,并从原子结构的角度解释这样排序的原因______ 。

(1)表中所列元素中,属于短周期元素的有
(2)下列_______元素的单质可能都是电的良导体。
| A.b、c、i | B.a、g、k | C.c、g、l | D.d、e、f |
(4)按原子半径从小到大的顺序排列元素b、c、f、l,并从原子结构的角度解释这样排序的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知X、Y、Z均为元素周期表中前20号元素,X和Z位于同一周期,Y的阳离子和Z的阴离子的核外电子排布相同,Y2Z2与H2Z或XZ2反应都能生成单质气体Z2。
(1)写出元素名称:X________ ,Y________ ,Z________ 。
(2)写出下列物质的电子式:Y2Z2__________________ ,XZ2__________________ 。
(3)用电子式表示Y2Z的形成过程:____________________________ 。
(1)写出元素名称:X
(2)写出下列物质的电子式:Y2Z2
(3)用电子式表示Y2Z的形成过程:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】下列是都分短周期中第二、第三周期元素的原子半径及主要化合价.
回答下列问题:
(1)⑦在元素周期表中的位置是(周期、族)______________ 。
(2)七种元素的最高价氧化物的水化物中,酸性最强的是______________ ,碱性最强的是______________ (填化学式)。
(3)②、⑤、⑦的离子半径由大到小的顺序是______________ (填离子符号)。
(4)①、⑤、⑦按原子个数比 组成的盐是“84”消毒液的主要成分,与洁厕灵混合使用易发生中毒事件.从氧化还原反应的角度分析其原因是(用化学方程式表示)
组成的盐是“84”消毒液的主要成分,与洁厕灵混合使用易发生中毒事件.从氧化还原反应的角度分析其原因是(用化学方程式表示)______________ 。
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
原子半径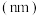 | 0.186 | 0.160 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 |  |  |  | +5、-3 | +7、-1 | +5、-3 | 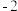 |
(1)⑦在元素周期表中的位置是(周期、族)
(2)七种元素的最高价氧化物的水化物中,酸性最强的是
(3)②、⑤、⑦的离子半径由大到小的顺序是
(4)①、⑤、⑦按原子个数比
 组成的盐是“84”消毒液的主要成分,与洁厕灵混合使用易发生中毒事件.从氧化还原反应的角度分析其原因是(用化学方程式表示)
组成的盐是“84”消毒液的主要成分,与洁厕灵混合使用易发生中毒事件.从氧化还原反应的角度分析其原因是(用化学方程式表示)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】现有X、Y、Z三种非金属元素,A、B、C三种金属元素,有:
①X、Y、Z的单质在常温下均为气体;
②X的单质在Z的单质中燃烧,火焰呈苍白色。产物XZ的水溶液可使石蕊试液变红;
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体;
④Z的单质溶于X2Y中所得的溶液具有漂白性;
⑤A的单质可以在Z的单质中燃烧,生成黑棕色固体,该固体溶于水得到棕黄色溶液;
⑥B与Z可形成化合物BZ3,向BZ3的溶液中逐滴滴加NaOH溶液,先生成白色沉淀后沉淀逐渐溶解;
⑦C的单质与Y的单质反应可能得到两种产物,其中一种为淡黄色固体M
请回答下列问题:
(1)写出下列物质的化学式:XZ__________ ,X2Y__________ ,M__________
(2)Z的单质溶于X2Y中所得溶液中起漂白作用的物质是__________ (填化学式)
(3)A的单质与Z的单质反应的化学方程式为__________
(4)BZ3与过量的NaOH溶液反应的离子方程式为__________
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,则原混合气体中X的单质与Z的单质的体积关系可能为__________ (用相应化学式表示X、Z的单质)
①X、Y、Z的单质在常温下均为气体;
②X的单质在Z的单质中燃烧,火焰呈苍白色。产物XZ的水溶液可使石蕊试液变红;
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体;
④Z的单质溶于X2Y中所得的溶液具有漂白性;
⑤A的单质可以在Z的单质中燃烧,生成黑棕色固体,该固体溶于水得到棕黄色溶液;
⑥B与Z可形成化合物BZ3,向BZ3的溶液中逐滴滴加NaOH溶液,先生成白色沉淀后沉淀逐渐溶解;
⑦C的单质与Y的单质反应可能得到两种产物,其中一种为淡黄色固体M
请回答下列问题:
(1)写出下列物质的化学式:XZ
(2)Z的单质溶于X2Y中所得溶液中起漂白作用的物质是
(3)A的单质与Z的单质反应的化学方程式为
(4)BZ3与过量的NaOH溶液反应的离子方程式为
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,则原混合气体中X的单质与Z的单质的体积关系可能为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素①~⑧在元素周期表中的位置如下,回答有关问题:
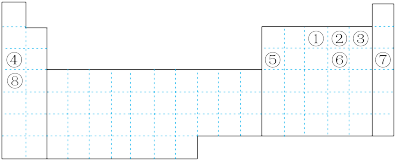
(1)画出⑥的离子结构示意图___________________ 。
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为________________ 【示例:用r(A2-)>r(B-)的形式表示】。
(3)元素②、③氢化物的稳定性由强到弱的顺序为(填化学式)____________________________ 。
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式___________ 。
(5)比较①与其同族短周期元素的氢化物的熔沸点高低,并说明理由____________________________ 。

(1)画出⑥的离子结构示意图
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为
(3)元素②、③氢化物的稳定性由强到弱的顺序为(填化学式)
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式
(5)比较①与其同族短周期元素的氢化物的熔沸点高低,并说明理由
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下图是元素周期表的一部分,根据① ~ ⑨在周期表中的位置按题目要求回答:
(1)画出⑩的原子结构示意图_________________________
(2)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的结构式__________________________________ 。
(3)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式__________________ 。
(4)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程__________________ 。
(5)②、⑥分别形成的两种氢化物中,沸点较高的是______ (填化学式),原因是:___________________________________________________ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ⅡA | …… …… …… | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ||||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||||
| 4 | ⑧ | ⑨ | ⑩ | |||||||
(1)画出⑩的原子结构示意图
(2)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,写出甲物质的结构式
(3)元素③⑤对应的最高价氧化物的水化物,写出它们相互之间能发生反应化学方程式
(4)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程
(5)②、⑥分别形成的两种氢化物中,沸点较高的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A和气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:A_______ ,B_______ , E_______ 。
(2)画出E的原子结构示意图________________ 。
写出电子式D2A2______________ ,EB4_____________ 。
(3)比较EA2与EB4的熔点高低(填化学式)_______ >_______ 。
(4)A的氢化物的沸点与同族下一周期元素的氢化物相比,A的氢化物的沸点______ (填“高”或“低”),原因是___________________ 。
(1)写出下列元素的名称:A
(2)画出E的原子结构示意图
写出电子式D2A2
(3)比较EA2与EB4的熔点高低(填化学式)
(4)A的氢化物的沸点与同族下一周期元素的氢化物相比,A的氢化物的沸点
您最近一年使用:0次




