几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A.R的氧化物对应的水化物可能具有两性 |
| B.L、Q形成的简单离子核外电子排布相同 |
| C.T、Q的氢化物的稳定性:Q>T |
| D.L、M的单质中金属键的强弱:L>M |
更新时间:2020-08-20 16:03:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列排列顺序错误的是
| A.金属性Rb>K>Mg>Al | B.非金属性As>S>Cl>F |
| C.稳定性PH3<H2S<HCl | D.半径Na>P>O>F |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验装置正确且能达到相应实验目的的是
 |  |  |  |
| A.制备并收集少量NH3 | B.制备少量O2 | C.制备并检验SO2气体 | D.比较元素非金属性:Cl>C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期元素原子半径与原子序数的关系如图,下列有关说法正确的是
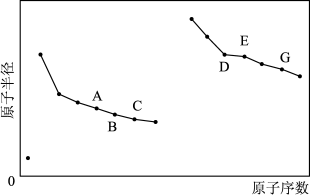
| A.简单氢化物的热稳定性:E>G | B.G的最高价氧化物中含有离子键 |
C.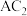 、 、 、 、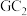 均是酸性氧化物 均是酸性氧化物 | D.简单离子半径大小:D<C |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用 制取金属钾,下列说法正确的是
制取金属钾,下列说法正确的是
 制取金属钾,下列说法正确的是
制取金属钾,下列说法正确的是A.原子半径: |
B.第一电离能: |
C.金属性: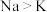 |
D.电解饱和食盐水可以制得金属 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M元素的原子是短周期中原子半径最大的。下列说法正确的是
| A.X、Z、W三元素形成的化合物都是共价化合物 |
| B.简单离子的半径从大到小的顺序是:M>Y>Z>W |
| C.氢化物的稳定性强弱顺序为:Y>Z>W |
| D.M2W2既含有离子键,也含有非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化合物甲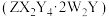 是制药工业和电池材料等的原料,其组成元素W、X、Y、Z是原子序数依次增大的前四周期元素;其中W、X、Y为短周期主族元素,W是元素周期表中原子半径最小的元素,X、Y同周期,且X原子和Y原子的最外层电子数之比为
是制药工业和电池材料等的原料,其组成元素W、X、Y、Z是原子序数依次增大的前四周期元素;其中W、X、Y为短周期主族元素,W是元素周期表中原子半径最小的元素,X、Y同周期,且X原子和Y原子的最外层电子数之比为 ,
, 的电子数比Z原子的电子数多20。化合物甲的热重曲线如图所示。下列说法错误的是
的电子数比Z原子的电子数多20。化合物甲的热重曲线如图所示。下列说法错误的是

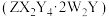 是制药工业和电池材料等的原料,其组成元素W、X、Y、Z是原子序数依次增大的前四周期元素;其中W、X、Y为短周期主族元素,W是元素周期表中原子半径最小的元素,X、Y同周期,且X原子和Y原子的最外层电子数之比为
是制药工业和电池材料等的原料,其组成元素W、X、Y、Z是原子序数依次增大的前四周期元素;其中W、X、Y为短周期主族元素,W是元素周期表中原子半径最小的元素,X、Y同周期,且X原子和Y原子的最外层电子数之比为 ,
, 的电子数比Z原子的电子数多20。化合物甲的热重曲线如图所示。下列说法错误的是
的电子数比Z原子的电子数多20。化合物甲的热重曲线如图所示。下列说法错误的是
A.非金属性: |
| B.X、Y形成的两种常见化合物常温下为气体 |
C.M点时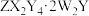 热分解失去2个 热分解失去2个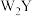 |
D. 时剩余固体的组成可表示为 时剩余固体的组成可表示为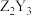 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素叙述正确的是
| A.气态氢化物的稳定性:D>C | B.原子半径:A>B>C>D |
| C.单质的还原性:B>A | D.原子序数:b>a>c>d |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关化学键、氢键和范德华力的叙述中,不正确的是( )
| A.金属键是金属离子与“电子气”之间的强烈作用,金属键无方向性和饱和性 |
| B.共价键是原子之间通过共用电子对形成的化学键,共价键有方向性和饱和性 |
| C.范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大 |
| D.氢键不是化学键而是一种较弱的作用力,所以氢键只存在于分子与分子之间 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.若R2-和M+的电子层结构相同,则原子序数R>M |
| B.非金属性Cl>Br>I,则酸性HCl>HBr>HI |
| C.Li、Na、K的熔点逐渐降低 |
| D.Na2O2固体中的阴离子和阳离子个数比是1:1 |
您最近一年使用:0次

 、
、 、
、 、
、 )的沸点与相对分子质量的关系图,下列说法
)的沸点与相对分子质量的关系图,下列说法