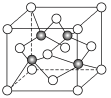
上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED铝片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
(1)镓的基态原子的价电子排布式是_____________ 。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为________ ,与同一个镓原子相连的砷原子构成的立体构型为_________ 。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是______ (用氢化物分子式表示)。
(4)砷化镓可由(CH3)3Ga和AsH3在700 ℃时制得,(CH3)3Ga中镓原子的杂化方式为_______ ,GaAs的熔点为1238 ℃,该晶体的类型为_________ 。
(5)比较二者的第一电离能:As________ Ga(填“<”“>”或“=”)。
(6)下列说法正确的是________ (填字母)。
A. 砷化镓晶胞结构与NaCl相同 B. GaP与GaAs互为等电子体
C. 电负性:As>Ga D. 砷化镓晶体中含有配位键
(7)砷化镓的晶胞结构如上图所示,密度为ρ g·cm-3,相对分子质量为M,其晶胞中Ga原子与As原子最近距离是_________ nm。

(1)镓的基态原子的价电子排布式是
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是
(4)砷化镓可由(CH3)3Ga和AsH3在700 ℃时制得,(CH3)3Ga中镓原子的杂化方式为
(5)比较二者的第一电离能:As
(6)下列说法正确的是
A. 砷化镓晶胞结构与NaCl相同 B. GaP与GaAs互为等电子体
C. 电负性:As>Ga D. 砷化镓晶体中含有配位键
(7)砷化镓的晶胞结构如上图所示,密度为ρ g·cm-3,相对分子质量为M,其晶胞中Ga原子与As原子最近距离是
更新时间:2020-08-05 11:34:10
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】叶绿素是绿色植物进行光合作用所必需的催化剂,其结构如图所示。

(1)基态镁原子的核外电子排布式_______ ,能量最高的电子占据的轨道形状呈_______ 形。根据对角线规则,Mg的一些化学性质与元素_______ 相似。
(2)C、N、O三种非金属元素的第一电离能由大到小顺序是_______ 。
(3)叶绿素分子中,N原子的杂化类型是_______ 。
(4) 的热分解温度
的热分解温度_______ (填“高于”或“低于”) 的原因是
的原因是_______ 。
(5) 具有
具有 型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得
型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得 的晶胞参数为
的晶胞参数为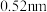 ,晶体密度是
,晶体密度是_______  (设NA为阿伏加德罗常数的值,列出计算式)。
(设NA为阿伏加德罗常数的值,列出计算式)。


(1)基态镁原子的核外电子排布式
(2)C、N、O三种非金属元素的第一电离能由大到小顺序是
(3)叶绿素分子中,N原子的杂化类型是
(4)
 的热分解温度
的热分解温度 的原因是
的原因是(5)
 具有
具有 型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得
型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得 的晶胞参数为
的晶胞参数为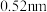 ,晶体密度是
,晶体密度是 (设NA为阿伏加德罗常数的值,列出计算式)。
(设NA为阿伏加德罗常数的值,列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)下列各组物质性质的比较,结论正确的是_______。
(2)下列叙述正确的有_______。
(3)磷酸根离子的空间构型为_______ ,其中P的价层电子对数为_______ ,杂化轨道类型为:_______ 。
(4)苯胺(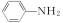 )与甲苯(
)与甲苯(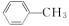 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(5)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X-射线衍射测得化合物R的晶体结构,其局部结构如图所示。

①从结构角度分析,R中两种阳离子的相同之处为_______ ,不同之处为_______ 。(填标号)
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
②R中阴离子N 中的σ键总数为
中的σ键总数为_______ 个。
③图中虚线代表氢键,其表示式为(NH )N—H…Cl、
)N—H…Cl、_______ 。
(1)下列各组物质性质的比较,结论正确的是_______。
| A.分子的极性:BCl3<NCl3 |
| B.Mn的+2价比Fe的+2价稳定 |
| C.物质的沸点:HF<HCl |
| D.在CS2中的溶解度:CCl4<H2O |
| A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7 |
| B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 |
| C.CH2Cl—COOH酸性大于CH3CH2COOH酸性 |
| D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点 |
(4)苯胺(
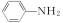 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(5)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X-射线衍射测得化合物R的晶体结构,其局部结构如图所示。

①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
②R中阴离子N
 中的σ键总数为
中的σ键总数为③图中虚线代表氢键,其表示式为(NH
 )N—H…Cl、
)N—H…Cl、
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有四种短周期元素A,B,C,D,已知:①C,D在同一周期,A,B在同一主族;②它们可以组成化合物A2C、B2C2、DC2、D2A4等;③B的阳离子与C的阴离子的核外电子排布相同;④B2C2同A2C或DC2反应都生成气体C2,B与A2C反应生成气体A2,A2与气体C2按体积比2∶1混合后点燃发生爆炸,其产物是一种常温下常见的无色无味的液体。请回答:
(1)写出元素符号:A________ 、B________ 、C________ 、D________ 。
(2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为__________ ;按原子轨道重叠方式,其非极性键的类型是________ 。化合物DC2的结构式__________ 。
(3)A2C分子的电子式____________ ,按原子轨道重叠方式,其共价键的类型是____________ 。D2A4是平面形分子,其分子中含有______ 个σ键,______ 个π键。
(4)写出化学方程式或离子方程式:
B2C2与A2C反应的化学方程式:___________________________________________ ;
B2C2与DC2反应的化学方程式:___________________________________________ ;
B与A2C反应的离子方程式:______________________________________________ 。
(1)写出元素符号:A
(2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为
(3)A2C分子的电子式
(4)写出化学方程式或离子方程式:
B2C2与A2C反应的化学方程式:
B2C2与DC2反应的化学方程式:
B与A2C反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】物质结构决定物质性质,试用物质结构知识解释下列实验事实
(1)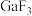 熔点比
熔点比 熔点高很多:
熔点高很多:_______ 。
(2)接近沸点的水蒸气的相对分子质量测定值大于18:_______ 。
(3)向 的
的 溶液中加入浓
溶液中加入浓 溶液,振荡后静置,
溶液,振荡后静置, 层紫色变浅:
层紫色变浅:_______ 。
(4) 分子中
分子中 键角大于
键角大于 分子中
分子中 :
:_______ 。
(5)Mn的第三电离能大于Fe的第三电离能:_______ 。
(1)
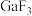 熔点比
熔点比 熔点高很多:
熔点高很多: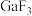 |  | 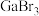 | |
熔点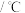 |  | 77.75 | 122.3 |
(3)向
 的
的 溶液中加入浓
溶液中加入浓 溶液,振荡后静置,
溶液,振荡后静置, 层紫色变浅:
层紫色变浅:(4)
 分子中
分子中 键角大于
键角大于 分子中
分子中 :
:(5)Mn的第三电离能大于Fe的第三电离能:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布为msnmpn;③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4;请回答下列问题:
(1)Z2+的核外电子排布式是________ 。
(2)Q、R、Y三种元素的第一电离能数值由小至大的顺序为________ (用元素符号作答)。
(3)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为________ 。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于________ (填晶体类型)。
(1)Z2+的核外电子排布式是
(2)Q、R、Y三种元素的第一电离能数值由小至大的顺序为
(3)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为
(4)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】磷是生物体中不可缺少的元素之一,它能形成多种化合物。
(1)基态磷原子中,电子占据的最高能层符号为___________ ;该能层能量最高的电子云在空间有___________ 个伸展方向,原子轨道呈__________ 形。
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为___________ 。
(3)单质磷与Cl2反应,可以生成PCl3和PCl5.其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为__________ ,其分子的空间构型为____________ 。
(4)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其晶胞,硼原子与磷原子最近的距离为acm。用Mg/mol表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为___________ 。

(5)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为__________ ;PO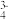 作为
作为_________ 为Fe提供_________ 。
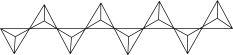
(6)磷酸盐分为直链多磷酸盐、支链状超磷酸盐和环状聚偏磷酸盐三类。某直链多磷酸钠的阴离子呈如图所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连。则该多磷酸钠的化学式为_______ 。
(1)基态磷原子中,电子占据的最高能层符号为
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为
(3)单质磷与Cl2反应,可以生成PCl3和PCl5.其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为
(4)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其晶胞,硼原子与磷原子最近的距离为acm。用Mg/mol表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为

(5)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为
 作为
作为(6)磷酸盐分为直链多磷酸盐、支链状超磷酸盐和环状聚偏磷酸盐三类。某直链多磷酸钠的阴离子呈如图所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连。则该多磷酸钠的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W是原子序数依次增大的前四周期元素。X的三个能级中排布的电子数相等;Y基态原子的未成对电子数与能级数相等;Z位于X的下两个周期,其电离能数据分别是:I1 = 419kJ·mol-1,I2 =" 3051" kJ·mol-1,I3 =" 4411" kJ·mol-1;W3+的核外电子排布式是[Ar]3d5。回答下列问题:
(1)X、Y、Z三种元素电负性由大到小的顺序为_________ 。
(2)X的某种氧化物与Y2互为等电子体,写出该氧化物的结构简式_________ ,该氧化物所含的化学键类型是_________ 。
(3)YH4+的空间构型是_________ 。X原子的杂化方式均为sp2、相对分子质量最小的X的氢化物分子式为_________ 。
(4)四种元素可形成化合物Z4[W(XY)n],W原子的最外层电子数和配体形成配位键时提供的电子数之和为14,则 n ="_________ " 。
(5)下图____ (填“A”、“B”或“C”)表示的是Z晶体中微粒的堆积方式。若Z晶体中一个晶胞的边长为a pm,则Z晶体的密度为____________ (写出含a的表达式,用NA表示阿伏加德罗常数)。

(1)X、Y、Z三种元素电负性由大到小的顺序为
(2)X的某种氧化物与Y2互为等电子体,写出该氧化物的结构简式
(3)YH4+的空间构型是
(4)四种元素可形成化合物Z4[W(XY)n],W原子的最外层电子数和配体形成配位键时提供的电子数之和为14,则 n ="
(5)下图

您最近一年使用:0次
【推荐2】I 锰元素的化合物在多个领域中均有重要应用。
(1)Mn2+基态核外电子排布式为___ ,SO32-分子的空间构型为____ 。
(2)二价锰的3种离子化合物MnCl2、MnS、MnO中晶格能最大的是___ 。
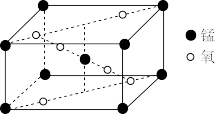
(3)某锰氧化物的晶胞结构如图所示,该氧化物的化学式为___ 。
(4)在配离子[Mn(CN)6]3-中存在的作用力有___ (填字母)。
a. 离子键 b. 共价键 c. 配位键 d. 氢键
II 铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)铜与N2O4在一定条件下可制备无水Cu(NO3)2。
①基态Cu的电子排布式为___ 。
②与NO3-互为等电子体的一种分子为__ (填化学式)。
(2)邻氨基吡啶(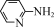 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
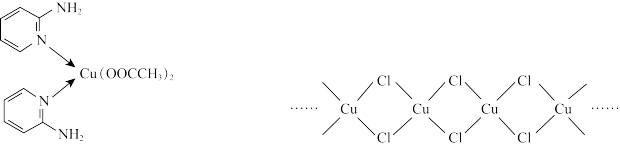
①C、N、O三种元素的第一电离能由大到小的顺序为___ 。
②邻氨基吡啶的铜配合物中,C原子轨道杂化类型为___ 。
③1mol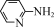 中含有σ键的数目为
中含有σ键的数目为___ mol。
(1)Mn2+基态核外电子排布式为
(2)二价锰的3种离子化合物MnCl2、MnS、MnO中晶格能最大的是
(3)某锰氧化物的晶胞结构如图所示,该氧化物的化学式为

(4)在配离子[Mn(CN)6]3-中存在的作用力有
a. 离子键 b. 共价键 c. 配位键 d. 氢键
II 铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)铜与N2O4在一定条件下可制备无水Cu(NO3)2。
①基态Cu的电子排布式为
②与NO3-互为等电子体的一种分子为
(2)邻氨基吡啶(
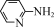 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
①C、N、O三种元素的第一电离能由大到小的顺序为
②邻氨基吡啶的铜配合物中,C原子轨道杂化类型为
③1mol
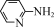 中含有σ键的数目为
中含有σ键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】如表为元素周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)元素②形成的含氧酸中,酸根离子呈正三角形的酸是__________ (填化学式)。
(2)元素②③⑧的第一电离能由大到小的顺序是_________________________ (填元素符号)。
(3)元素④⑥⑦的简单气态氢化物中最稳定的是_______ (填化学式),元素⑤最高价氧化物对应的水化物的化学式为__________ 。
(4)写出元素⑨的基态原子的价电子排布式:________________ 。
(5)将元素⑩的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式__________________________ (必须将配位键表示出来)。
(6)元素①和②形成的分子呈三角锥形的化合物为___________ (填化学式);元素①和③形成的分子中既含有极性共价键,又含有非极性共价键的化合物有___________ (填化学式,写一种)。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | |||||||||||||||
| ⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)元素②形成的含氧酸中,酸根离子呈正三角形的酸是
(2)元素②③⑧的第一电离能由大到小的顺序是
(3)元素④⑥⑦的简单气态氢化物中最稳定的是
(4)写出元素⑨的基态原子的价电子排布式:
(5)将元素⑩的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式
(6)元素①和②形成的分子呈三角锥形的化合物为
您最近一年使用:0次
【推荐1】砷化镓( )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: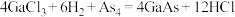 或
或 。
。
(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
(2) 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为_______ , 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是_______ ,写出一种与甲烷互为等电子体的离子的化学式:_______ 。
(3)上述反应涉及的几种元素中,电负性最大的元素是_______ ,砷可形成多种卤化物,其中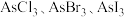 的沸点由低到高的原因为
的沸点由低到高的原因为_______ 。
(4) 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
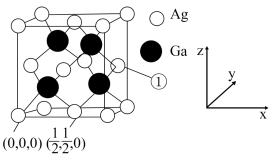
则①处原子的分数坐标为_______ ,已知紧邻的 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的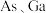 原子之间的距离为
原子之间的距离为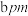 ,则
,则
_______ b,该晶胞的密度为_______  (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
 )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: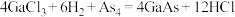 或
或 。
。(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
A.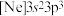 | B. | C.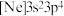 | D.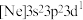 |
 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是(3)上述反应涉及的几种元素中,电负性最大的元素是
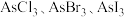 的沸点由低到高的原因为
的沸点由低到高的原因为(4)
 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
则①处原子的分数坐标为
 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的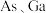 原子之间的距离为
原子之间的距离为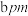 ,则
,则
 (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为_______ ,它位于元素周期表的_______ 区。
(2)元素A、B、C中,电负性最大的是_______ (填元素符号,下同),元素B、C、D第一电离能由大到小的顺序为_______ 。
(3)与同族其他元素X形成的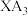 相比,
相比, 易液化的原因是
易液化的原因是_______ 。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ , 离子的空间结构为
离子的空间结构为_______ 。
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为_______  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)E的元素名称为
(2)元素A、B、C中,电负性最大的是
(3)与同族其他元素X形成的
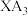 相比,
相比, 易液化的原因是
易液化的原因是(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 离子的空间结构为
离子的空间结构为(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为
 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁及其化合物有重要的用途:Fe能与CO形成配合物五羰基铁化合物Fe(CO)5,加热分解成CO和Fe,得到的铁为葱头状结构的铁粉,其稳定性好,磁导率高,是一种应用广泛的吸波材料。回答下列问题:
(1)基态Fe原子的价电子排布式为_______ ;通常情况下,铁的+2价化合物没有+3价的稳定,请从核外电子排布的角度解释其原因:_______ 。
(2)五羰基铁Fe(CO)5:熔点20.3℃,沸点103.6℃,固态五羰基铁属于_______ 晶体(填晶体类型);1molFe(CO)5中含有_______ molσ键
(3)血液中运输氧气的血红素又称为亚铁血红素,是Fe2+形成的卟啉配合物,结构如下图所示:
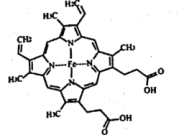
则1mol该配合物中配位原子有_______ mol,碳原子的杂化轨道方式为_______ ;组成该物质的4种非金属元素的第一电离能大小关系为_______ 。
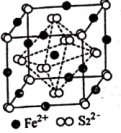
(4)我国生产硫酸所用的原料主要是黄铁矿(主要成分是FeS2),FeS2晶体的晶胞如下图所示。晶胞边长为anm、FeS2的摩尔质量为Mg∙mol-1,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_______ g∙cm-3。
(1)基态Fe原子的价电子排布式为
(2)五羰基铁Fe(CO)5:熔点20.3℃,沸点103.6℃,固态五羰基铁属于
(3)血液中运输氧气的血红素又称为亚铁血红素,是Fe2+形成的卟啉配合物,结构如下图所示:

则1mol该配合物中配位原子有
(4)我国生产硫酸所用的原料主要是黄铁矿(主要成分是FeS2),FeS2晶体的晶胞如下图所示。晶胞边长为anm、FeS2的摩尔质量为Mg∙mol-1,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为

您最近一年使用:0次



