 、
、 、
、 、
、 、
、 五种分属于不同主族的短周期元素,原子序数依次增大,
五种分属于不同主族的短周期元素,原子序数依次增大, 的气态氢化物分子中只有一对孤电子对;
的气态氢化物分子中只有一对孤电子对; 的原子半径是短周期中最大的,
的原子半径是短周期中最大的, 的离子半径是第三周期元素形成的简单离子半径中最小的,
的离子半径是第三周期元素形成的简单离子半径中最小的, 的最外层p轨道上有一对成对电子。
的最外层p轨道上有一对成对电子。(1)
 在周期表中的位置是
在周期表中的位置是(2)
 、
、 、
、 的电负性大小顺序为
的电负性大小顺序为(3)
 的最高正价氧化物的分子构型为
的最高正价氧化物的分子构型为 杂化轨道类型为
杂化轨道类型为(4)将
 的单质与
的单质与 的最高价氧化物对应的水化物混合,其反应的离子方程式为:
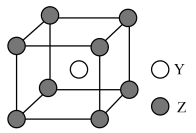
的最高价氧化物对应的水化物混合,其反应的离子方程式为:(5)如图所示为
 、
、 形成的合金晶胞结构,如果将含
形成的合金晶胞结构,如果将含 的该合金置于足量的水中充分反应,放出标准状况下气体的体积为
的该合金置于足量的水中充分反应,放出标准状况下气体的体积为 。
。
更新时间:2020-08-26 18:07:16
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】最近我国科研人员成功攻克了 通信芯片制造中关键材料氮化镓
通信芯片制造中关键材料氮化镓 的研制难题.已知元素镓
的研制难题.已知元素镓 与
与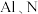 与
与 分别是同主族的元素,请回答下列问题:
分别是同主族的元素,请回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为
_________ 。
(2)根据元素周期律,元素的电负性
________ (填“大于”或“小于”,下同) ;
;
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与_______ 个氮原子相连,氮化铝晶体属于________ 晶体。
(4) 是氮的氢化物,中心原子的杂化方式是
是氮的氢化物,中心原子的杂化方式是_________ , 的沸点比
的沸点比 高的原因是
高的原因是_______ 。
(5) 可采用
可采用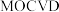 (金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与
(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与 发生系列反应得到
发生系列反应得到 和另一种产物,该过程的化学方程式为:
和另一种产物,该过程的化学方程式为:____________________________ 。
(6)原子晶体 的晶胞参数
的晶胞参数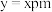 ,它的晶胞结构如下图所示,该晶胞内部存在的共价键数为
,它的晶胞结构如下图所示,该晶胞内部存在的共价键数为_________ ;紧邻的 原子之间的距离为a,紧邻的
原子之间的距离为a,紧邻的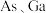 原子之间的距离为b,则
原子之间的距离为b,则
_________ .该晶胞的密度为__________  (阿伏加德罗常数用
(阿伏加德罗常数用 表示)。
表示)。
 通信芯片制造中关键材料氮化镓
通信芯片制造中关键材料氮化镓 的研制难题.已知元素镓
的研制难题.已知元素镓 与
与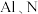 与
与 分别是同主族的元素,请回答下列问题:
分别是同主族的元素,请回答下列问题:(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为
(2)根据元素周期律,元素的电负性

 ;
;(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与
(4)
 是氮的氢化物,中心原子的杂化方式是
是氮的氢化物,中心原子的杂化方式是 的沸点比
的沸点比 高的原因是
高的原因是(5)
 可采用
可采用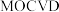 (金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与
(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与 发生系列反应得到
发生系列反应得到 和另一种产物,该过程的化学方程式为:
和另一种产物,该过程的化学方程式为:(6)原子晶体
 的晶胞参数
的晶胞参数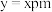 ,它的晶胞结构如下图所示,该晶胞内部存在的共价键数为
,它的晶胞结构如下图所示,该晶胞内部存在的共价键数为 原子之间的距离为a,紧邻的
原子之间的距离为a,紧邻的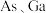 原子之间的距离为b,则
原子之间的距离为b,则
 (阿伏加德罗常数用
(阿伏加德罗常数用 表示)。
表示)。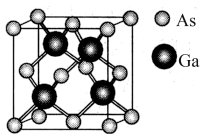
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:_______ ;B、N、H的电负性由大到小的顺序为_______ 。
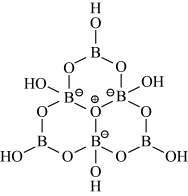
(2)科学家合成了一种含硼阴离子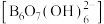 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(3) 与
与 结合形成固态化合物
结合形成固态化合物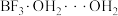 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出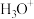 和一种含硼阴离子
和一种含硼阴离子_______ (填离子符号);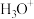 空间构型为
空间构型为_______ 。
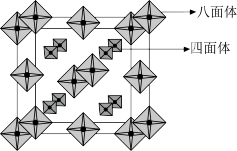
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体晶胞棱边夹角均为90°,棱长为apm,密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①该晶体的化学式为_______ 。
②金属M的相对原子质量为_______ (列出表达式)。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
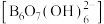 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物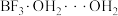 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出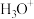 和一种含硼阴离子
和一种含硼阴离子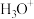 空间构型为
空间构型为(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体晶胞棱边夹角均为90°,棱长为apm,密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。①该晶体的化学式为
②金属M的相对原子质量为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D、E、W是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E4+与氩原子的核外电子排布相同。W是第四周期d区原子序数最大的元素。请回答下列问题:
(1)填元素名称, C:________ 写出E的价层电子排布式_________ ,W在周期表中的位置:___________________
第二周期基态原子未成对电子数与W相同且电负性最小的元素是________ (填元素符号).
(2)W(BD)n为无色挥发性剧毒液体,熔点﹣25℃,沸点43℃.不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,W(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=________ ,BD分子的结构式是________
(3)3﹣氯﹣2﹣丁氨酸的结构简式为: ,一个该有机物分子中含有
,一个该有机物分子中含有_____ 个手性碳原子.
(1)填元素名称, C:
第二周期基态原子未成对电子数与W相同且电负性最小的元素是
(2)W(BD)n为无色挥发性剧毒液体,熔点﹣25℃,沸点43℃.不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,W(BD)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(3)3﹣氯﹣2﹣丁氨酸的结构简式为:
 ,一个该有机物分子中含有
,一个该有机物分子中含有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】主族元素N、P、As、Se、Cl等的某些化合物对工农业生产意义重大,回答下列问题:
(1)N、P、As电负性由大到小的顺序为_______ ,As的第一电离能比Se的第一电离能大的原因为_______
(2)阿散酸(如图)是一种饲料添加剂,能溶于NaOH溶液中,常含有H3AsO3、NaCl等杂质,该结构中N的杂化方式为_______ ,AsO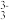 的空间构型为
的空间构型为_______

(3)液氨可作制冷剂,汽化时吸收大量的热的原因是_______
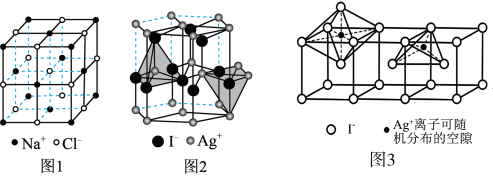
(4)NaCl晶体与Na或Cl2在50~300 GPa的高压下反应,可以形成不同的晶体,其中一种晶体的晶胞如图1所示,该晶体的化学式为_______

(5)CrCl3能与H2O、NH3形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为_______ 。
(1)N、P、As电负性由大到小的顺序为
(2)阿散酸(如图)是一种饲料添加剂,能溶于NaOH溶液中,常含有H3AsO3、NaCl等杂质,该结构中N的杂化方式为
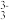 的空间构型为
的空间构型为
(3)液氨可作制冷剂,汽化时吸收大量的热的原因是
(4)NaCl晶体与Na或Cl2在50~300 GPa的高压下反应,可以形成不同的晶体,其中一种晶体的晶胞如图1所示,该晶体的化学式为

(5)CrCl3能与H2O、NH3形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1,1mol该配合物溶于水,加入足量的硝酸银溶液可得430.5g白色沉淀,则该配合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】卤族元素的单质和化合物在生产生活中有重要的用途。请回答:
(1)卤素元素位于元素周期表的___________ 区,溴原子的原子核外有___________ 种不同运动状态的电子,其M能层电子排布式为___________ 。
(2) 中心原子的杂化类型为
中心原子的杂化类型为___________ , 的空间构型为
的空间构型为___________ 。
(3)一定条件下 与
与 以物质的量之比为
以物质的量之比为 混舍得到一种固态离子化合物,其结构组成可能为:(a)
混舍得到一种固态离子化合物,其结构组成可能为:(a)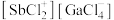 或(b)
或(b)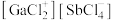 ,该离子化合物最可能的结构组成为
,该离子化合物最可能的结构组成为___________ (填“a”或“b”),理由是___________ 。
(4)在离子晶体中,当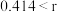 (阳离子)
(阳离子)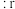 (阴离子)
(阴离子)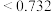 时,
时, 型化合物往往采用和
型化合物往往采用和 晶体相同的晶体结构(如下图1)。已知
晶体相同的晶体结构(如下图1)。已知 ,但在室温下,
,但在室温下, 的晶体结构如下图2所示,称为六方碘化银。
的晶体结构如下图2所示,称为六方碘化银。 的配位数为
的配位数为___________ ,造成 晶体结构不同于
晶体结构不同于 晶体结构的原因不可能是
晶体结构的原因不可能是___________ 。
a.几何因素 b.电荷因素 c.键性因素
若六方碘化银晶胞底边边长为 ,高为
,高为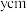 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,碘化银晶体的密度为
,碘化银晶体的密度为___________ 列出计算式。
(5)当温度处于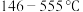 间时,六方碘化银转化为
间时,六方碘化银转化为 (如图3),
(如图3), 可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在
可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在 晶体中,
晶体中, (八面体空隙):n(四面体空隙)=
(八面体空隙):n(四面体空隙)=___________ 。
(1)卤素元素位于元素周期表的
(2)
 中心原子的杂化类型为
中心原子的杂化类型为 的空间构型为
的空间构型为(3)一定条件下
 与
与 以物质的量之比为
以物质的量之比为 混舍得到一种固态离子化合物,其结构组成可能为:(a)
混舍得到一种固态离子化合物,其结构组成可能为:(a)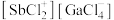 或(b)
或(b)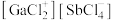 ,该离子化合物最可能的结构组成为
,该离子化合物最可能的结构组成为(4)在离子晶体中,当
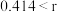 (阳离子)
(阳离子)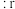 (阴离子)
(阴离子)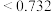 时,
时, 型化合物往往采用和
型化合物往往采用和 晶体相同的晶体结构(如下图1)。已知
晶体相同的晶体结构(如下图1)。已知 ,但在室温下,
,但在室温下, 的晶体结构如下图2所示,称为六方碘化银。
的晶体结构如下图2所示,称为六方碘化银。 的配位数为
的配位数为 晶体结构不同于
晶体结构不同于 晶体结构的原因不可能是
晶体结构的原因不可能是a.几何因素 b.电荷因素 c.键性因素
若六方碘化银晶胞底边边长为
 ,高为
,高为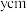 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,碘化银晶体的密度为
,碘化银晶体的密度为
(5)当温度处于
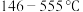 间时,六方碘化银转化为
间时,六方碘化银转化为 (如图3),
(如图3), 可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在
可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在 晶体中,
晶体中, (八面体空隙):n(四面体空隙)=
(八面体空隙):n(四面体空隙)=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】现有周期表中前四周期的五种元素A、B、C、D、E,其中A、B、C为金属且位于同一周期,原子序数C>B>A;A、C核外均没有未成对电子;B被誉为“21世纪的金属”,B原子核外有二个未成对电子和三个空轨道;D原子最外层电子数是其周期序数的三倍;E能与D形成化合物ED2,可用于自来水的消毒。
(1)B元素基态原子的电子排布式为_______ ,E元素在周期表中的位置为_______ 。
(2)化合物E2D分子的立体构型为________ ,中心原子采用_______ 杂化。
(3)B与E能形成一种化合物BE4,其熔点:-25℃,沸点:136.4℃。则该化合物属于____ 晶体,晶体内含有的作用力类型有_______ 。
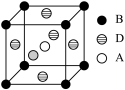
(4)A、B、D三种元素形成的某晶体的晶胞结构如图,则晶体的化学式为______ 。若最近的B 与D的原子距离为acm,该物质的摩尔质量为Mg/mol,阿伏伽德罗常数的数值为NA,则该晶体的密度为_______ g/cm3。
(1)B元素基态原子的电子排布式为
(2)化合物E2D分子的立体构型为
(3)B与E能形成一种化合物BE4,其熔点:-25℃,沸点:136.4℃。则该化合物属于
(4)A、B、D三种元素形成的某晶体的晶胞结构如图,则晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】甲烷作为天然气、页岩气、可燃冰的主要成分,拥有最稳定的烷烃分子结构,具有高度的四面体对称性,极难在温和的条件下对其活化。因此,甲烷的选择活化和定向转化一直是世界性的难题。我国科学家经过长达6年的努力,研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂材料,在室温条件下以H2O2为氧化剂直接将甲烷氧化成C1(只含一个C原子)含氧化合物,被业内认为是甲烷化学领域的重要突破。请回答下列问题:
(1)基态Cu原子的外围电子排布式为_________ 。
(2)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力________ (填“减弱”或“不变”);铁晶体中粒子之间的作用力类型是_______ 。
(3)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①CH3OH、HCHO、HCOOH的沸点分别为64.7℃、-195℃、100.8℃,其主要原因是_______ ;
②CH4和HCHO比较,键角较大的是________ ,主要原因是_______ 。
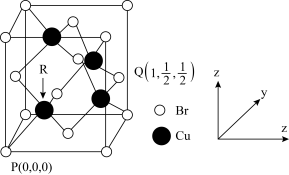
(4)一种铜的溴化物晶胞结构如图所示,与溴紧邻的溴原子数目是______ ;由图中P和Q点原子坐标参数可确定R点的原子坐标参数为________ 。
(4)钴晶胞和白铜(铜镍合金)晶胞分别如图所示。
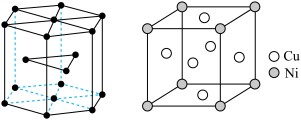
①钴晶胞堆积方式的名称为________ ;
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加 德罗常数的值。晶胞中两个面心上铜原子最短核间距为_______ pm(列出计算式)。
(1)基态Cu原子的外围电子排布式为
(2)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力
(3)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①CH3OH、HCHO、HCOOH的沸点分别为64.7℃、-195℃、100.8℃,其主要原因是
②CH4和HCHO比较,键角较大的是
(4)一种铜的溴化物晶胞结构如图所示,与溴紧邻的溴原子数目是

(4)钴晶胞和白铜(铜镍合金)晶胞分别如图所示。

①钴晶胞堆积方式的名称为
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加 德罗常数的值。晶胞中两个面心上铜原子最短核间距为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氮族元素在工业、农业上应用广泛。请回答下列问题:
(1)基态P原子中,电子占据的最高能层符号为____ ,氮族元素中原子序数最大的非金属元素基态原子的核外电子排布式是____ 。
(2)NCl3的分子构型是____ ,请任写出一种与NCl3互为等电子体的离子的化学式:____ ,已知键角:NCl3< NH3,原因是____ 。
(3)PCl3可与过渡金属形成配合物,已知过渡金属配合物的中心原子价电子数与配体提供电子总数之和为18,则计算1mol配合物Ni(PCl3)x中的σ键的数目是____ 。
(4)碳和磷的有关化学键键能如表所示,试从键能方面简要分析和解释下列有关事实:
磷也有系列氢化物,但其氢化物在种类和数量上都远不如烷烃多,原因是___ 。
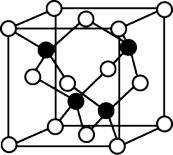
(5)As与Ga形成的化合物是一种良好的导体,其晶胞结构如图(白球为As,黑球为Ga,且Ga填充正四面体空隙),则该化合物的化学式是____ ,若该物质的密度为ρg/cm3,阿伏加德罗常数用NA表示,则As与Ga之间最近的距离是___ pm。
(1)基态P原子中,电子占据的最高能层符号为
(2)NCl3的分子构型是
(3)PCl3可与过渡金属形成配合物,已知过渡金属配合物的中心原子价电子数与配体提供电子总数之和为18,则计算1mol配合物Ni(PCl3)x中的σ键的数目是
(4)碳和磷的有关化学键键能如表所示,试从键能方面简要分析和解释下列有关事实:
| 化学键 | C—C | C—H | P—P | P—H |
| 键能/(kJ·mol-1) | 356 | 413 | 213 | 312 |
磷也有系列氢化物,但其氢化物在种类和数量上都远不如烷烃多,原因是
(5)As与Ga形成的化合物是一种良好的导体,其晶胞结构如图(白球为As,黑球为Ga,且Ga填充正四面体空隙),则该化合物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
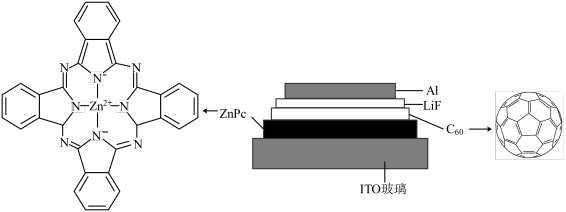
【推荐3】我国科学家制备了一种 太阳电池,其结构示意图如下。
太阳电池,其结构示意图如下。
(1)铝元素属于______ 区(填“s”“d”“ds”或“p”)。
(2) 分子中60个碳原子都是等价的,均以近似
分子中60个碳原子都是等价的,均以近似_____ 杂化的方式形成3个不共平面的 键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,
键,余下的1个p轨道电子互相重叠形成闭壳层电子结构, 电子云分布在
电子云分布在 分子笼的内外层表面上。循环伏安测试表明:
分子笼的内外层表面上。循环伏安测试表明: 在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
(3)① 中基态
中基态 的电子排布式为
的电子排布式为_______ 。
② 中存在配位键的原因是
中存在配位键的原因是________ 。
(4)某溶剂中, 可以和
可以和 形成分子间电荷转移复合物,反应方程式可表示为:
形成分子间电荷转移复合物,反应方程式可表示为: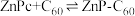 ,不同温度下生成电荷转移复合物的平衡常数如下表。
,不同温度下生成电荷转移复合物的平衡常数如下表。
反应: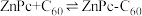

____ 0(填“>”或。“<”),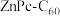 中
中 是电子
是电子_____ (填“给体”或“受体”)。
(5) 晶体结构属于氯化钠型,其晶胞结构如图所示。
晶体结构属于氯化钠型,其晶胞结构如图所示。

① 的熔点和沸点比
的熔点和沸点比 的高,请解释原因
的高,请解释原因________ 。
② 晶体的密度约为
晶体的密度约为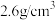 ,
, 晶胞的体积约为
晶胞的体积约为______  (计算结果保留一位有效数字)。
(计算结果保留一位有效数字)。
③一种 的晶胞如图所示。
的晶胞如图所示。
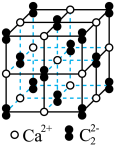
 晶体属于
晶体属于_____ (填晶体类型)晶体,每个 在
在____ 个阴离子构成的多面体中心。一个 晶胞中,含有
晶胞中,含有____ 个 键和
键和____ 个 键。
键。
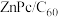 太阳电池,其结构示意图如下。
太阳电池,其结构示意图如下。
(1)铝元素属于
(2)
 分子中60个碳原子都是等价的,均以近似
分子中60个碳原子都是等价的,均以近似 键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,
键,余下的1个p轨道电子互相重叠形成闭壳层电子结构, 电子云分布在
电子云分布在 分子笼的内外层表面上。循环伏安测试表明:
分子笼的内外层表面上。循环伏安测试表明: 在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。(3)①
 中基态
中基态 的电子排布式为
的电子排布式为②
 中存在配位键的原因是
中存在配位键的原因是(4)某溶剂中,
 可以和
可以和 形成分子间电荷转移复合物,反应方程式可表示为:
形成分子间电荷转移复合物,反应方程式可表示为: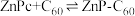 ,不同温度下生成电荷转移复合物的平衡常数如下表。
,不同温度下生成电荷转移复合物的平衡常数如下表。| 温度 | 生成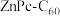 的K 的K |
 | 1.2329 |
 | 0.9674 |
 | 0.4923 |
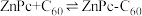

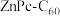 中
中 是电子
是电子(5)
 晶体结构属于氯化钠型,其晶胞结构如图所示。
晶体结构属于氯化钠型,其晶胞结构如图所示。
①
 的熔点和沸点比
的熔点和沸点比 的高,请解释原因
的高,请解释原因②
 晶体的密度约为
晶体的密度约为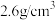 ,
, 晶胞的体积约为
晶胞的体积约为 (计算结果保留一位有效数字)。
(计算结果保留一位有效数字)。③一种
 的晶胞如图所示。
的晶胞如图所示。
 晶体属于
晶体属于 在
在 晶胞中,含有
晶胞中,含有 键和
键和 键。
键。
您最近一年使用:0次



