A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):A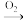 B
B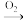 C
C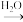 D。
D。
(1)若A是黄色晶体,B为酸雨的成因之一,且可使品红溶液褪色,则将B通入KMnO4溶液的现象为:________________ ;体现B的________ (填“氧化性”“还原性”“漂白性”);请写出D的浓溶液与单质铜反应的化学方程式:________________________________ ;此反应中作氧化剂的D与参加反应的D的物质的量之比为:______________ ;
(2)若A气体可使湿润的红色石蕊试纸变蓝,常温下D的浓溶液能使金属Fe、Al钝化,请写出实验室制备A的化学方程式:__________________________________ ;请写出A→B的化学方程式:______________________________________ ;请写出C→D的离子方程式:__________________________________________ 。
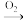 B
B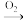 C
C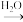 D。
D。(1)若A是黄色晶体,B为酸雨的成因之一,且可使品红溶液褪色,则将B通入KMnO4溶液的现象为:
(2)若A气体可使湿润的红色石蕊试纸变蓝,常温下D的浓溶液能使金属Fe、Al钝化,请写出实验室制备A的化学方程式:
更新时间:2020-09-06 15:01:54
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:
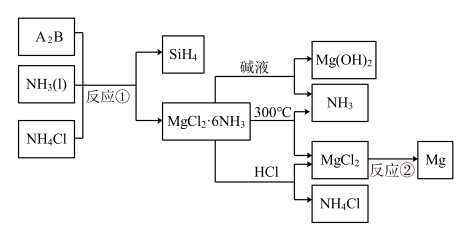
(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):_______________ ,Mg在元素周期表中的位置:_____________________ ,Mg(OH)2的电子式:____________________ 。
(2)A2B的化学式为_______________ 。反应②的必备条件是_______________ 。上图中可以循环使用的物质有_______________ 。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料_______________ (写化学式)。

(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):
(2)A2B的化学式为
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】正盐A能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、②、④、⑤为无色气体,⑥为红棕色气体。
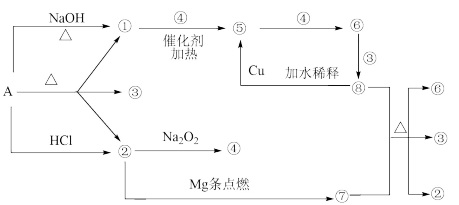
请完成下列各题:
(1)写出化学式A___________ ⑥___________ ⑦___________
(2)写出下列反应方程式:
⑧+⑦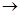 ②+③+⑥:
②+③+⑥:___________
①+④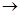 ⑤:
⑤:___________
(3)⑧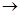 ⑤的离子方程式为:
⑤的离子方程式为:___________

请完成下列各题:
(1)写出化学式A
(2)写出下列反应方程式:
⑧+⑦
 ②+③+⑥:
②+③+⑥:①+④
 ⑤:
⑤:(3)⑧
 ⑤的离子方程式为:
⑤的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
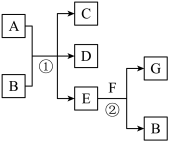
【推荐1】下图中的每一个方格表示有关的一种反应物或生成物,其中X为酸式盐,A是能使澄清石灰水变浑浊的无色无味气体,C是能使湿润的红色的石蕊试纸变蓝的无色气体,请回答:
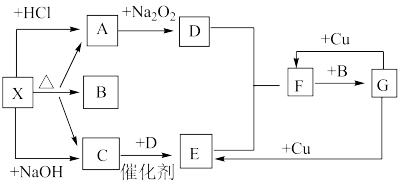
(1)写出A的电子式__________________ 。干燥C所用药品是_______________ 。
(2)X形成的化合物为________ 化合物(填“离子”或“共价”);检验X 中阳离子的方
法是_____________________________________________________________________
(3)写出反应的化学方程式
C→E:_______________________________________________________
F→G:______________________________________________________
(4)X与足量烧碱反应的离子方程式__________________________________________________

(1)写出A的电子式
(2)X形成的化合物为
法是
(3)写出反应的化学方程式
C→E:
F→G:
(4)X与足量烧碱反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】工业废水中的氨氨(以NH3、 形式存在),可通过微生物法或氧化法处理,使水中氨氮达到国家规定的排放标准。
形式存在),可通过微生物法或氧化法处理,使水中氨氮达到国家规定的排放标准。
(1)微生物法:(酸性废水中的部分 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 ,
, 作用生成N2。
作用生成N2。
① 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
② 与
与 在转化为N2的反应中消耗
在转化为N2的反应中消耗 与
与 的物质的量之比为
的物质的量之比为___________ 。
(2)次氯酸钠氧化法:向氨氮废水中加入NaClO,氨氮转化为N2而除去。NaClO氧化NH3的离子方程式为___________ 。
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,·OH为羟基自由基,其氧化性比O3更强。

活性炭奥氧氧化氨氮的机理可描述为___________ 。
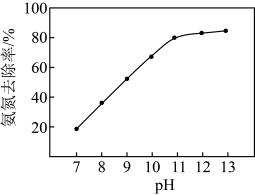
②其它条件不变调节废水的pH,废水中氨氮去除率随pH的变化如题17图-3所示。随pH增大氨氮去除率先明显增大,后变化较小,可能的原因是___________ 。
 形式存在),可通过微生物法或氧化法处理,使水中氨氮达到国家规定的排放标准。
形式存在),可通过微生物法或氧化法处理,使水中氨氮达到国家规定的排放标准。(1)微生物法:(酸性废水中的部分
 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 ,
, 作用生成N2。
作用生成N2。①
 转化为
转化为 的离子方程式为
的离子方程式为②
 与
与 在转化为N2的反应中消耗
在转化为N2的反应中消耗 与
与 的物质的量之比为
的物质的量之比为(2)次氯酸钠氧化法:向氨氮废水中加入NaClO,氨氮转化为N2而除去。NaClO氧化NH3的离子方程式为
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,·OH为羟基自由基,其氧化性比O3更强。

活性炭奥氧氧化氨氮的机理可描述为
②其它条件不变调节废水的pH,废水中氨氮去除率随pH的变化如题17图-3所示。随pH增大氨氮去除率先明显增大,后变化较小,可能的原因是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组同学欲探究NH3催化氧化反应,按下图装置进行实验。

A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)NH3催化氧化的化学方程式是___________ 。
(2)装置B中产生气体的原因有(结合化学用语解释)___________ 。
(3)甲乙两同学分别按上述装置进行实验。一段时间后,装置G中溶液都变成蓝色。
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是___________ 。
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)___________ 。
③用离子方程式解释装置G中溶液变成蓝色的原因:___________ 。
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
①甲认为可调节K1和K2控制A、B装置中的产气量,应(填“增加”或“减少”)___________ 装置A中的产气量,或(填“增加”或“减少”)___________ 装置B中的产气量。
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号)___________ 。
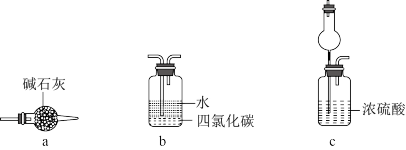
(5)将一定量的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

①打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中,Y管中现象___________ 。
②将注射器活塞退回原处并固定,待装置恢复到室温,打开K2后的实验现象___________ 。

A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)NH3催化氧化的化学方程式是
(2)装置B中产生气体的原因有(结合化学用语解释)
(3)甲乙两同学分别按上述装置进行实验。一段时间后,装置G中溶液都变成蓝色。
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式)
③用离子方程式解释装置G中溶液变成蓝色的原因:
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
①甲认为可调节K1和K2控制A、B装置中的产气量,应(填“增加”或“减少”)
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号)

(5)将一定量的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

①打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中,Y管中现象
②将注射器活塞退回原处并固定,待装置恢复到室温,打开K2后的实验现象
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)工业合成氨是制取氮肥的基础。合成氨反应中,反应物 N2的结构式是_______________ ,产物NH3的电子式是_________________ 。
(2)某小组在实验室模拟以 NH3为原料, 制备少量硝态氮肥 Ca(NO3)2,转化途径如下(转化所需试剂及条件已略去)。
NH3 NO
NO NO2
NO2 HNO3
HNO3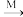 Ca(OH3)2
Ca(OH3)2
①NO→NO2的现象是______________ , NO2→HNO3的化学方程式为____________________ 。
②将HNO3转化为 Ca(NO3)2,列举两种不同类别的化合物 M___________________ (写化学式) 。
(3)①NH4HCO3是一种铵态氮肥,需阴凉处保存,原因是_______________ (写化学方程式)。
②实验室检验某化肥是铵态氮肥,检验过程中发生反应的离子方程式为___________________ 。
(4)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)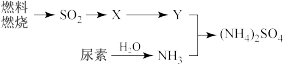
①X可能是SO3 或_______________ ,Y是_____________ 。
②尿素CO(NH2)2是一种常用有机氮肥,缓慢与 H2O 发生非氧化还原反应释放出NH3和另外一种气体,该反应的化学方程式为________________ 。
(1)工业合成氨是制取氮肥的基础。合成氨反应中,反应物 N2的结构式是
(2)某小组在实验室模拟以 NH3为原料, 制备少量硝态氮肥 Ca(NO3)2,转化途径如下(转化所需试剂及条件已略去)。
NH3
 NO
NO NO2
NO2 HNO3
HNO3 Ca(OH3)2
Ca(OH3)2①NO→NO2的现象是
②将HNO3转化为 Ca(NO3)2,列举两种不同类别的化合物 M
(3)①NH4HCO3是一种铵态氮肥,需阴凉处保存,原因是
②实验室检验某化肥是铵态氮肥,检验过程中发生反应的离子方程式为
(4)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
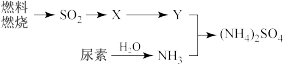
①X可能是SO3 或
②尿素CO(NH2)2是一种常用有机氮肥,缓慢与 H2O 发生非氧化还原反应释放出NH3和另外一种气体,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】连二亚硫酸钠 又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
Ⅰ.查阅材料
i.连二亚硫酸钠 是一种白色粉末,易溶于水,难溶于乙醇。
是一种白色粉末,易溶于水,难溶于乙醇。
ii.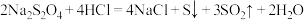
iii.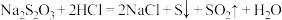
II.制备方法
 ℃时将甲酸钠和纯碱加入乙醇水溶液中,通入
℃时将甲酸钠和纯碱加入乙醇水溶液中,通入 进行反应,完成其反应方程式:
进行反应,完成其反应方程式:_____ 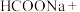
______ 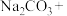
______ = ______ 
______ 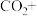
____ ,冷却至40℃~45℃,过滤,用 ______ 洗涤,干燥制得 ;
;
III. 的性质
的性质
(1) 溶液在空气中易被氧化,课题小组测定
溶液在空气中易被氧化,课题小组测定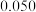

 溶液在空气中pH变化如图:
溶液在空气中pH变化如图: 段主要生成
段主要生成 ,根据pH变化图,
,根据pH变化图, 的电离平衡
的电离平衡 ______ 水解平衡 填“
填“ ”或“
”或“ ”
” ,课题小组推测
,课题小组推测 溶液在空气中易被氧化,
溶液在空气中易被氧化, 发生离子反应方程式为
发生离子反应方程式为 ______  时溶液中主要阴离子符号是
时溶液中主要阴离子符号是 ______ 。
(2)隔绝空气加热 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和气体为
和气体为 ______  填化学式
填化学式 请你设计实验验证产物有
请你设计实验验证产物有 存在,完成下表中内容.
存在,完成下表中内容. 供选择的试剂:稀盐酸、稀硝酸、
供选择的试剂:稀盐酸、稀硝酸、 溶液、
溶液、 溶液
溶液
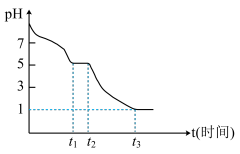
 又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。Ⅰ.查阅材料
i.连二亚硫酸钠
 是一种白色粉末,易溶于水,难溶于乙醇。
是一种白色粉末,易溶于水,难溶于乙醇。ii.
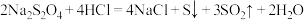
iii.
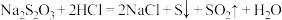
II.制备方法
 ℃时将甲酸钠和纯碱加入乙醇水溶液中,通入
℃时将甲酸钠和纯碱加入乙醇水溶液中,通入 进行反应,完成其反应方程式:
进行反应,完成其反应方程式: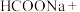
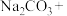

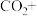
 ;
;III.
 的性质
的性质(1)
 溶液在空气中易被氧化,课题小组测定
溶液在空气中易被氧化,课题小组测定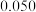

 溶液在空气中pH变化如图:
溶液在空气中pH变化如图: 段主要生成
段主要生成 ,根据pH变化图,
,根据pH变化图, 的电离平衡
的电离平衡  填“
填“ ”或“
”或“ ”
” ,课题小组推测
,课题小组推测 溶液在空气中易被氧化,
溶液在空气中易被氧化, 发生离子反应方程式为
发生离子反应方程式为 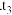 时溶液中主要阴离子符号是
时溶液中主要阴离子符号是 (2)隔绝空气加热
 固体完全分解得到固体产物
固体完全分解得到固体产物 、
、 和气体为
和气体为  填化学式
填化学式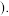 请你设计实验验证产物有
请你设计实验验证产物有 存在,完成下表中内容.
存在,完成下表中内容. 供选择的试剂:稀盐酸、稀硝酸、
供选择的试剂:稀盐酸、稀硝酸、 溶液、
溶液、 溶液
溶液
实验步骤 不要求写出具体操作过程 不要求写出具体操作过程 | 预期的实验现象和结论 |
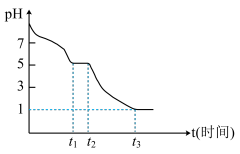
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】煤是我国重要的化石燃料。
(1)煤液化过程中产生的 可生产硫酸,部分过程如图所示:
可生产硫酸,部分过程如图所示:
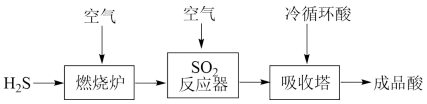
 反应器中的化学方程式是
反应器中的化学方程式是_______ 。
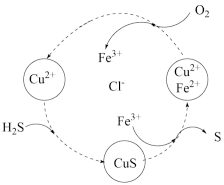
(2) 还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有
还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有_______ ,该图示总反应的化学方程式为_______ 。
(3)煤燃烧产生的废气中含有 ,可以用工业废碱渣(主要成分为
,可以用工业废碱渣(主要成分为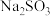 )来吸收,还可以得到亚硫酸钠(
)来吸收,还可以得到亚硫酸钠(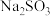 )粗品。其流程如图:
)粗品。其流程如图:
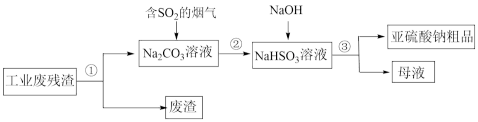
①上述流程中,加入NaOH后,发生反应的化学方程式为_______ 。
②亚硫酸钠粗品中含有少量 ,设计实验证明亚硫酸钠粗品含有少量
,设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有 。
。
(4)已知有VL(已换算成标准状况)尾气,通入足量 吸收再加足量
吸收再加足量 溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。 吸收
吸收 的化学方程式是
的化学方程式是_______ ;尾气中 的含量(体积分数)的计算式是
的含量(体积分数)的计算式是_______ 。
(1)煤液化过程中产生的
 可生产硫酸,部分过程如图所示:
可生产硫酸,部分过程如图所示:
 反应器中的化学方程式是
反应器中的化学方程式是(2)
 还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有
还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有
(3)煤燃烧产生的废气中含有
 ,可以用工业废碱渣(主要成分为
,可以用工业废碱渣(主要成分为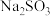 )来吸收,还可以得到亚硫酸钠(
)来吸收,还可以得到亚硫酸钠(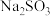 )粗品。其流程如图:
)粗品。其流程如图:
①上述流程中,加入NaOH后,发生反应的化学方程式为
②亚硫酸钠粗品中含有少量
 ,设计实验证明亚硫酸钠粗品含有少量
,设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解, 。
。(4)已知有VL(已换算成标准状况)尾气,通入足量
 吸收再加足量
吸收再加足量 溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。 吸收
吸收 的化学方程式是
的化学方程式是 的含量(体积分数)的计算式是
的含量(体积分数)的计算式是
您最近一年使用:0次