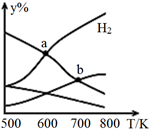
在某一恒温、容积可变的密闭容器中发生如下反应: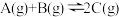
 。
。 时刻达到平衡后,在
时刻达到平衡后,在 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
时刻改变某一条件,其反应过程如图所示。下列说法正确的是
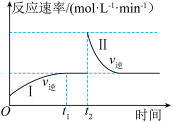
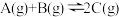
 。
。 时刻达到平衡后,在
时刻达到平衡后,在 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
时刻改变某一条件,其反应过程如图所示。下列说法正确的是
A.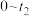 时, 时, |
B.Ⅰ、Ⅱ两过程达到平衡时, 的体积分数: 的体积分数: |
C. 时刻改变的条件可以是向密闭容器中加入 时刻改变的条件可以是向密闭容器中加入 |
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数: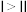 |
17-18高二上·天津静海·期末 查看更多[9]
山东师范大学附属中学2023-2024学年高二上学期10月月考化学试题福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题陕西省咸阳市泾阳县2021-2022学年高二上学期期中考试化学试题(已下线)专题2.2.4 化学平衡图像(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)选择性必修1 专题2 第三单元 课时1 影响化学平衡的因素高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时3 影响化学平衡的因素鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2节 化学反应的限度 课时2 反应条件对化学平衡的影响【全国百强校】河南省实验中学2018-2019学年高二上学期期中考试化学试题天津市静海县第一中学2017-2018学年高二上学期期末终结性检测化学试题
更新时间:2020-09-13 14:47:57
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在3个初始温度均为T℃的密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g) (正反应放热)。下列说法不正确的是
2SO3(g) (正反应放热)。下列说法不正确的是
 2SO3(g) (正反应放热)。下列说法不正确的是
2SO3(g) (正反应放热)。下列说法不正确的是容器编号 | 容器类型 | 初始体积 | 起始物质的量/mol | 平衡时SO3物质的量/mol | ||
SO2 | O2 | SO3 | ||||
I | 恒温恒容 | 1.0 L | 2 | 1 | 0 | 1.6 |
II | 绝热恒容 | 1.0 L | 2 | 1 | 0 | a |
III | 恒温恒压 | 0.5 L | 0 | 0 | 1 | b |
| A.a<1.6 |
| B.b<0.8 |
| C.平衡时v正(SO2):v(I)<v(II) |
| D.若起始时向容器I中充入1.0 molSO2(g)、0.20 mol O2(g)和4.0molSO3(g),则反应将向正反应方向进行 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5(g) PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度(mol·L−1) | 物质的平衡浓度(mol·L−1) | ||
| c(PCl5) | c(PCl3) | c(Cl2) | c(Cl2) | |
| Ⅰ | 0.4 | 0 | 0 | 0.2 |
| Ⅱ | 1.05 | 0.05 | 1.95 | |
| Ⅲ | 0.8 | 0 | 0 | |
A.达到平衡时,容器Ⅰ中 比容器Ⅱ的大 比容器Ⅱ的大 |
| B.达到平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为6︰31 |
C.达到平衡时,容器Ⅲ中的Cl2体积分数小于 |
| D.达到平衡时,容器Ⅲ中0.4 mol·L−1<c(PCl5)<0.8 mol·L−1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】以 CO2、H2为原料合成 CH3OH 涉及的反应如下:
反应Ⅰ: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-49kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49kJ·mol-1
反应Ⅱ: CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ·mol-1
CO(g)+H2O(g) ΔH2=+41kJ·mol-1
反应Ⅲ: CO(g)+2H2(g) CH3OH(g) ΔH3
CH3OH(g) ΔH3
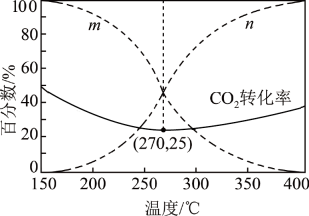
在 5MPa 下,按照 n(CO2):n(H2)=1:3 投料,平衡时,CO和CH3OH在含碳产物中物质的量分数及 CO2的转化率随温度的变化如图。下列说法正确的是
反应Ⅰ: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-49kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49kJ·mol-1反应Ⅱ: CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ·mol-1
CO(g)+H2O(g) ΔH2=+41kJ·mol-1反应Ⅲ: CO(g)+2H2(g)
 CH3OH(g) ΔH3
CH3OH(g) ΔH3在 5MPa 下,按照 n(CO2):n(H2)=1:3 投料,平衡时,CO和CH3OH在含碳产物中物质的量分数及 CO2的转化率随温度的变化如图。下列说法正确的是
| A.反应Ⅲ中反应物的总键能大于生成物的总键能 |
| B.曲线 n 代表 CH3OH 在含碳产物中物质的量分数 |
| C.该条件下温度越低,越有利于工业生产 CH3OH |
| D.图示 270℃时,平衡体系中CO2的体积分数为 20% |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
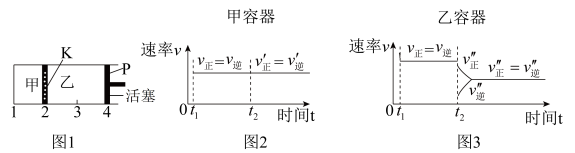
【推荐2】一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
| A.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均减小 |
| B.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| C.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| D.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
您最近半年使用:0次