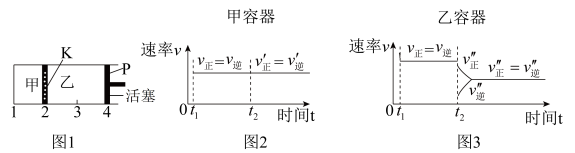
一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
| A.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均减小 |
| B.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| C.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| D.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
更新时间:2018-12-10 19:37:34
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
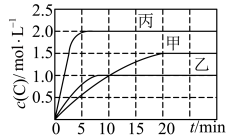
【推荐1】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g) + xB(g)  2C(g)。各容器的反应温度、反应物起始量、反应过程中C的浓度随时间变化关系分别以下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量、反应过程中C的浓度随时间变化关系分别以下表和下图表示:
下列说法正确的是
 2C(g)。各容器的反应温度、反应物起始量、反应过程中C的浓度随时间变化关系分别以下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量、反应过程中C的浓度随时间变化关系分别以下表和下图表示:容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物 | 1.5 mol A | 1.5 mol A | 6.0 mol A |

下列说法正确的是
| A.10min内甲容器中反应的平均速率v(A)=0.025mol·L-1·min-1 |
| B.由图可知:T1<T2,且该反应为吸热反应 |
| C.若平衡时保持温度不变,改变容器体积平衡不移动 |
| D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25% |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
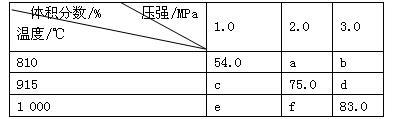
【推荐2】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
| A.a<54.0 |
| B.b> f |
| C.915 ℃,2.0 MPa时E的转化率为60% |
| D.K(1000 ℃)>K(810 ℃) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】温度为T时,向4.0 L恒容密闭容器中充入2.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
下列说法正确的是
 PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
下列说法正确的是
| A.反应在前50 s的平均速率为v(PCl3)=0.006 4 mol·L-1·s-1 |
| B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0 |
| C.相同温度下,起始时向容器中充入4.0 mol PCl3、4.0 mol Cl2,达到平衡时,则此反应的化学平衡常数为1/40 |
| D.相同温度下,起始时向容器中充入2.0 mol PCl5、0.40 mol PCl3和0.40 mol Cl2,达到平衡前v(正)<v(逆) |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1)
2NH3(g) ΔH=-92.4kJ·mol-1)
下列说法正确的是( )
 2NH3(g) ΔH=-92.4kJ·mol-1)
2NH3(g) ΔH=-92.4kJ·mol-1)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH4 |
| NH3浓度(mol·L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2c1>c3 | B.a+b=92.4 | C.2p1<p3 | D.α1+α3>1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
下列叙述错误 的是 ( )
 2NH3(g)
2NH3(g)  H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体 系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A.容器①、②中反应的平衡常数相等 |
| B.平衡时,两个容器中NH3的体积分数均为1/7 |
| C.容器②中达平衡时放出的热量Q=23.15 kJ |
| D.若将容器①体积拉至0.5 L,上述反应的反应热ΔH一定不改变 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】将2 mol A和1 mol B充入某密闭容器中发生反应:2A(g)+B(g)⇌xC(g),当达到化学平衡后,A的体积分数为a%。下列判断不正确的是
| A.若在恒温恒压下,当x=1时,将1.5 mol A、l mol C作起始物质,平衡后,A的体积分数大于a% |
| B.若在恒温恒压下,当x=2时,将2 mol A、2 mol B作起始物质,平衡后,A的体积分数小于a% |
| C.若在恒温恒容下,按0.2 mol A、0.1 mol B、1.8 mol C作起始物质,平衡后,A的体积分数仍为a%,则x为2或3 |
| D.若在恒温恒压下,当x=3时,将l mol A、1 mol B、6 mol C作起始物质,平衡后,A的体积分数大于a% |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。对于反应2SiHCl3(g) ⇌SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。下列说法不正确的是
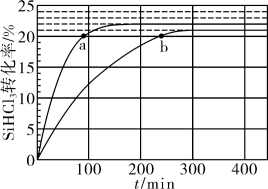

| A.343K时反应的平衡转化率为22% |
| B.a处反应速率大于b处 |
| C.在343K下,要缩短反应达到平衡的时间,可采取的措施有及时移去产物、改进催化剂 |
D.已知反应速率v=v正-v逆=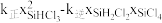 ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,则a处 ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,则a处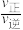 =1.3(保留1位小数) =1.3(保留1位小数) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定条件下存在反应
 ,向甲、乙、丙三个恒容容器中加入一定量的C和
,向甲、乙、丙三个恒容容器中加入一定量的C和 ,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是


 ,向甲、乙、丙三个恒容容器中加入一定量的C和
,向甲、乙、丙三个恒容容器中加入一定量的C和 ,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 |  ℃ ℃ |  ℃ ℃ |  ℃ ℃ |
| 起始量 | 2mol C、1molH2O | 1mol CO、1molH2 | 4mol C、2molH2O |

A.丙容器的体积 |
B.甲容器中,反应在前15min的平均速率 |
C.当温度为 ℃时,反应的平衡常数 ℃时,反应的平衡常数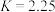 |
D.乙容器中,若平衡时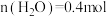 ,则 ,则 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
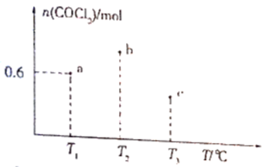
【推荐3】在体积均为2L的a、b、e三个恒容密闭容器中分别充入1molCO(g)和1molCl2(g),发生反应CO(g)+Cl2(g) COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
 COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
COCl2(g),若三个容器的反应温度分别为T1℃、T2℃、T3℃且保持恒定不变,测得反应均进行到2min时,COCl2(g)的物质的量如图所示。下列说法正确的是
| A.a容器中,0~2min时平均反应速率v(COCl2)=0.3mol.·L-1·min-1 |
| B.反应进行到2min时,三个容器中一定达到化学平衡状态的是b容器 |
| C.当三个容器内的反应都达到化学平衡时,Cl2转化率最大的是a容器 |
| D.若开始时向b容器中充入CO(g)、Cl2(g)、COCl2(g)各0.5mol,则开始时v正<v逆 |
您最近半年使用:0次



