三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。对于反应2SiHCl3(g) ⇌SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。下列说法不正确的是
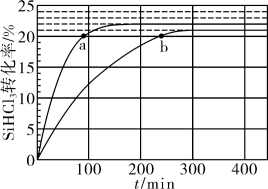

| A.343K时反应的平衡转化率为22% |
| B.a处反应速率大于b处 |
| C.在343K下,要缩短反应达到平衡的时间,可采取的措施有及时移去产物、改进催化剂 |
D.已知反应速率v=v正-v逆=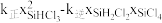 ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,则a处 ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,则a处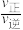 =1.3(保留1位小数) =1.3(保留1位小数) |
更新时间:2021-11-08 21:24:54
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】向体积均为IL的两恒容容器中分别充入3 X和2
X和2 Y发生反应:
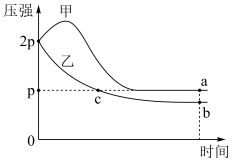
Y发生反应: ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
 X和2
X和2 Y发生反应:
Y发生反应: ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
| A.升高温度可以促进该反应正向进行 | B.反应速率: |
C.混合气体的平均相对分子质量 | D.a点平衡常数: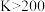 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的2.3倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的2.3倍,下列叙述正确的是
 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的2.3倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的2.3倍,下列叙述正确的是| A.A的转化率变小 | B.平衡向逆反应方向移动 |
| C.a>c+d | D.D的体积分数变小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
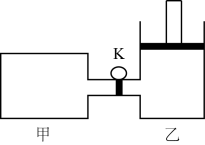
【推荐3】如图所示,初始体积均为1 L的两容器,甲保持恒容,乙保持恒压。起始时关闭活塞K,向甲中充入1 mol PCl5(g),乙中充入1 mol PCl3(g)和1 mol Cl2(g)。恒温下,均发生反应:PCl5(g) PCl3(g)+Cl2(g)。达平衡时,乙的容积为0.8 L。下列说法不正确的是
PCl3(g)+Cl2(g)。达平衡时,乙的容积为0.8 L。下列说法不正确的是
 PCl3(g)+Cl2(g)。达平衡时,乙的容积为0.8 L。下列说法不正确的是
PCl3(g)+Cl2(g)。达平衡时,乙的容积为0.8 L。下列说法不正确的是
| A.平衡时PCl5(g)的体积分数:甲<乙 |
| B.从甲中移走0.5 mol PCl3(g),0.5 mol Cl2(g),再次平衡时0.2 mol<n(PCl5)<0.4 mol |
| C.甲中PCl5(g)的转化率大于60% |
| D.打开K一段时间,再次平衡时乙容器的体积为0.6 L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在某一恒容密闭容器中充入X(g)和Y(g),发生反应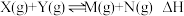 ,所得实验数据如表所示:
,所得实验数据如表所示:
下列说法错误的是
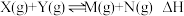 ,所得实验数据如表所示:
,所得实验数据如表所示:| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.4 | 0.1 | 0.09 |
| ② | 800 | 0.1 | 0.4 | 0.08 |
| ③ | 800 | 0.2 | 0.3 | a |
| ④ | 900 | 0.1 | 0.15 | b |
| A.该反应的反应物的总能量大于生成物的总能量 |
B.实验①中,若某时刻测得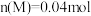 ,则此时混合气体中Y的物质的量分数为12% ,则此时混合气体中Y的物质的量分数为12% |
C.实验①和③中,反应均达到平衡时,平衡常数之比为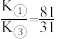 |
| D.实验④中,反应达到平衡时,Y的转化率为40% |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】 制
制 的平衡体系中存在如下反应:
的平衡体系中存在如下反应:
反应Ⅰ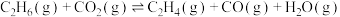

反应Ⅱ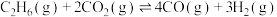

将2 mol 和3 mol
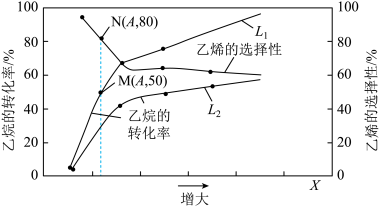
和3 mol  投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性(
投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性( 条件下)与温度、压强的关系如图所示。已知:乙烯的选择性
条件下)与温度、压强的关系如图所示。已知:乙烯的选择性 。下列说法错误的是
。下列说法错误的是
 制
制 的平衡体系中存在如下反应:
的平衡体系中存在如下反应:反应Ⅰ
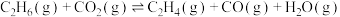

反应Ⅱ
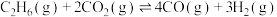

将2 mol
 和3 mol
和3 mol  投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性(
投入容积为1 L的恒容密闭容器中发生反应,测得平衡时乙烷的转化率、乙烯的选择性( 条件下)与温度、压强的关系如图所示。已知:乙烯的选择性
条件下)与温度、压强的关系如图所示。已知:乙烯的选择性 。下列说法错误的是
。下列说法错误的是
| A.X代表温度,L代表压强 |
B.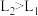 |
C.N点时, 转化成的CO的物质的量为0.4 mol 转化成的CO的物质的量为0.4 mol |
| D.M点时,反应Ⅰ的平衡常数为0.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在两个固定体积均为 密闭容器中以不同的氢碳比
密闭容器中以不同的氢碳比 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: ,
, 的平衡转化率
的平衡转化率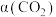 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
 密闭容器中以不同的氢碳比
密闭容器中以不同的氢碳比 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: ,
, 的平衡转化率
的平衡转化率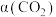 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是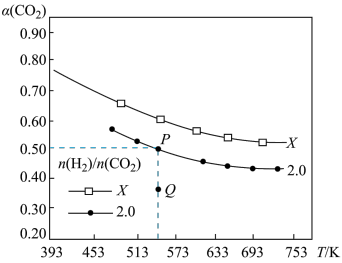
| A.该反应在常温下不可能自发进行 |
B.X的氢碳比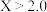 ,在氢碳比为2.0时Q点 ,在氢碳比为2.0时Q点 点 点 |
C.向处于P点状态的容器中,按2∶4∶1∶4的比例再充入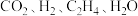 ,再次平衡后 ,再次平衡后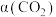 减小 减小 |
D.若起始时 、 、 浓度分别为 浓度分别为 、 、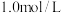 ,则可得P点对应温度的平衡常数的值为512 ,则可得P点对应温度的平衡常数的值为512 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应: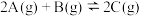 ,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
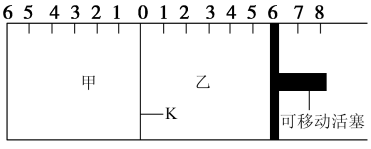
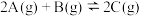 ,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
,反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
| A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡 |
| B.达到平衡后,隔板K最终停留在左侧刻度0-2之间 |
| C.若一开始就将K和可移动活塞都固定,其他条件均不变,达到平衡时测得甲中A的转化率为a,则乙中C的转化率也为a |
| D.若平衡时K停留在左侧1刻度处,则活塞停留在6刻度右侧 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列图示与对应的叙述相符的是
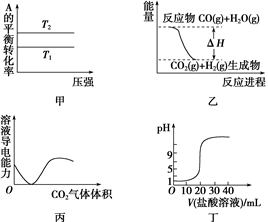
A.由图甲可以判断:对于反应A(g)+B(g)  2C(g),若T1>T2,则ΔH<0 2C(g),若T1>T2,则ΔH<0 |
B.图乙表示可逆反应CO(g)+H2O(g)  CO2(g)+H2(g) ΔH>0 CO2(g)+H2(g) ΔH>0 |
| C.图丙表示CO2通入饱和Na2CO3溶液中,溶液导电性变化 |
| D.图丁表示0.1 mol·L-1的盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液pH随加入盐酸体积的变化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在某合成塔中主要发生的反应为:
反应Ⅰ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) △H1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2
调节 =4,充入合成塔,当气体总压强为aMPa,平衡时各物质的物质的量分数如图1所示;不同压强时,CO2的平衡转化率如图2所示:
=4,充入合成塔,当气体总压强为aMPa,平衡时各物质的物质的量分数如图1所示;不同压强时,CO2的平衡转化率如图2所示:
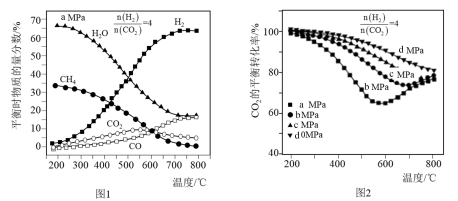
反应Ⅰ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) △H1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2
调节
 =4,充入合成塔,当气体总压强为aMPa,平衡时各物质的物质的量分数如图1所示;不同压强时,CO2的平衡转化率如图2所示:
=4,充入合成塔,当气体总压强为aMPa,平衡时各物质的物质的量分数如图1所示;不同压强时,CO2的平衡转化率如图2所示:
A.反应Ⅰ的平衡常数可以表示为K= |
| B.图中压强a、b、c、d的大小关系为d>c>b>a |
| C.高温、高压的条件对提升甲烷的产率有利 |
| D.反应CO2(g)+CH4(g)⇌2CO(g)+2H2(g)的△H=△H1-2△H2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】有关下列图象的分析正确的是

A.图①可表示反N2(g)+3H2(g)  2NH3(g)在达到平衡后,减少NH3的浓度,正逆反应速率的变化趋势 2NH3(g)在达到平衡后,减少NH3的浓度,正逆反应速率的变化趋势 |
| B.图②表示FeCl3溶液和KSCN溶液反应达平衡后,向该混合液中逐渐加入固体KCl的过程中C(Fe3+)的变化趋势(忽略溶液体积变化) |
| C.图③表示等体积等pH的弱酸HA和强酸HB加水稀释过程中的pH变化趋势 |
D.图④表示密闭容器中CH3OCH3(g)+3H2O(g)  6H2(g)+2CO2(g) △H>0达到平衡后,恒压升高温度过程中,CH3OCH3的转化率变化趋势 6H2(g)+2CO2(g) △H>0达到平衡后,恒压升高温度过程中,CH3OCH3的转化率变化趋势 |
您最近一年使用:0次


 ,以
,以 、
、 表示速率常数,反应速率可表示为
表示速率常数,反应速率可表示为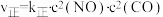 ,
, 。T℃下,向恒容容器中充入2molNO和2molCO,反应过程中
。T℃下,向恒容容器中充入2molNO和2molCO,反应过程中 和CO的物质的量变化如图所示,下列说法不正确的是
和CO的物质的量变化如图所示,下列说法不正确的是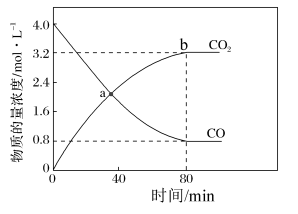
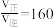



 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知:
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知: ,假设A的相对分子质量为267)。下列说法正确的是
,假设A的相对分子质量为267)。下列说法正确的是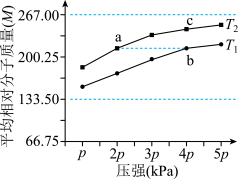

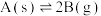 ,平衡后恒温压缩容器体积,
,平衡后恒温压缩容器体积, 的浓度不变
的浓度不变

