已知恒容密闭容器中发生反应:
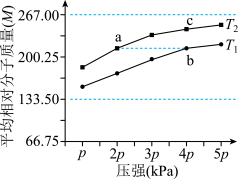
 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知:
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知: ,假设A的相对分子质量为267)。下列说法正确的是
,假设A的相对分子质量为267)。下列说法正确的是

 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知:
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知: ,假设A的相对分子质量为267)。下列说法正确的是
,假设A的相对分子质量为267)。下列说法正确的是
A. |
B.反应平衡常数: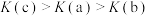 |
| C.当气体平均相对分子质量为200.25时,A的转化率约为50%(反应起始时B的浓度为0) |
D.若容器内发生反应: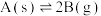 ,平衡后恒温压缩容器体积, ,平衡后恒温压缩容器体积, 的浓度不变 的浓度不变 |
更新时间:2023-12-25 15:10:08
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列事实不能用勒夏特列原理解释的是
①溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
②工业合成氨反应N2(g) +3H2(g) 2NH3(g) △H<0,为提高氨的产率,实际生产中采取高温、高压的措施
2NH3(g) △H<0,为提高氨的产率,实际生产中采取高温、高压的措施
③反应2 NO2(g) N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅
N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅
④对于2HI(g) H2(g) +I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g) +I2(g),达平衡后,缩小容器体积可使体系颜色变深
①溴水中有下列平衡Br2+H2O
 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅②工业合成氨反应N2(g) +3H2(g)
 2NH3(g) △H<0,为提高氨的产率,实际生产中采取高温、高压的措施
2NH3(g) △H<0,为提高氨的产率,实际生产中采取高温、高压的措施③反应2 NO2(g)
 N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅
N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅④对于2HI(g)
 H2(g) +I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g) +I2(g),达平衡后,缩小容器体积可使体系颜色变深| A.①② | B.②③ | C.③④ | D.②④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】使用合适的催化剂进行乙酸直接加氢可制备乙醇,反应原理如下:
主反应:

副反应:
 (热效应小可忽略)
(热效应小可忽略)
在密闭容器中控制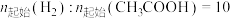 。
。 下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为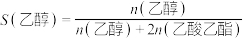 。下列说法正确的是
。下列说法正确的是
主反应:


副反应:

 (热效应小可忽略)
(热效应小可忽略)在密闭容器中控制
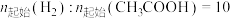 。
。 下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为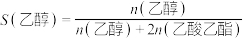 。下列说法正确的是
。下列说法正确的是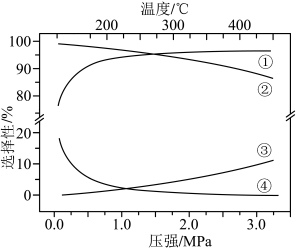
A.反应  |
| B.曲线②变化的原因是随温度升高,副反应正向进行的程度减小 |
| C.图中曲线③表示250℃,乙醇选择性随压强变化的曲线 |
D.300℃、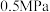 下,反应足够长时间,S(乙醇) 下,反应足够长时间,S(乙醇)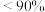 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】105℃时,将一定量的某碳酸氢盐(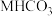 )固体置于真空恒容容器中,存在如下反应:
)固体置于真空恒容容器中,存在如下反应: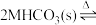
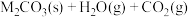 。已知该条件下,反应达平衡时体系的总压强为46 kPa,保持温度不变,下列说法正确的是
。已知该条件下,反应达平衡时体系的总压强为46 kPa,保持温度不变,下列说法正确的是
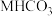 )固体置于真空恒容容器中,存在如下反应:
)固体置于真空恒容容器中,存在如下反应: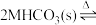
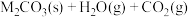 。已知该条件下,反应达平衡时体系的总压强为46 kPa,保持温度不变,下列说法正确的是
。已知该条件下,反应达平衡时体系的总压强为46 kPa,保持温度不变,下列说法正确的是| A.混合气体中各组分的体积分数不变,说明反应达到平衡状态 |
B.混合气体的平均摩尔质量为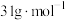 |
C.再添加一定量的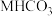 固体,体系的压强一定不变 固体,体系的压强一定不变 |
| D.若原容器中有残留空气,达平衡时,体系的总压仍为46 kPa |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度下,两种碳酸氢盐在2个体积相同的容器中各自达到平衡时,总压强分别为p1和p2。
反应1:NH4HCO3(s) NH3(g)+H2O(g)+CO2(g) p1=3.6×104Pa
NH3(g)+H2O(g)+CO2(g) p1=3.6×104Pa
反应2:2NaHCO3(s) Na2CO3(s)+H2O(g)+CO2(g) p2=4×103Pa
Na2CO3(s)+H2O(g)+CO2(g) p2=4×103Pa
该温度下,向某刚性密闭容器中放入一定量NH4HCO3和Na2CO3固体,平衡后以上3种固体均大量存在。下列说法错误的是
反应1:NH4HCO3(s)
 NH3(g)+H2O(g)+CO2(g) p1=3.6×104Pa
NH3(g)+H2O(g)+CO2(g) p1=3.6×104Pa反应2:2NaHCO3(s)
 Na2CO3(s)+H2O(g)+CO2(g) p2=4×103Pa
Na2CO3(s)+H2O(g)+CO2(g) p2=4×103Pa该温度下,向某刚性密闭容器中放入一定量NH4HCO3和Na2CO3固体,平衡后以上3种固体均大量存在。下列说法错误的是
| A.反应2的平衡常数为4×106Pa2 |
| B.平衡后总压强为4.36×105Pa |
| C.通入NH3,再次平衡后,总压强增大 |
| D.缩小体积,再次平衡后,H2O的体积分数不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】下列说法不正确的是
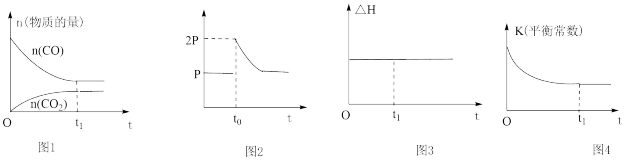

A.图1可表示将一定量的CO和NO通入刚性容器发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),物质的量随时间的变化关系,且t1时候达到平衡 2CO2(g)+N2(g),物质的量随时间的变化关系,且t1时候达到平衡 |
| B.图2可表示反应CaCO3(s)=CaO(s)+CO2(g),在t0时刻将容器的体积缩小为原来的一半后再次平衡的过程中压强随时间的变化关系 |
| C.图3可表示反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH与时间的变化关系,且t1时候不一定达到平衡 |
D.图4可表示在绝热容器中充入一定量的A和B,发生反应mA(g)+nB(g) pC(g)+qD(g) ΔH<0,平衡常数与时间的关系图,且t1时候达到平衡 pC(g)+qD(g) ΔH<0,平衡常数与时间的关系图,且t1时候达到平衡 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知:CO(g)+H2O(g) CO2(g)+H2(g) △H= -41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) △H= -41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
下列说法中,不正确的是
 CO2(g)+H2(g) △H= -41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) △H= -41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
| CO | H2O | CO2 | H2 | ||
| ① | 1 | 4 | 0 | 0 | 放出热量: 32.8 kJ |
| ② | 0 | 0 | 1 | 4 | 热量变化:Q |
| A.容器①中反应达平衡时,CO 的转化率为80% |
| B.容器①中的平衡常数等于容器②中平衡常数 |
| C.Q=32.8 |
| D.容器①中CO 反应速率等于H2O的反应速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25°C时,用NaOH溶液分别滴定HX、CuSO4、MgSO4三种溶液,pM[p表示负对数,M表示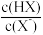 、c(Cu2+)、c(Mg2+ )等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]< Ksp[Mg(OH)2],下列说法不正确的是
、c(Cu2+)、c(Mg2+ )等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]< Ksp[Mg(OH)2],下列说法不正确的是
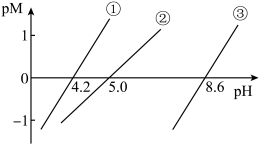
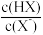 、c(Cu2+)、c(Mg2+ )等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]< Ksp[Mg(OH)2],下列说法不正确的是
、c(Cu2+)、c(Mg2+ )等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]< Ksp[Mg(OH)2],下列说法不正确的是
| A.HX的电离平衡常数Ka=10-5 |
| B.滴定HX当pH=7时,c(X- )>c(HX) |
| C.③代表滴定CuSO4溶液的变化关系 |
| D.Mg(OH)2易溶于HX溶液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】在二氧化碳加氢制甲醇的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)∆H1=-49.5kJ·mol-1
反应Ⅱ:CO(g)+2H2(g)=CH3OH(g)∆H2
反应Ⅲ:CO2(g)+H2(g)=CO(g)+H2O(g)∆H3=40.9kJ·mol-1
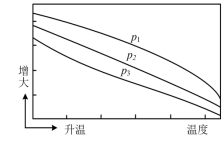
在体积为1L的恒容密闭容器中通入1molCO2和3molH2,发生上述反应,CO2的平衡转化率随温度和压强的变化如图所示。下列说法正确的是
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)∆H1=-49.5kJ·mol-1
反应Ⅱ:CO(g)+2H2(g)=CH3OH(g)∆H2
反应Ⅲ:CO2(g)+H2(g)=CO(g)+H2O(g)∆H3=40.9kJ·mol-1
在体积为1L的恒容密闭容器中通入1molCO2和3molH2,发生上述反应,CO2的平衡转化率随温度和压强的变化如图所示。下列说法正确的是

| A.∆H2=90.4kJ·mol-1 |
| B.在某温度下,平衡时容器中CH3OH(g)为0.3mol,CO(g)为0.3mol,则反应Ⅲ的平衡常数为0.25 |
| C.压强p1、p2、p3由小到大的顺序为p1<p2<p3 |
| D.高温、高压一定有利于提高CO2的平衡转化率 |
您最近一年使用:0次
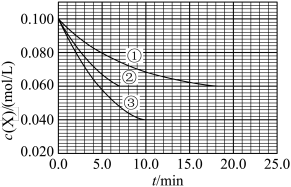
【推荐1】在1L的密闭容器中充入2molN2和7molH2,发生反应N2+3H2 2NH3,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列说法正确的是
2NH3,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列说法正确的是

 2NH3,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列说法正确的是
2NH3,保持其他条件不变,相同时间内测得NH3的浓度与温度的关系如图所示。下列说法正确的是
| A.图中a、b、c三点只有b点表示平衡状态 |
| B.a、c两点对应的反应速率:va=vc |
| C.温度为T1K时,N2的平衡转化率为50% |
| D.温度为T1K时,再加入1molN2和1molNH3,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在盛有足量A的体积可变的密闭容器中,保持压强一定,加入B,发生反应:A(s)+2B(g) 4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
 4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是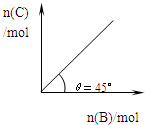
| A.当温度升高后,则图中θ>45° |
| B.平衡时B的转化率为50% |
| C.若保持温度压强不变,再加入B,则平衡后正、逆反应速率均逐渐增大 |
| D.若保持温度压强不变,再加入B,则平衡后反应体系气体密度减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】尿素在生产生活中应用非常广泛,2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(l)是工业上合成氮肥尿素的主要方法,在生产条件下,单位时间内获得尿素的产量与压强及n(NH3):n(CO2)的关 系如图甲所示。当氨碳比n(NH3):n(CO2)=4 时,CO2的转化率随时间的变化关系如图乙所示。下列说法不正确的是
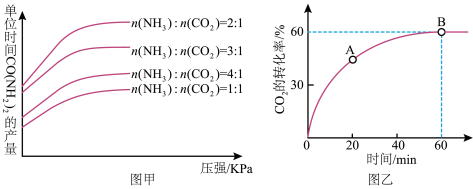

| A.生产过程中n(NH3):n(CO2)的 最佳配比为2:1 |
| B.若开始投料按照n(NH3):n(CO2)为2:1投料,平衡后若压缩容器的体积,则再次平衡时c(NH3)比压缩前小 |
| C.A点的逆反应速率小于B点的正反应速率 |
| D.由图乙可知NH3的平衡转化率为30% |
您最近一年使用:0次