相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
下列叙述错误 的是 ( )
 2NH3(g)
2NH3(g)  H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体 系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A.容器①、②中反应的平衡常数相等 |
| B.平衡时,两个容器中NH3的体积分数均为1/7 |
| C.容器②中达平衡时放出的热量Q=23.15 kJ |
| D.若将容器①体积拉至0.5 L,上述反应的反应热ΔH一定不改变 |
更新时间:2019-06-11 16:44:51
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知: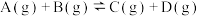
 ,在一体积为2L的恒容密闭容器中,充入1mol A和1molB开始反应,测得平衡常数随温度的变化如下表。下列说法错误的是
,在一体积为2L的恒容密闭容器中,充入1mol A和1molB开始反应,测得平衡常数随温度的变化如下表。下列说法错误的是
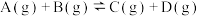
 ,在一体积为2L的恒容密闭容器中,充入1mol A和1molB开始反应,测得平衡常数随温度的变化如下表。下列说法错误的是
,在一体积为2L的恒容密闭容器中,充入1mol A和1molB开始反应,测得平衡常数随温度的变化如下表。下列说法错误的是| T/℃ | 700 | 800 | 850 | 1000 |
| K | 0.49 | 0.64 | 1.00 | 1.21 |
| A.该反应为吸热反应 |
| B.800℃下,A的平衡转化率约为44.4% |
| C.850℃下,向平衡体系中再加入1mol A和1mol C,反应向逆反应方向进行 |
| D.1000℃下,向平衡体系中再加入1mol A和1mol B,达到平衡后,各物质的百分含量不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】甲、乙均为1 L的恒容密闭容器,向甲中充入1 mol CH4和1 mol CO2,乙中充入1 mol CH4和n mol CO2,在催化剂存在下发生反应:CH4(g)+CO2(g)⇌2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
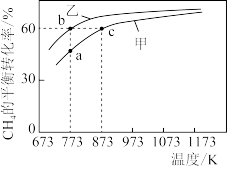

| A.该反应的正反应是放热反应 |
| B.773K时,该反应的平衡常数小于12.96 |
| C.H2的体积分数:φ(b)=φ(c) |
| D.873K时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2 mol,平衡不发生移动 |
您最近一年使用:0次
【推荐1】 与
与 可结合生成多种络合物,在水溶液中存在如下平衡:
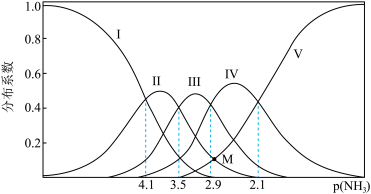
可结合生成多种络合物,在水溶液中存在如下平衡: ,向某浓度的硫酸铜溶液中通入氨气,实验测得含Cu微粒的物质的量分布系数与溶液中
,向某浓度的硫酸铜溶液中通入氨气,实验测得含Cu微粒的物质的量分布系数与溶液中 关系如图。下列说法正确的是
关系如图。下列说法正确的是
 与
与 可结合生成多种络合物,在水溶液中存在如下平衡:
可结合生成多种络合物,在水溶液中存在如下平衡: ,向某浓度的硫酸铜溶液中通入氨气,实验测得含Cu微粒的物质的量分布系数与溶液中
,向某浓度的硫酸铜溶液中通入氨气,实验测得含Cu微粒的物质的量分布系数与溶液中 关系如图。下列说法正确的是
关系如图。下列说法正确的是
A.曲线Ⅱ表示 分布系数的变化情况 分布系数的变化情况 |
B.当 时, 时,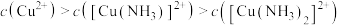 |
C.反应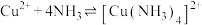 的平衡常数 的平衡常数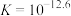 |
D.M点时 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】实验室测定反应 的平衡常数K的过程为:
的平衡常数K的过程为:
①一定温度下,将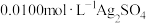 溶液与
溶液与 溶液
溶液 等体积混合,产生灰黑色沉淀;
等体积混合,产生灰黑色沉淀;
②待步骤①中反应达到平衡时,取v mL上层清液,用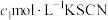 标准溶液滴定
标准溶液滴定 ,至出现稳定的浅红色时消耗KSCN标准溶液
,至出现稳定的浅红色时消耗KSCN标准溶液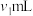 。
。
资料: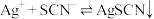 (白色)
(白色) 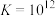 ,
,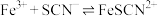 (红色)
(红色) 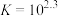
下列说法正确的是
 的平衡常数K的过程为:
的平衡常数K的过程为:①一定温度下,将
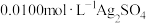 溶液与
溶液与 溶液
溶液 等体积混合,产生灰黑色沉淀;
等体积混合,产生灰黑色沉淀;②待步骤①中反应达到平衡时,取v mL上层清液,用
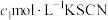 标准溶液滴定
标准溶液滴定 ,至出现稳定的浅红色时消耗KSCN标准溶液
,至出现稳定的浅红色时消耗KSCN标准溶液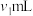 。
。资料:
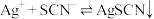 (白色)
(白色) 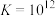 ,
,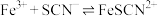 (红色)
(红色) 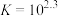
下列说法正确的是
A. 溶液可替换为 溶液可替换为 溶液 溶液 |
| B.过程①中产生的灰黑色沉淀为Fe或Ag元素的氧化物 |
C.可用KCl标准溶液代替KSCN的标准溶液滴定 |
D.步骤②中不待溶液澄清,直接用浊液做滴定实验测定 ,则所测K值偏小 ,则所测K值偏小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】用压强传感器可测得2NO2(g)⇌N2O4(g)反应平衡移动过程中的压强变化。在室温、100kPa条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是
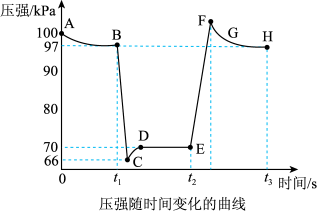

| A.B点处NO2的转化率为3% |
| B.B点到D点的过程中,NO2的物质的量浓度先减小后增大 |
| C.t2时刻迅速移动活塞到达的位置比初始位置刻度小 |
| D.E、H两点气体的平均相对分子质量大小为ME>MH |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知:无CO时反应 、有CO时反应
、有CO时反应 。在容积为
。在容积为 的容器中,相同时间下测得
的容器中,相同时间下测得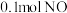 转化为
转化为 的转化率随温度变化如图所示。下列说法不正确的是
的转化率随温度变化如图所示。下列说法不正确的是
 、有CO时反应
、有CO时反应 。在容积为
。在容积为 的容器中,相同时间下测得
的容器中,相同时间下测得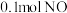 转化为
转化为 的转化率随温度变化如图所示。下列说法不正确的是
的转化率随温度变化如图所示。下列说法不正确的是
A.反应 的 的 |
| B.有CO时,该反应在低温条件下自发进行 |
C.Y点再通入CO、 各 各 ,此时v(CO,正)<v(CO,逆) ,此时v(CO,正)<v(CO,逆) |
D.达平衡后,其他条件不变改变物料使 ,CO转化率下降 ,CO转化率下降 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】温度为 时,在三个容积均为1L的恒容密闭容器中仅发生反应:
时,在三个容积均为1L的恒容密闭容器中仅发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: ,
, ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是
 时,在三个容积均为1L的恒容密闭容器中仅发生反应:
时,在三个容积均为1L的恒容密闭容器中仅发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: ,
, ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是| 容器编号 | 物质的起始浓度(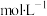 ) ) | 物质的平衡浓度(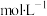 ) ) | ||
 |  |  |  | |
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.3 | 0.5 | 0.2 | |
| III | 0 | 0.6 | 0.3 | |
| A.达平衡时,容器I反应前、后的总压强之比为4∶5 |
B.达平衡时,容器II中 比容器I中的大 比容器I中的大 |
C.达平衡时,容器III中 的体积分数小于50% 的体积分数小于50% |
D.当温度改变为 时,若 时,若 ,则 ,则 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g) 2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
 2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是| 容器 | 起始各物质的物质的量/mol | 达到平衡时体 系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A.Q1=Q2=Q3 |
| B.达到平衡时,丙容器中SO2的体积分数最大 |
| C.甲、乙、丙3个容器中反应的平衡常数不相等 |
| D.若在上述条件下反应生成2molSO3(s)的放热大于197kJ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知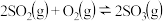 ;
; 向同温、同体积的三个密闭容器中分别充入气体:
向同温、同体积的三个密闭容器中分别充入气体: 甲
甲 和
和 ;
; 乙
乙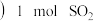 和
和 ;
; 丙
丙 和
和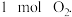 恒温、恒容下反应达平衡时,下列关系一定正确的是
恒温、恒容下反应达平衡时,下列关系一定正确的是
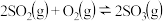 ;
; 向同温、同体积的三个密闭容器中分别充入气体:
向同温、同体积的三个密闭容器中分别充入气体: 甲
甲 和
和 ;
; 乙
乙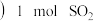 和
和 ;
; 丙
丙 和
和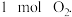 恒温、恒容下反应达平衡时,下列关系一定正确的是
恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P: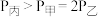 |
B.气体的总物质的量n: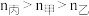 |
C. 的体积分数 的体积分数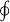 : :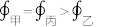 |
D.反应热量的数值Q: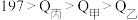 |
您最近一年使用:0次
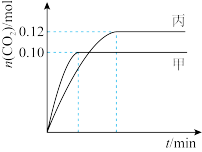
【推荐2】汽车尾气净化的主要原理为 ,一定温度下,在三个容积均为2.0L的恒容密闭容器中反应,起始物质的量与反应温度如表所示,反应过程中甲、丙容器中
,一定温度下,在三个容积均为2.0L的恒容密闭容器中反应,起始物质的量与反应温度如表所示,反应过程中甲、丙容器中 的物质的量随时间变化关系如图所示。下列说法正确的是
的物质的量随时间变化关系如图所示。下列说法正确的是
 ,一定温度下,在三个容积均为2.0L的恒容密闭容器中反应,起始物质的量与反应温度如表所示,反应过程中甲、丙容器中
,一定温度下,在三个容积均为2.0L的恒容密闭容器中反应,起始物质的量与反应温度如表所示,反应过程中甲、丙容器中 的物质的量随时间变化关系如图所示。下列说法正确的是
的物质的量随时间变化关系如图所示。下列说法正确的是
| 容器 | 温度/ | 起始物质的量/ | |
 |  | ||
| 甲 |  | 0.20 | 0.20 |
| 乙 |  | 0.30 | 0.30 |
| 丙 |  | 0.20 | 0.20 |
| A.该反应的正反应为吸热反应 |
B.达到平衡时,乙中 的体积分数比甲中的大 的体积分数比甲中的大 |
C. 时,若起始时向甲中充入 时,若起始时向甲中充入 和 和 ,则反应达到新平衡前 ,则反应达到新平衡前 |
D. 时,若起始时向丙中充入 时,若起始时向丙中充入 和 和 ,则达平衡时 ,则达平衡时 的转化率为 的转化率为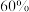 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】恒容密闭容器中充入3mol CH4和6mol H2S,发生反应:CH4(g)+2H2S(g) CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如下图所示:
CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如下图所示:

下列说法错误的是
 CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如下图所示:
CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如下图所示:
下列说法错误的是
| A.当满足2v逆(H2S)=v正(H2)时,反应达到平衡状态 |
| B.采用高温、低压条件,有利于提高CH4的平衡转化率 |
| C.图中M点时,保持温度不变,再向容器中充入3molCH4和6moH2S,达到新平衡时,CH4的物质的量分数小于H2的 |
D.图中N点对应温度下,以物质的量分数表示的化学平衡常数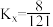 |
您最近一年使用:0次

 2Z(g)+W(g);
2Z(g)+W(g);


