温度为 时,在三个容积均为1L的恒容密闭容器中仅发生反应:
时,在三个容积均为1L的恒容密闭容器中仅发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: ,
, ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是
 时,在三个容积均为1L的恒容密闭容器中仅发生反应:
时,在三个容积均为1L的恒容密闭容器中仅发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: ,
, ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是| 容器编号 | 物质的起始浓度(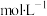 ) ) | 物质的平衡浓度(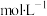 ) ) | ||
 |  |  |  | |
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.3 | 0.5 | 0.2 | |
| III | 0 | 0.6 | 0.3 | |
| A.达平衡时,容器I反应前、后的总压强之比为4∶5 |
B.达平衡时,容器II中 比容器I中的大 比容器I中的大 |
C.达平衡时,容器III中 的体积分数小于50% 的体积分数小于50% |
D.当温度改变为 时,若 时,若 ,则 ,则 |
更新时间:2022-10-11 20:59:05
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列说法不正确的是
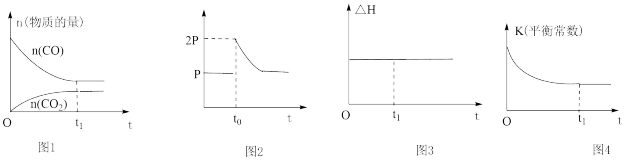

A.图1可表示将一定量的CO和NO通入刚性容器发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),物质的量随时间的变化关系,且t1时候达到平衡 2CO2(g)+N2(g),物质的量随时间的变化关系,且t1时候达到平衡 |
| B.图2可表示反应CaCO3(s)=CaO(s)+CO2(g),在t0时刻将容器的体积缩小为原来的一半后再次平衡的过程中压强随时间的变化关系 |
| C.图3可表示反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH与时间的变化关系,且t1时候不一定达到平衡 |
D.图4可表示在绝热容器中充入一定量的A和B,发生反应mA(g)+nB(g) pC(g)+qD(g) ΔH<0,平衡常数与时间的关系图,且t1时候达到平衡 pC(g)+qD(g) ΔH<0,平衡常数与时间的关系图,且t1时候达到平衡 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】一定条件下,分别向体积为2L的密闭容器中充入气体,发生反应:2A(g)+B(g)  C(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
C(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
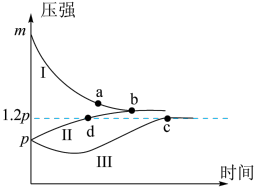
实验①:恒温恒容条件下充入4molA、2molB
实验②:恒温恒容条件下充入2molC
实验③:绝热恒容条件下充入2molC
 C(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
C(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
实验①:恒温恒容条件下充入4molA、2molB
实验②:恒温恒容条件下充入2molC
实验③:绝热恒容条件下充入2molC
| A.曲线Ⅰ对应实验③ |
| B.正反应为吸热反应 |
| C.b点平衡常数比c点平衡常数大 |
| D.气体的总物质的量:nc>nd |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】某小组欲制备配离子 ,实验如下。
,实验如下。
已知: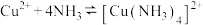
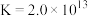
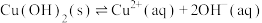
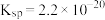
下列说法不正确的是
 ,实验如下。
,实验如下。| 序号 | 步骤 |
| Ⅰ | 向2mL 溶液中滴加0.5mL 溶液中滴加0.5mL 氨水,产生蓝色沉淀;继续滴加约1.5mL氨水,沉淀完全溶解,得到深蓝色溶液 氨水,产生蓝色沉淀;继续滴加约1.5mL氨水,沉淀完全溶解,得到深蓝色溶液 |
| Ⅱ | 分别向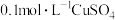 溶液和实验Ⅰ所得深蓝色溶液中加入光亮的铁钉;1min后,前者铁钉表面有红色物质析出,后者铁钉无现象 溶液和实验Ⅰ所得深蓝色溶液中加入光亮的铁钉;1min后,前者铁钉表面有红色物质析出,后者铁钉无现象 |
| Ⅲ | 取0.1g氢氧化铜固体于试管中,加入5mL 氨水,溶液略变为蓝色,固体未见明显溶解;滴加2滴饱和氯化铵溶液,固体完全溶解,得到深蓝色溶液 氨水,溶液略变为蓝色,固体未见明显溶解;滴加2滴饱和氯化铵溶液,固体完全溶解,得到深蓝色溶液 |
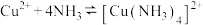
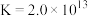
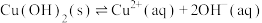
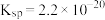
下列说法不正确的是
A.Ⅰ中产生蓝色沉淀的离子方程式为 |
B.加热蒸干Ⅰ中的深蓝色溶液,不能得到纯净的 固体 固体 |
C.Ⅱ中现象证明了 溶液和实验Ⅰ所得深蓝色溶液中,+2价铜的存在形式不同 溶液和实验Ⅰ所得深蓝色溶液中,+2价铜的存在形式不同 |
D.Ⅲ中固体完全溶解的离子方程式为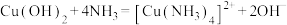 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】 的排放来自汽车尾气,研究利用反应
的排放来自汽车尾气,研究利用反应
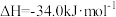 。用活性炭可对其进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如下图所示。(已知:气体分压=气体总压×物质的量分数),下列有关说法错误的是
。用活性炭可对其进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如下图所示。(已知:气体分压=气体总压×物质的量分数),下列有关说法错误的是
 的排放来自汽车尾气,研究利用反应
的排放来自汽车尾气,研究利用反应
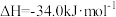 。用活性炭可对其进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如下图所示。(已知:气体分压=气体总压×物质的量分数),下列有关说法错误的是
。用活性炭可对其进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如下图所示。(已知:气体分压=气体总压×物质的量分数),下列有关说法错误的是
A.若能测得反应产生22g  ,则反应放出的热量为17.0kJ ,则反应放出的热量为17.0kJ |
| B.将炭块粉碎,可提高反应速率 |
C.在950K~1000K之间,化学反应速率: |
D.1050K时,反应的化学平衡常数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在T℃、101kPa下, 作催化剂,向反应器中充入1mol气态乙苯发生主反应I:
作催化剂,向反应器中充入1mol气态乙苯发生主反应I: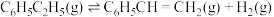 ,其平衡转化率为50%;温度,压强保持不变,以水蒸气作稀释气,还会发生如下副反应:
,其平衡转化率为50%;温度,压强保持不变,以水蒸气作稀释气,还会发生如下副反应:
II: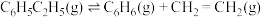
III: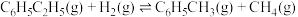
在以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S( )随乙苯转化率的变化曲线如图所示(计算时忽略副反应),下列说法错误的是
)随乙苯转化率的变化曲线如图所示(计算时忽略副反应),下列说法错误的是
 作催化剂,向反应器中充入1mol气态乙苯发生主反应I:
作催化剂,向反应器中充入1mol气态乙苯发生主反应I: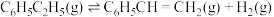 ,其平衡转化率为50%;温度,压强保持不变,以水蒸气作稀释气,还会发生如下副反应:
,其平衡转化率为50%;温度,压强保持不变,以水蒸气作稀释气,还会发生如下副反应:II:
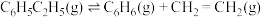
III:
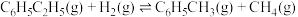
在以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S(
 )随乙苯转化率的变化曲线如图所示(计算时忽略副反应),下列说法错误的是
)随乙苯转化率的变化曲线如图所示(计算时忽略副反应),下列说法错误的是
A. 降低了乙苯脱氢反应的活化能 降低了乙苯脱氢反应的活化能 |
B.反应I的 为 为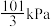 |
| C.若使反应I平衡转化率提升至75%,需向反应器中充入5mol水蒸气作稀释气 |
| D.a代表苯乙烯、b代表甲苯、c代表苯 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】相同温度下,分别在起始体积均为1L的两个密闭容器中发生反应:X2(g)+3Y2(g) 2XY3(g)△H=-akJ/mol。实验测得反应的有关数据如表。下列叙述正确的是
2XY3(g)△H=-akJ/mol。实验测得反应的有关数据如表。下列叙述正确的是
 2XY3(g)△H=-akJ/mol。实验测得反应的有关数据如表。下列叙述正确的是
2XY3(g)△H=-akJ/mol。实验测得反应的有关数据如表。下列叙述正确的是| 容器 | 反应条件 | 起始物质的量/mol | 达到平衡所用时间/min | 达平衡过程中的能量变化 | ||
| X2 | Y2 | XY3 | ||||
| ① | 恒容 | 1 | 3 | 0 | 10 | 放热0.1akJ |
| ② | 恒压 | 1 | 3 | 0 | t | 放热bkJ |
| A.对于上述反应,①、②中反应的平衡常数K的值不同 |
| B.①中:从开始至10min内的平均反应速率v(X2)=0.1mol/(L•min) |
| C.②中:X2的平衡转化率小于10% |
| D.b>0.1a |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在 温度下,向1L恒容容器中加入1molCO和
温度下,向1L恒容容器中加入1molCO和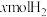 ,发生反应
,发生反应
 ,得到
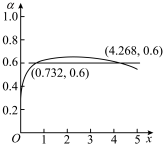
,得到 的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知
的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知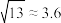 )
)
 温度下,向1L恒容容器中加入1molCO和
温度下,向1L恒容容器中加入1molCO和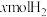 ,发生反应
,发生反应
 ,得到
,得到 的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知
的平衡转化率α随着x的变化情况如下图所示。下列说法正确的是(已知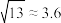 )
)
A.起始时向容器中加入 ,平衡后再加入 ,平衡后再加入 ,再次平衡时 ,再次平衡时 的转化率会减小 的转化率会减小 |
B.其他条件相同,只改变温度和 初始投料,使 初始投料,使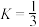 ,x=3,此时 ,x=3,此时 的平衡转化率约为56.7% 的平衡转化率约为56.7% |
C.与x=0.732相比,当x=4.268时,平衡体系中 的体积分数更小 的体积分数更小 |
D.一定温度下,向1L恒容容器中加入HI(g),使其分解达到平衡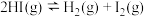 ,当HI投料量增大时,HI的平衡转化率先增大后减小 ,当HI投料量增大时,HI的平衡转化率先增大后减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】异丁烯(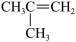 )是重要的化工原料,可由异丁醇(
)是重要的化工原料,可由异丁醇(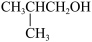 )脱水制得.异丁醇催化脱水时发生如下反应:
)脱水制得.异丁醇催化脱水时发生如下反应:
反应1(主反应):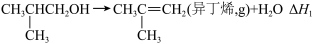
反应2(副反应):
 不变,向一定体积的密闭容器中充入
不变,向一定体积的密闭容器中充入 的混合气体(
的混合气体( 不参与反应),平衡时所得异丁醇的转化率、异丁烯的产率与温度的关系如图所示.下列说法错误的是
不参与反应),平衡时所得异丁醇的转化率、异丁烯的产率与温度的关系如图所示.下列说法错误的是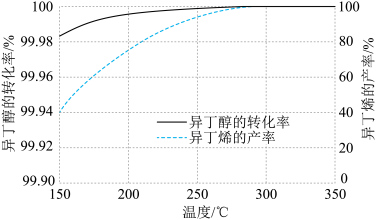
| A.反应1为消去反应,反应2为加成反应 |
| B.保持其他条件不变,升高温度,反应1和反应2平衡均向正反应方向移动 |
C.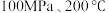 时, 时, 起始比值越小,平衡时异丁烯的产率越高 起始比值越小,平衡时异丁烯的产率越高 |
D.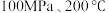 时,若起始时将 时,若起始时将 改为 改为 ,平衡时异丁烯的产率降低 ,平衡时异丁烯的产率降低 |
您最近一年使用:0次
【推荐1】向三个体积均为3 L的恒容绝热容器中,按不同方式投入反应物,500 ℃条件下开始发生如下反应:H2(g)+Br2(g)  2HBr(g) ΔH<0,测得达平衡时有关数据如下:
2HBr(g) ΔH<0,测得达平衡时有关数据如下:
下列说法正确的是
 2HBr(g) ΔH<0,测得达平衡时有关数据如下:
2HBr(g) ΔH<0,测得达平衡时有关数据如下:容器 | Ⅰ | Ⅱ | Ⅲ |
反应物投入量 | 1 mol H2、1 mol Br2 | 2 mol HBr | 2 mol H2、2 mol Br2 |
平衡时正反应速率 | v1 | v2 | v3 |
平衡常数 | K1 | K2 | K3 |
平衡时H2的物质的量 | n1 | n2 | n3 |
反应物的转化率 | α1 | α2 | α3 |
| A.v1=v2 | B.K1=K3 |
| C.n1>n2 | D.α1+α2>1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在温度相同、容积均为2L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
(已知N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ·mol-1)
(已知N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ·mol-1)
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol N2、6mol H2 | 2mol NH3 |
| NH3的浓度( mol·L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2p1=2p3<p2 |
| B.α2+α3<1 |
| C.达到平衡时乙容器中NH3的体积分数最大 |
| D.Q3+Q1>92.4 |
您最近一年使用:0次

 制
制 的平衡体系中存在如下反应:
的平衡体系中存在如下反应: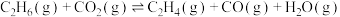

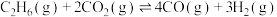
 条件下)与温度、压强的关系如图所示。已知:乙烯的选择性
条件下)与温度、压强的关系如图所示。已知:乙烯的选择性 。下列说法错误的是
。下列说法错误的是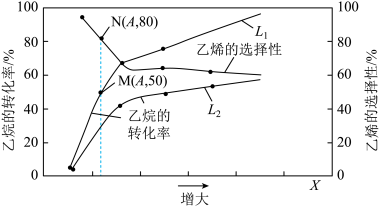
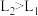
 、
、
 、
、 、
、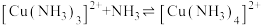 ,平衡常数依次为
,平衡常数依次为 已知
已知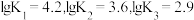 ,体系中含Cu物种的组分分布系数δ与
,体系中含Cu物种的组分分布系数δ与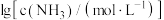 的关系如图所示,N点的横坐标为-2.2,δ(x)=
的关系如图所示,N点的横坐标为-2.2,δ(x)=  。下列说法错误的是
。下列说法错误的是
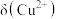 的变化曲线
的变化曲线
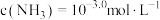 时,
时,


