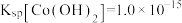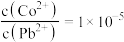某小组欲制备配离子 ,实验如下。
,实验如下。
已知: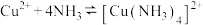
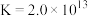
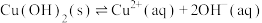
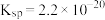
下列说法不正确的是
 ,实验如下。
,实验如下。| 序号 | 步骤 |
| Ⅰ | 向2mL 溶液中滴加0.5mL 溶液中滴加0.5mL 氨水,产生蓝色沉淀;继续滴加约1.5mL氨水,沉淀完全溶解,得到深蓝色溶液 氨水,产生蓝色沉淀;继续滴加约1.5mL氨水,沉淀完全溶解,得到深蓝色溶液 |
| Ⅱ | 分别向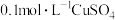 溶液和实验Ⅰ所得深蓝色溶液中加入光亮的铁钉;1min后,前者铁钉表面有红色物质析出,后者铁钉无现象 溶液和实验Ⅰ所得深蓝色溶液中加入光亮的铁钉;1min后,前者铁钉表面有红色物质析出,后者铁钉无现象 |
| Ⅲ | 取0.1g氢氧化铜固体于试管中,加入5mL 氨水,溶液略变为蓝色,固体未见明显溶解;滴加2滴饱和氯化铵溶液,固体完全溶解,得到深蓝色溶液 氨水,溶液略变为蓝色,固体未见明显溶解;滴加2滴饱和氯化铵溶液,固体完全溶解,得到深蓝色溶液 |
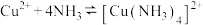
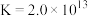
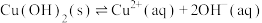
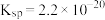
下列说法不正确的是
A.Ⅰ中产生蓝色沉淀的离子方程式为 |
B.加热蒸干Ⅰ中的深蓝色溶液,不能得到纯净的 固体 固体 |
C.Ⅱ中现象证明了 溶液和实验Ⅰ所得深蓝色溶液中,+2价铜的存在形式不同 溶液和实验Ⅰ所得深蓝色溶液中,+2价铜的存在形式不同 |
D.Ⅲ中固体完全溶解的离子方程式为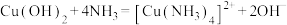 |
更新时间:2024-05-24 16:34:57
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】工业上可通过甲醇羰基化法制取甲酸甲酯(HCOOCH3):CH3OH(g)+CO(g)⇌HCOOCH3 (g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示,下列说法正确的是
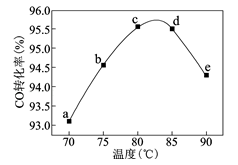

| A.a→c,CO的转化率随温度的升高而增大的原因是因为该反应是吸热反应,升高温度反应正向移动 |
| B.平衡常数Kb<Kd,由图可知生产时反应温度控制在80~85℃为宜 |
| C.向该容器中充入N2,CH3OH的转化率增大 |
| D.反应速率υb<υd |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在恒压条件下化学反应:2SO2(g)+O2(g)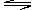 2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
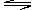 2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是
2SO3(g);ΔH=-Q kJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列。判断下列叙述正确的是| 容器 | SO2(mol) | O2(mol) | SO3(mol) | N2(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | 0 | Q2 |
| 丙 | 0 | 0 | 2 | 0 | Q3 |
| 丁 | 1 | 0.5 | 0 | 1 | Q4 |
| A.平衡时,向甲容器中再加1mol O2,一段时间后达到平衡时O2的体积分数减小 |
| B.平衡时,升高丙容器温度,正反应速率增大,逆反应速率减小,平衡逆向移动 |
| C.各容器中反应放出热量的关系为:Q1=2Q2>2Q4 |
| D.丁容器中反应达到平衡时,其化学平衡常数小于乙容器中反应的平衡常数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】不能正确表示下列反应的离子方程式是
A.将少量溴水滴入过量 溶液中: 溶液中: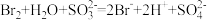 |
B.将足量 溶液滴入 溶液滴入 浊液中: 浊液中: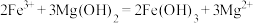 |
C.将过量 通入 通入 溶液中: 溶液中: |
D.将葡萄糖溶液与足量银氨溶液共热: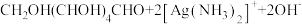  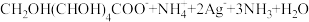 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】有关下列说法中,正确的是
| A.用标准盐酸滴定未知浓度的NaOH溶液,滴定前酸式滴定管尖嘴有气泡未排出,滴定后气泡消失,会造成测定结果偏低。 |
| B.工业废水中的Cu2+、Hg2+等重金属阳离子可以通过加入FeS除去 |
| C.在米汤中加入食盐,可以检验食盐中是否加碘 |
| D.等体积的pH均为2的酸HA和HB的溶液分别与足量的铁粉反应,HA放出的H2多,说明HA酸性强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】氯化银(AgCl,白色)、铬酸银( ,砖红色)都是难溶电解质。T℃下,将
,砖红色)都是难溶电解质。T℃下,将 溶液分别逐滴滴入体积均为10mL、浓度均为
溶液分别逐滴滴入体积均为10mL、浓度均为 的NaCl溶液和
的NaCl溶液和 溶液中,所得的沉淀溶解平衡图像如图所示(X为
溶液中,所得的沉淀溶解平衡图像如图所示(X为 或
或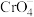 )。下列叙述正确的是
)。下列叙述正确的是
 ,砖红色)都是难溶电解质。T℃下,将
,砖红色)都是难溶电解质。T℃下,将 溶液分别逐滴滴入体积均为10mL、浓度均为
溶液分别逐滴滴入体积均为10mL、浓度均为 的NaCl溶液和
的NaCl溶液和 溶液中,所得的沉淀溶解平衡图像如图所示(X为
溶液中,所得的沉淀溶解平衡图像如图所示(X为 或
或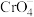 )。下列叙述正确的是
)。下列叙述正确的是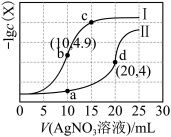
A.T℃下,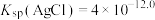 |
B.曲线Ⅱ表示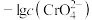 与V( 与V( 溶液)的变化关系 溶液)的变化关系 |
| C.向a点对应的体系中加入少量NaCl固体,白色固体逐渐变为砖红色 |
D.浓度均为 的 的 和 和 ,可通过分步沉淀进行分离 ,可通过分步沉淀进行分离 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是
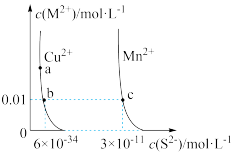
| A.在含有CuS和MnS固体的溶液中c(Cu2+)∶c(Mn2+)=1∶2×10-23 |
| B.向CuSO4溶液中加入MnS发生反应: Cu2+(aq)+MnS(s) |
| C.a点对应的Ksp等于b点对应的Ksp |
| D.该温度下,Ksp(CuS)小于Ksp(MnS) |
您最近一年使用:0次

 发生反应:
发生反应: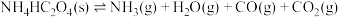 ,实验数据如表所示。
,实验数据如表所示。 )
)

 浓度均为
浓度均为 )进行实验:滴加一定量
)进行实验:滴加一定量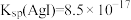 、
、 。下列分析
。下列分析 ,白色沉淀是
,白色沉淀是

 )
)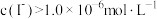
 CuS(s)+Mn2+(aq)
CuS(s)+Mn2+(aq) ,
,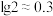 。常温下在含大量
。常温下在含大量 和
和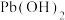 的浊液中滴加
的浊液中滴加 溶液,浊液中
溶液,浊液中 [
[ ,
, 、
、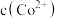 、
、 ]与
]与 关系如图,平衡常数K大于或等于
关系如图,平衡常数K大于或等于 时认为反应不可逆(即完全反应),下列叙述正确的是
时认为反应不可逆(即完全反应),下列叙述正确的是
 直线代表
直线代表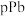 和
和