将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
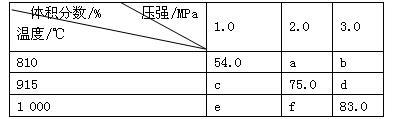
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。下列说法错误的是
| A.a<54.0 |
| B.b> f |
| C.915 ℃,2.0 MPa时E的转化率为60% |
| D.K(1000 ℃)>K(810 ℃) |
更新时间:2016-12-09 08:30:50
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在工业生产上通常利用硫(S8)与CH4为原料制备CS2,主要发生以下两个反应: 反应I:S8(g)=4S2(g);反应II:2S2(g)+CH4(g)  CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法
CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法不正确 的是
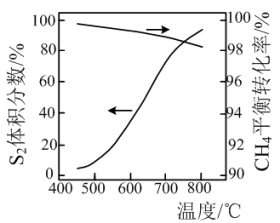
 CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法
CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法
| A.反应II的正反应为放热反应 |
| B.某温度下若S8完全分解成S2,在恒容密闭容器中,n(S2)∶n(CH4)=2∶1开始反应,当CS2体积分数为10%时,CH4转化率为60% |
| C.通过增大S8的浓度可以提高CH4的转化率 |
| D.制备CS2时温度需高于600℃的原因是:此温度CH4平衡转化率已很高,低于此温度,S2浓度小,反应速率慢 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
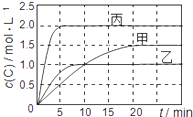
下列说法正确的是
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 1L | 1L | 2L |
| 温度 | T1 | T2 | T2 |
| 反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
| A.由图可知:T1<T2,且该反应为吸热反应 |
| B.T1时该反应的平衡常数K=7.2 |
| C.前10min甲、乙、丙三个容器中A的平均反应速率:v(A)乙<v(A)甲<v(A)丙 |
| D.平衡时A的质量m:m乙<m甲<m丙 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】 在电子、光学和催化剂领域有广泛应用,设计通过
在电子、光学和催化剂领域有广泛应用,设计通过 制备
制备 和
和 制备
制备 的反应原理分别如下:I.
的反应原理分别如下:I.

Ⅱ.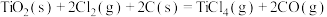
 。
。
下列说法错误的是
 在电子、光学和催化剂领域有广泛应用,设计通过
在电子、光学和催化剂领域有广泛应用,设计通过 制备
制备 和
和 制备
制备 的反应原理分别如下:I.
的反应原理分别如下:I.

Ⅱ.
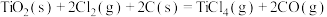
 。
。下列说法错误的是
| A.反应I能自发进行主要是焓减驱动 |
| B.反应I的体系中加入碳粉,可改变反应进行的方向 |
| C.反应Ⅱ正反应的活化能比逆反应的活化能大 |
D.减小压强和降低温度,会降低反应Ⅱ的速率,但可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】向体积均为1L的两个恒容密闭容器中分别加入足量X(s)和0.1molY(g),发生反应X(s)+Y(g) G(g)+W(g) △H,其中甲为绝热过程,乙为恒温过程,两个反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
G(g)+W(g) △H,其中甲为绝热过程,乙为恒温过程,两个反应体系的压强随时间的变化曲线如图所示。下列说法错误的是

 G(g)+W(g) △H,其中甲为绝热过程,乙为恒温过程,两个反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
G(g)+W(g) △H,其中甲为绝热过程,乙为恒温过程,两个反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
| A.△H>0 |
| B.单位时间内,气体压强变化较大的是曲线乙 |
| C.气体的总物质的量:na<nb |
| D.b点平衡常数K>0.05mol•L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列图示与对应的叙述相符的是


| A.图1表示将SO2气体通入溴水中,所得溶液的pH变化 |
| B.图2表示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀的物质的量与盐酸体积的关系 |
| C.图3表示常温下,向0.1000mol•L-1HCl溶液中滴加20.00mL 0.1000mol•L-1氨水的滴定曲线 |
| D.图4表示乙醇的催化氧化反应中速率随温度的变化图像,升高温度该反应的平衡常数减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】某温度下,在密封石英管内完全充满 的
的 水溶液,使
水溶液,使 分解,分解产物均完全溶于水.含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式).
分解,分解产物均完全溶于水.含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式).
已知在密封石英管中发生如下反应:(Ⅰ)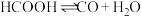 (快);(Ⅱ)
(快);(Ⅱ) (慢).
(慢).
研究发现:在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催化加速作用;反应Ⅰ的速率远大于反应Ⅱ,可以近似认为反应Ⅰ达到平衡后始终处于平衡状态(忽略水电离,其浓度视为常数).
仅对反应Ⅰ有催化加速作用;反应Ⅰ的速率远大于反应Ⅱ,可以近似认为反应Ⅰ达到平衡后始终处于平衡状态(忽略水电离,其浓度视为常数).
则以下说法错误的是

 的
的 水溶液,使
水溶液,使 分解,分解产物均完全溶于水.含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式).
分解,分解产物均完全溶于水.含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式).已知在密封石英管中发生如下反应:(Ⅰ)
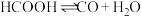 (快);(Ⅱ)
(快);(Ⅱ) (慢).
(慢).研究发现:在反应Ⅰ、Ⅱ中,
 仅对反应Ⅰ有催化加速作用;反应Ⅰ的速率远大于反应Ⅱ,可以近似认为反应Ⅰ达到平衡后始终处于平衡状态(忽略水电离,其浓度视为常数).
仅对反应Ⅰ有催化加速作用;反应Ⅰ的速率远大于反应Ⅱ,可以近似认为反应Ⅰ达到平衡后始终处于平衡状态(忽略水电离,其浓度视为常数).则以下说法错误的是

A.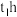 时刻反应I达到平衡状态 时刻反应I达到平衡状态 |
B.反应Ⅰ的活化能 小于反应Ⅱ的活化能 小于反应Ⅱ的活化能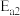 |
C.若反应起始时,向溶液中加入盐酸提高 ,则 ,则 的浓度峰值点可能变为b点 的浓度峰值点可能变为b点 |
D.若增大密封管的体积,仍按上述操作进行实验,达到新平衡时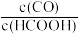 的值不变 的值不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将NO2装入带活塞的密闭容器中,当反应2NO2(g)⇌N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是
| A.恒温恒压时,充入少量惰性气体,平衡向右移动,混合气体的颜色变浅 |
| B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅 |
| C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 |
| D.恒温恒容时,充入少量惰性气体,压强增大,平衡向右移动,混合气体的颜色变浅 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:
①v1<v2 ②v1<v3 ③c2<2c1 ④c2>2c3 ⑤p2>2p3 ⑥p2<2p1 ⑦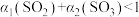 ⑧
⑧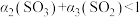 ⑨
⑨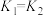 ⑩
⑩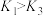
以上说法正确的有
 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2mol 、1mol 、1mol | 4mol | 2mol 、1mol 、1mol |
平衡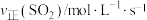 | v1 | v2 | v3 |
平衡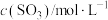 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率 | 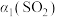 | 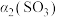 | 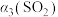 |
| 平衡常数K | 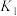 | 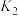 |  |
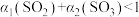 ⑧
⑧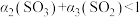 ⑨
⑨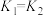 ⑩
⑩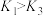
以上说法正确的有
| A.6 | B.7 | C.8 | D.9 |
您最近一年使用:0次

 ,按投料比
,按投料比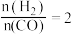 将
将 与
与 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得
 ,
,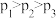
 、
、 压强下,Q点对应的
压强下,Q点对应的


