下列叙述中正确的是
| A.石蕊、酚酞、甲基橙均能用作中和滴定的指示剂 |
| B.25°C时,pH=12的溶液一定是碱溶液 |
| C.等温下,AgCl在浓度均为0.1 mol·L-1的NaCl溶液、MgCl2溶液中Ksp相等 |
| D.等温下,饱和溶液的导电能力, BaCO3强于BaSO4,则Ksp(BaCO3)<Ksp (BaSO4) |
更新时间:2020-09-16 09:53:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,向20.00mL0.1000 盐酸中滴加0.1000
盐酸中滴加0.1000 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知:①
NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知:① ;②甲基红是一种常用的酸碱指示剂,其pH在4.4~6.2区间时呈橙色,
;②甲基红是一种常用的酸碱指示剂,其pH在4.4~6.2区间时呈橙色, 时呈红色,
时呈红色,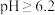 时呈黄色。下列说法不正确的是
时呈黄色。下列说法不正确的是

 盐酸中滴加0.1000
盐酸中滴加0.1000 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知:①
NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知:① ;②甲基红是一种常用的酸碱指示剂,其pH在4.4~6.2区间时呈橙色,
;②甲基红是一种常用的酸碱指示剂,其pH在4.4~6.2区间时呈橙色, 时呈红色,
时呈红色,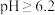 时呈黄色。下列说法不正确的是
时呈黄色。下列说法不正确的是
| A.滴定时,边摇动锥形瓶边观察锥形瓶中溶液的颜色变化 |
| B.NaOH与盐酸恰好完全反应时,pH=7 |
| C.选择甲基红指示反应终点,误差比甲基橙的大 |
| D.V(NaOH)=30.00mL时,所得溶液的pH=12.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】为测定某样品中 含量,取
含量,取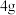 配成
配成 溶液(杂质不溶解),再用该溶液滴定
溶液(杂质不溶解),再用该溶液滴定
 盐酸,并用酚酞作为指示剂。下图是该滴定过程的滴定曲线。下列说法错误的是
盐酸,并用酚酞作为指示剂。下图是该滴定过程的滴定曲线。下列说法错误的是
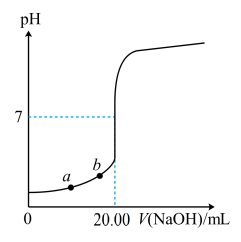
 含量,取
含量,取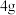 配成
配成 溶液(杂质不溶解),再用该溶液滴定
溶液(杂质不溶解),再用该溶液滴定
 盐酸,并用酚酞作为指示剂。下图是该滴定过程的滴定曲线。下列说法错误的是
盐酸,并用酚酞作为指示剂。下图是该滴定过程的滴定曲线。下列说法错误的是
| A.该反应还可以用甲基橙做指示剂 |
| B.溶液由无色变为浅红色且一段时间不褪色时为滴定终点 |
C.碱式滴定管用蒸馏水洗净后未润洗,则c( )偏大 )偏大 |
| D.NaOH的质量分数为62.5% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀 | 该溶液中一定含有 |
| B | 用pH试纸测定浓度均为0.1mol·L-1HCOONa溶液与CH3COONa溶液的pH,CH3COONa溶液的pH较大 | CH3COOH电离出H+的能力比HCOOH的强 |
| C | 向0.1mol·L-1H2O2溶液中滴加0.1mol·L-1KMnO4溶液,溶液褪色并放出能使带火星木条复燃的气体 | H2O2具有氧化性 |
| D | 向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1AgNO3溶液,振荡,出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是
| A.X的简单氢化物的热稳定性比W的强 |
| B.Y的简单离子与X的具有相同的电子层结构 |
| C.Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红 |
| D.Z与X属于同一主族,与Y属于同一周期 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列对实验操作和现象的解释与结论错误的是
| 操作和现象 | 解释与结论 | |
| A | 25℃,测得可溶性正盐MR溶液的pH=7 | MR为强酸强碱盐 |
| B | 向FeCl3溶液中滴加过量的KI溶液,充分反应后滴入KSCN溶液,溶液变为红色 | KI与FeCl3的反应是可逆反应 |
| C | 向淀粉溶液中加适量稀H2SO4溶液,加热4~5min,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液不变蓝 | 淀粉酸性条件下水解完全 |
| D | 向饱和NaHCO3溶液中滴加饱和CaCl2溶液,先有白色沉淀产生,后生成无色气泡 | Ca2+与CO 结合,破坏HCO 结合,破坏HCO 的电离平衡,溶液中H+浓度增大,与HCO 的电离平衡,溶液中H+浓度增大,与HCO 反应产生气体 反应产生气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】HX为一元弱酸,YOH为一元强碱。常温下,向难溶强电解质(YX)的悬浊液中加入某酸,测得c(Y+)与c(H+)的变化关系如图实线所示。下列说法错误的是
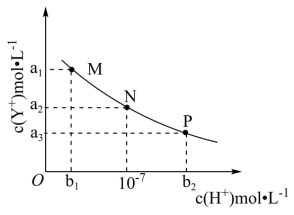

| A.M点时,c(X-)<c(Y+) |
| B.水的电离程度:N>P |
| C.实验时可加入的酸为盐酸 |
| D.难溶物YX的溶度积K为a22 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验及其结论都正确的是( )
| 实验 | 结论 | |
| A. | 氯气的水溶液可以导电 | 氯气是电解质 |
| B. | 室温下,用pH试纸测定浓度均为0.1 mol·L-1的NaClO溶液和CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| C. | 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性HA比HB弱 |
| D. | 10mL 1mol·L-1的AgNO3溶液中先滴加1mol·L-1的NaCl溶液1mL,再滴加1mol·L-1的NaI溶液1 mL,先产生白色沉淀后沉淀变为黄色 | Ksp(AgI)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断正确的是
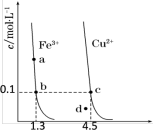

| A.升温可使溶液由a点变到b点 |
B.Ksp[Cu(OH)2]=1.0 10-20 10-20 |
| C.c点变成d点,可以往溶液中加少许Cu(OH)2固体 |
| D.FeCl3溶液中含有少量Cu2+,可以通过调节溶液pH除去 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作、实验现象以及所得出的结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向1mL2mol/LNaOH溶液中先滴加2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液,振荡 | 先生成白色沉淀,后生成红褐色沉淀 | Ksp[Mg(OH)2]<Ksp[Fe(OH)3] |
| B | 将甲烷与氯气按体积比1:4混合于试管中光照 | 反应后的混合气体能使湿润的石试纸变红 | 生成的氯代甲烷具有酸性 |
| C | 将木炭和浓硫酸共热生成的气体通入澄清石灰水中 | 澄清石灰水变浑浊 | 该气体只含CO2 |
| D | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该溶液中可能含有SO42- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 标准溶液滴定草酸时,
标准溶液滴定草酸时, 的吸光度(A)与溶液中的
的吸光度(A)与溶液中的 成正比,其标准曲线如图所示。常温时,测得
成正比,其标准曲线如图所示。常温时,测得 饱和溶液
饱和溶液
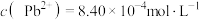
 的数量级为
的数量级为


